
Philippe Nguy1,2,3, Pharm.D., M.Sc., Adrian Maxim1,3,4, Pharm.D., M.Sc., Gabriel Dorais1,4,5, Pharm.D., M.Sc., Qian Du1,6,7, Pharm.D., M.Sc.
1Candidat à la maîtrise en pharmacothérapie avancée au moment de la rédaction de l’article, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
2Résident en pharmacie, Centre universitaire de santé McGill, Montréal (Québec) Canada;
3Pharmacien, Hôpital général juif Sir Mortimer B. Davis, Montréal (Québec) Canada;
4Résident en pharmacie, Hôpital général juif Sir Mortimer B. Davis, Montréal (Québec) Canada;
5Pharmacien, Centre hospitalier universitaire de Sherbrooke, Sherbrooke (Québec) Canada;
6Résident en pharmacie, Centre hospitalier de l’Université de Montréal, Montréal (Québec) Canada;
7Pharmacien, Centre hospitalier de l’Université de Montréal, Montréal (Québec) Canada
Reçu le 6 septembre 2016; Accepté après révision par les pairs le 21 décembre 2016
Titre de l’article : A randomized trial of intensive versus standard blood-pressure control. N Engl J Med 2015;373:2103-161.
Auteurs : Wright JT, Williamson JD, Whelton PK, Snyder JK, Sink KM, Rocco MV et coll.
Commanditaires : Cette étude a été commanditée par le National Heart, Lung and Blood Institute en collaboration avec le National Institute of Diabetes and Digestive and Kidney Diseases, le National Institute of Neurological Disorders and Stroke et le National Institute on Aging. Les compagnies pharmaceutiques Takeda Pharmaceuticals International et Arbor Pharmaceuticals ont fourni gratuitement les médicaments azilsartan et azilsartan en combinaison avec la chlorthalidone.
Cadre de l’étude : L’hypertension artérielle est une maladie prévalente principalement dans la population adulte. Selon les plus récentes données statistiques au Canada, un adulte sur cinq en souffre actuellement2. L’élévation de la pression artérielle systolique est un facteur de risque indépendant de maladies cardiovasculaires et de mortalité, et cette relation est d’autant plus significative à mesure que la pression artérielle systolique d’un patient augmente3,4.
La littérature médicale démontre que le traitement de l’hypertension réduit les risques d’évènements cardiovasculaires5–10. Actuellement, la thérapie antihypertensive est basée sur l’atteinte de cibles thérapeutiques. Ces cibles sont généralement fixées selon des consensus d’experts et tentent de prédire le seuil de pression artérielle à partir duquel un patient retirera plus de bénéfices que de risques de son traitement11. Jusqu’à maintenant, faute de données probantes, les études ciblant les différentes populations n’ont pas pu clairement définir ce seuil11. À cet effet, les études à répartition aléatoire et contrôlées n’abordent que les bénéfices du traitement visant la pression artérielle systolique inférieure à 150 mmHg, avec des données limitées concernant des cibles inférieures9,10,12–15. Dans ces circonstances, le National Heart, Lung and Blood Institute a émis, en 2007, l’hypothèse qu’une pression artérielle systolique inférieure à 120 mmHg pourrait diminuer la morbidité et mortalité cardiovasculaires16. Deux essais cliniques importants, soit SPRINT et ACCORD-BP, sont partis de cette hypothèse1,17.
Cependant, les résultats de l’étude ACCORD-BP ont remis en question l’atteinte des cibles inférieures de pression artérielle ainsi que l’hypothèse décrite ci-dessus17. À la suite de la comparaison d’un contrôle intensif de la pression artérielle systolique (moins de 120 mmHg) à un contrôle standard (moins de 140 mmHg) chez les patients diabétiques de type 2, les résultats obtenus n’ont démontré aucune différence statistiquement significative quant à l’incidence d’évènements cardiovasculaires et de mortalité17.
Ces données ont contribué au fait qu’au cours des dernières années, plusieurs lignes directrices portant sur le traitement de l’hypertension ont augmenté leur cible de pression artérielle systolique à 130 ou 140 mmHg pour la population à haut risque18–21. Les lignes directrices américaines ont même établi une cible de pression artérielle systolique à 150 mmHg pour les patients dont l’âge est égal ou supérieur à 60 ans, une décision controversée, alors que les lignes directrices canadiennes, européennes et du National Institute for Health and Clinical Excellence (NICE) ne recommandent cette cible qu’à partir de 80 ans8,18–20.
Bref, l’étude SPRINT découle de la volonté d’obtenir davantage de données objectives sur la cible de pression artérielle systolique à viser pour une population non diabétique, âgée d’au moins 50 ans. L’objectif principal de l’étude était donc d’évaluer si un contrôle intensif avec une valeur de pression artérielle systolique inférieure à 120 mmHg était plus efficace qu’un contrôle standard visant une pression artérielle systolique inférieure à 140 mmHg afin de réduire l’incidence des évènements cardiovasculaires graves dans cette population.
Protocole de recherche : Il s’agit d’une étude clinique multicentrique (102 sites cliniques aux États-Unis) à répartition aléatoire et stratifiée selon le site, sans insu et dont la phase de recrutement s’est étendue entre novembre 2010 et mars 2013. Les participants et le personnel de soutien de l’étude étaient au courant du groupe assigné, mais l’analyse des objectifs a été effectuée à l’aveugle par un comité d’évaluateurs. En supposant un taux d’évènements par année de 2,2 % dans le groupe soumis à un traitement standard visant une pression systolique inférieure à 140 mmHg, les auteurs estimaient obtenir une puissance de 88,7 % avec une taille d’échantillon de 9250 sujets afin de détecter une réduction relative de 20 % du taux d’évènements de l’objectif composite primaire entre les deux groupes à l’étude.
Patients : Les principaux critères d’inclusion et d’exclusion sont détaillés dans le tableau I.
Tableau I Critères d’admissibilité

Ainsi, les sujets participant à l’étude devaient être âgés de 50 ans au minimum, avoir une pression artérielle systolique entre 130 et 180 mmHg et avoir au moins un facteur de risque d’évènements cardiovasculaires parmi les suivants : présence d’une maladie cardiovasculaire clinique ou subclinique autre qu’un accident vasculaire cérébral (voir tableau I), une insuffisance rénale chronique avec un débit de filtration glomérulaire estimé entre 20 et 59 mL/min/1,73 m2 selon l’équation modification of diet in renal disease (MDRD), un risque de maladie cardiovasculaire d’au moins 15 % à 10 ans selon le score de Framingham ou un âge égal ou supérieur à 75 ans.
Les participants atteints de diabète ainsi que ceux ayant un antécédent d’accident vasculaire cérébral, une insuffisance cardiaque symptomatique et ceux vivant en institution étaient exclus de l’étude. Tous les patients ont fourni un consentement écrit.
Interventions : Les participants ont été répartis de façon aléatoire dans l’un des deux groupes, soit un « traitement intensif » pour atteindre une pression artérielle systolique inférieure à 120 mmHg ou un « traitement standard » avec une cible inférieure à 140 mmHg. Cette répartition aléatoire n’a cependant pas été faite à l’aveugle, et les participants étaient au courant du groupe assigné. Les deux groupes bénéficiaient d’un enseignement sur des modifications à apporter à leurs habitudes de vie, portant entres autres sur la diète dietary approaches to stop hypertension (DASH), le contrôle du poids, l’activité physique et la cessation tabagique. Une fois la répartition effectuée, la thérapie antihypertensive initiale était ajustée selon le groupe assigné, en fonction d’un algorithme prédéterminé et d’un formulaire listant les médicaments antihypertenseurs fournis. Les prescripteurs pouvaient toutefois déroger à cette liste selon leur jugement clinique. Le protocole encourageait les prescripteurs à choisir les classes de médicaments antihypertenseurs qui avaient démontré le plus de bénéfices dans les études évaluant les objectifs cardiovasculaires selon les lignes directrices cliniques.
Le suivi des deux groupes de traitement était effectué tous les mois pendant les trois premiers mois et, par la suite, tous les trois mois. Toutefois, les suivis mensuels se poursuivaient au-delà des trois premiers mois pour les participants du groupe intensif jusqu’à l’obtention d’une pression artérielle systolique inférieure à 120 mmHg ou jusqu’à l’arrêt de la titration de la thérapie médicamenteuse. Quant au groupe visant une cible inférieure à 140 mmHg, des visites mensuelles supplémentaires étaient organisées seulement si la pression était supérieure à 160 mmHg. Toutefois, la thérapie antihypertensive était ajustée à la baisse lorsque la pression obtenue était inférieure à 135 mmHg lors de deux visites consécutives ou inférieure à 130 mmHg lors d’une seule visite.
Dans les deux groupes de traitement, une moyenne de trois valeurs de pression artérielle mesurées au repos pendant cinq minutes et effectuées à l’aide d’un tensiomètre automatisé était utilisée comme indicateur guidant l’ajustement de la thérapie antihypertensive lors des visites de suivi.
Points évalués : L’objectif primaire évalué dans l’étude était une variable composite des évènements suivants : un infarctus du myocarde, un syndrome coronarien aigu autre qu’un infarctus, un accident vasculaire cérébral, une décompensation aiguë d’une insuffisance cardiaque ou un décès d’origine cardiovasculaire.
Les objectifs secondaires évalués portaient sur les évènements cardiovasculaires et rénaux. Chacun des évènements inclus dans l’objectif primaire de même que la survenue d’un décès toutes causes confondues étaient analysés individuellement. De plus, un objectif utilisant un critère d’évaluation combiné incluant la survenue d’un évènement de l’objectif principal et du décès toutes causes confondues était également évalué. Pour les participants souffrant d’insuffisance rénale chronique à la base (débit de filtration glomérulaire estimé inférieur à 60 mL/min/1,73 m2 selon l’équation MDRD), l’objectif rénal secondaire se composait d’une diminution d’au moins 50 % du débit de filtration glomérulaire estimé ou de la survenue d’une insuffisance rénale terminale nécessitant une dialyse à long terme ou une transplantation. Quant à ceux n’ayant pas d’atteinte rénale initiale, l’objectif évalué était une diminution du débit de filtration glomérulaire estimé de 30 % ou plus menant à une valeur inférieure à 60 mL/min/1,73 m2.
Résultats : Un total de 9361 participants sur les 14 692 évalués répondaient aux critères d’inclusion dans l’étude. La répartition aléatoire est la suivante : 4678 participants ont participé au traitement intensif et 4683, au traitement comparateur. Le tableau II présente les caractéristiques initiales des participants. Les deux groupes étaient similaires à l’exception du taux d’utilisation d’une statine qui était supérieur dans le groupe du traitement standard (44,7 % comparativement à 42,6 %, p = 0,04). La moyenne d’âge était de 68 ans, et l’indice de masse corporelle moyen, de 30 kg/m2. Il faut aussi noter qu’il n’y avait approximativement que 35 % de femmes dans les deux groupes et que 90 % des participants étaient déjà sous traitement antihypertenseurs avec une moyenne de 1,8 antihypertenseurs par participant dans chaque groupe.
Tableau II Caractéristiques démographiques et cliniques de la population au début de l’étudea

Au total, 489 (10,5 %) participants du groupe du traitement intensif et 497 (10,6 %) du groupe du traitement standard n’ont pas terminé l’étude. L’analyse des résultats en intention de traiter a permis malgré tout d’inclure ces participants. En raison d’une différence de mortalité globale significative entre les deux groupes lors d’une analyse intermédiaire, l’étude a été interrompue prématurément. Le temps de suivi médian de l’étude aura été de 3,26 années, alors que les auteurs prévoyaient au départ une moyenne de cinq ans sur un maximum de six ans.
Pendant la durée de l’étude, la pression artérielle systolique moyenne a été de 121,5 mmHg pour le groupe du traitement intensif et de 134,6 mmHg pour celui du traitement standard. De plus, le nombre moyen de médicaments antihypertenseurs prescrits par participant était de 2,8 pour le traitement intensif comparativement à 1,8 pour le traitement standard. Les principaux résultats de l’étude sont présentés dans le tableau III.
Tableau III Principaux résultats de l’étudea
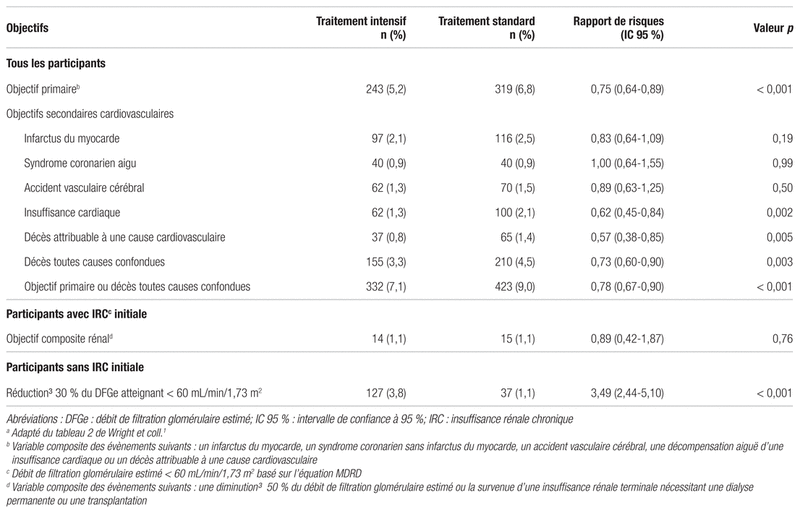
La première occurrence d’un élément composant l’objectif primaire, soit un infarctus du myocarde, un syndrome coronarien aigu autre qu’un infarctus, un accident vasculaire cérébral, une décompensation aiguë d’une insuffisance cardiaque ou un décès d’origine cardiovasculaire s’est confirmée chez 243 participants (1,65 % par an) dans le groupe de traitement intensif et 319 participants (2,19 % par an) dans le groupe de traitement standard. Cette diminution du taux d’incidence de l’objectif primaire ainsi que du décès toutes causes confondues a été constante dans tous les sous-groupes prédéterminés des participants dans le groupe de traitement intensif. Il faut noter que les patients souffrant d’insuffisance rénale, ceux âgés de moins de 75 ans, les femmes, les patients de race noire, ceux atteints d’une maladie cardiovasculaire et ceux avec une pression systolique supérieure à 132 mmHg n’ont pas démontré de résultats statistiquement significatifs lors de l’analyse par sous-groupes.
Comparativement au traitement standard, le traitement intensif présente une diminution statistiquement significative du nombre d’événements associés à l’objectif primaire (respectivement 5,2 % comparativement à 6,8 %, p < 0,001). Parmi les éléments qui composent l’objectif primaire, les seules différences statistiquement significatives portaient sur la prévention de l’insuffisance cardiaque (1,3 % comparativement à 2,1 %, p = 0,002) et du décès cardiovasculaire (0,8 % comparativement 1,4 %, p = 0,005). La prévention de l’infarctus du myocarde (2,1 % comparativement à 2,5 %, p = 0,19), du syndrome coronarien aigu autre que de l’infarctus (0,9 % dans les deux groupes, p = 0,99) ainsi que de l’accident vasculaire cérébral (1,3 % comparativement à 1,5 %, p = 0,50) n’a pas démontré de différence statistiquement significative.
Concernant les objectifs secondaires rénaux, une détérioration de la fonction rénale a été constatée chez les participants ne souffrant pas d’insuffisance rénale à la base dans le groupe de traitement intensif (3,8 % comparativement à 1,1 % pour le groupe de traitement standard, rapport de risques instantané [HR]: 3,49, p < 0,001). Aucune différence statistiquement significative n’a été observée parmi les participants qui souffraient déjà d’une insuffisance rénale chronique.
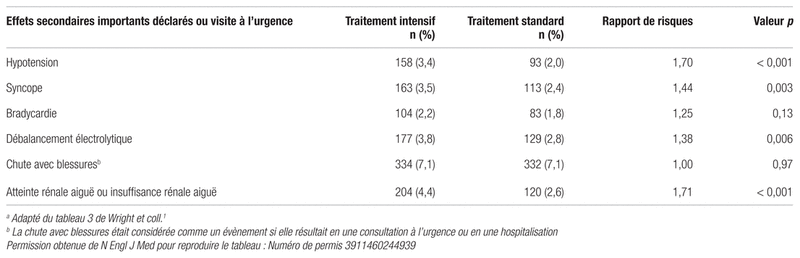
Quant à l’innocuité, 1793 (38,3 %) participants du groupe de traitement intensif ont subi des effets indésirables importants comparativement à 1736 (37,1 %) du groupe de traitement standard (HR: 1,04, p = 0,25). De ce nombre, 220 (4,7 %) participants du groupe intensif ont subi des effets secondaires possiblement ou réellement liés au traitement comparativement à 118 (2,5 %) dans le groupe recevant le traitement standard (HR: 1,88, p < 0,001). Le risque d’hypotension orthostatique asymptomatique (sans étourdissements), mesuré lors d’une visite clinique, avait significativement augmenté dans le groupe de traitement standard (HR: 0,88, p = 0,01). Toutefois, le risque d’hypotension qualifiée de sévère par les investigateurs ou ayant nécessité une visite à l’urgence avait augmenté dans le groupe de traitement intensif comparativement au groupe de traitement standard (HR: 1,70, p < 0,001). Le risque de syncope avait également augmenté dans le groupe à traitement intensif (HR: 1,44, p = 0,003), mais le risque de blessures lors des chutes n’était pas différent entre les deux groupes (HR: 1,00, p = 0,97). Parmi les autres effets secondaires qualifiés de sévères par les auteurs, une augmentation des troubles électrolytiques (HR: 1,38, p = 0,006) et de l’insuffisance rénale aiguë (HR: 1,71, p < 0,001) ont été notés parmi les participants du groupe de traitement intensif. Finalement, le tableau IV présente les données sur l’innocuité des traitements assignés.
Tableau IV Données sur l’innocuité des traitements étudiésa
L’étude SPRINT fournit de nouvelles données sur le traitement de l’hypertension et de la cible de pression artérielle à atteindre pour une population non diabétique âgée de 50 ans au minimum. L’approche consistant à viser une pression artérielle systolique de moins de 120 mm Hg a été comparée au traitement standard de la pression artérielle (moins de 140 mmHg).
Les résultats de SPRINT sont certes intéressants, mais leur généralisation à l’ensemble de la population souffrant d’hypertension est limitée. En effet, les critères d’inclusion et d’exclusion de SPRINT étaient stricts. Notamment, les patients ayant un antécédent d’accident vasculaire cérébral, une insuffisance rénale sévère (débit de filtration glomérulaire estimé inférieure à 20 mL/min/1,73 m2) et les diabétiques étaient exclus. Toutefois, SPRINT considérait que le risque d’évènements cardiovasculaires chez leurs patients était élevé. Plus de la moitié des participants inclus étaient des anciens fumeurs ou des fumeurs actifs, souffraient de surpoids ou d’obésité, ou prenaient déjà un antihypertenseur, une statine ou de l’acide acétylsalicylique. Cela dit, dans une étude évaluant la généralisation des résultats de SPRINT à la population américaine, seulement 16,7 % de tous les patients hypertendus recensés répondaient à ces critères22. Les effets d’un contrôle intensif de la pression artérielle démontrés par SPRINT sont donc inconnus pour une population plus jeune et ne s’appliquent pas aux patients ayant une hypertension réfractaire, une pression artérielle difficilement contrôlable, à ceux nécessitant plus de trois médicaments antihypertenseurs ainsi qu’aux patients exclus décrits précédemment.
Malgré toutes ces nuances, les lignes directrices canadiennes, récemment mises à jour, recommandent le traitement intensif pour une population semblable à celle de SPRINT. Elles préconisent toutefois qu’une stratification exhaustive du risque soit effectuée et que tant le patient que son médecin doivent être prêts à se conformer à des suivis plus étroits8. L’applicabilité des résultats de cette étude à une population âgée de plus de 75 ans, fragile ou vulnérable, polymédicamentée, souffrant de multiples comorbidités et syndromes gériatriques, est également limitée, malgré le fait qu’approximativement 35 % de la population étudiée dans les deux groupes était âgée de plus de 75 ans. Les patients demeurant en centre de soins de longue durée ou en résidence ont notamment été exclus de l’étude, et aucune des caractéristiques relevées parmi les participants à l’étude ne nous permet d’évaluer leur état fonctionnel et cognitif, la présence de syndromes gériatriques, tels que des antécédents de chutes, d’étourdissements, de délirium, d’autres comorbidités et la présence de polypharmacie. En effet, les bénéfices d’un traitement antihypertenseur pour la population gériatrique fragile et polymédicamentée sont inconnus23. Des études rapportent qu’une thérapie nécessitant la prise de plusieurs antihypertenseurs est non seulement associée à un risque accru de chutes, mais aussi de mortalité24,25. Les lignes directrices canadiennes n’ont donc pas modifié leur recommandation concernant la population âgée de plus de 80 ans en raison des preuves limitées8. Les résultats de cette étude ne devraient donc s’appliquer qu’à une population semblable à celle qui a été étudiée.
Par surcroît, l’amplitude des effets mesurés peut être contestée en raison de l’arrêt précoce de l’étude. Ceci aurait pu non seulement introduire plusieurs biais, mais aussi surestimer les effets bénéfiques mesurés26. L’hypertension étant une maladie chronique, il faut donc considérer l’efficacité et surtout l’innocuité d’un traitement intensif sur une plus longue durée de suivi. Avec un suivi médian que de 3,26 années, il est possible qu’un biais ait été introduit et que les effets à long terme d’un tel traitement soient différents des résultats obtenus, puisqu’ils finissent par tendre vers la normale. Par contre, il est compréhensible que l’étude ait été arrêtée prématurément en raison des résultats statistiquement significatifs démontrant des bénéfices sur la mortalité.
Quant à la mesure de la pression artérielle utilisée pour l’ajustement du traitement, elle était prise dans le bureau du clinicien à l’aide d’un appareil automatique sans la présence d’un professionnel de la santé. Cette pratique était non seulement requise afin d’uniformiser la méthode de mesure pendant l’étude, mais elle est actuellement recommandée par les lignes directrices du programme éducatif canadien sur l’hypertension. Elles recommandent également de guider la thérapie en se basant à la fois sur des mesures prises à domicile ainsi qu’au cabinet médical. Cette méthode permet de détecter les patients souffrant du syndrome de la blouse blanche ou de l’hypertension masquée8,27. Selon ces nouvelles recommandations et celles de l’étude SPRINT, l’ajustement du traitement antihypertenseur devra donc s’effectuer à partir de mesures de pression artérielle systoliques automatisées, prises par le patient seul, en l’absence d’un professionnel de la santé.
Pour assurer un bon contrôle de la pression artérielle, les participants de l’étude SPRINT ont aussi été encouragés à adopter de meilleures habitudes de vie, telles que l’exercice physique pour favoriser la perte de poids. En effet, l’indice de masse corporelle moyen des participants en début d’étude était de 30 kg/m2. Cependant, les données relatives au suivi de ce paramètre ainsi qu’au changement des habitudes de vie des participants n’ont pas été présentées. Il est possible que les participants du groupe de traitement intensif aient été plus enclins à adopter des habitudes de vie plus saines afin d’optimiser leur traitement comparativement aux participants du groupe de traitement standard.
Quant aux médicaments reçus, les résultats démontrent que les participants assignés au traitement intensif recevaient une plus grande proportion de médicaments ciblant le système rénine-angiotensine (77 % comparativement à 55 %) ainsi que des diurétiques thiazidiques (55 % comparativement à 33 %). Ces différences pourraient influencer les objectifs cardiovasculaires et rénaux. Une analyse de sensibilité complémentaire séparant les participants par classe thérapeutique employée aurait été bénéfique pour évaluer une telle possibilité.
En ce qui a trait à l’innocuité de la thérapie étudiée, il y avait plus d’évènements rapportés d’hypotension, de syncope, de désordre électrolytique et d’atteinte rénale dans le groupe à traitement intensif. Ces résultats renforcent l’importance de bien déterminer la population cible qui pourrait bénéficier en toute sécurité d’un tel traitement. Pour ce qui est spécifiquement des chutes pouvant causer des blessures, SPRINT n’a pas été en mesure de trouver de différence statistiquement significative entre les deux groupes. Toutefois, le fait que cette valeur ait été rapportée pour la durée réelle de l’étude, soit 3,2 années, pourrait avoir engendré une sous-estimation du résultat. En effet, le risque de chutes pouvant causer des blessures est plus important dans les 15 premiers jours qui suivent la mise en place d’un changement de la thérapie antihypertensive28. Il est donc important d’effectuer un suivi étroit, surtout après un ajustement de la thérapie. Quant à l’atteinte rénale, elle est préoccupante et pourrait être causée par la proportion plus importante de participants recevant des médicaments diurétiques et ciblant le système rénine-angiotensine dans le groupe de traitement intensif. Cet effet d’hypoperfusion rénale est potentiellement réversible, mais une plus longue période de suivi est nécessaire afin d’en évaluer les conséquences à long terme. Cet effet a été observé seulement parmi les participants qui n’avaient pas d’atteinte rénale initialement. Il faut noter que la collecte de données pour ce dernier objectif se poursuit actuellement, et les résultats concernant les effets à long terme sur le rein seront présentés ultérieurement.
À la lumière de ces résultats, nous pensons qu’il est pertinent, voire indispensable, d’effectuer une comparaison avec l’étude ACCORD-BP lors de l’évaluation de SPRINT17. L’étude ACCORD-BP, représentant une branche de l’étude principale ACCORD, évaluait les effets d’un traitement intensif pour l’obtention d’une pression artérielle systolique inférieure à 120 mmHg comparativement à un contrôle standard de la pression artérielle systolique à 140 mmHg uniquement parmi des patients diabétiques de type 2. Il s’agissait d’une étude à répartition aléatoire, contrôlée et multicentrique, menée à travers 77 centres au Canada et aux États-Unis. Des 10 251 participants initialement inclus dans ACCORD, 4733 ont été répartis aléatoirement selon un protocole factoriel deux par deux à l’étude ACCORD-BP.
Par contre, bien que les interventions aient été similaires entre SPRINT et ACCORD-BP, la population étudiée était sensiblement différente. L’étude SPRINT avait une population plus âgée (âge moyen de 68 ans comparativement à 62 ans pour ACCORD-BP), elle excluait les patients diabétiques et ceux ayant des antécédents d’accidents vasculaires cérébraux, et elle incluait des patients souffrant d’insuffisance rénale chronique et avec un risque cardiovasculaire de base plus faible (16,7 % de maladies cardiovasculaires cliniques comparativement à 34 % d’antécédents cardiovasculaires pour ACCORD-BP).
Les différences sont nombreuses entre les résultats de SPRINT et d’ACCORD-BP. Tout d’abord, ACCORD-BP n’a pas démontré de bénéfices significatifs du traitement intensif relativement à la mortalité (HR: 1,06, intervalle de confiance à 95 % [IC 95 %]: 0,85–1,35, p = 0,55) et aux objectifs cardiovasculaires (HR: 0,88, IC 95 %: 0,73–1,06, p = 0,20). Ces différences peuvent s’expliquer par le fait que les participants inclus dans ACCORD-BP étaient atteints de diabète de type 2, et une plus grande proportion d’entre eux avaient des antécédents de maladies cardiovasculaires, ce qui pouvait les exposer à un risque plus élevé de décès malgré une cible abaissée de pression artérielle systolique. Cette étude démontre également une diminution statistiquement significative des accidents vasculaires cérébraux dans le groupe de traitement intensif (HR: 0,59, IC 95 %: 0,39–0,89, p = 0,01), une mesure qui n’a pu être répliquée dans SPRINT (HR: 0,89, p = 0,50). En effet, il est possible que la réduction de la pression artérielle systolique n’ait pas eu de bénéfices significatifs pour diminuer l’incidence d’accidents vasculaires cérébraux parmi les participants de SPRINT, compte tenu de leur plus faible risque de base. À l’opposé, il est probable que les participants d’ACCORD-BP aient été plus à risque d’être victimes d’un accident vasculaire cérébral en raison de leur diabète de longue date. Quand le risque de base est plus élevé, l’action d’un traitement antihypertenseur intensif peut démontrer plus facilement une différence significative quant à la réduction d’événements liés à ce risque.
L’étude SPRINT démontre qu’un traitement intensif de la pression artérielle systolique pour l’obtention d’une valeur inférieure à 120 mmHg, comparativement à un traitement standard, diminue de manière statistiquement significative les événements associés à l’objectif composite primaire, mais qu’il augmente aussi l’incidence d’hypotension, entres autres, chez les patients non diabétiques, sans antécédents d’accidents vasculaires cérébraux. L’engouement autour de cette étude générera certainement d’autres hypothèses servant à déterminer la cible idéale de la pression artérielle à viser pour différentes populations. En général, les résultats de SPRINT accentuent l’importance de contrôler la pression artérielle dans le but de réduire les complications cardiovasculaires. En raison des spécificités de la population cible de cette étude, il faut donc s’assurer de bien identifier les patients pouvant bénéficier de ce traitement intensif. Ainsi, il sera important de discuter avec le patient des risques et bénéfices potentiels mis en évidence dans SPRINT et d’individualiser le traitement.
Aucun financement en relation avec le présent article n’a été déclaré par les auteurs.
Tous les auteurs ont rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts en relation avec le présent article.
Cet article a été réalisé dans le cadre du cours Communication scientifique de la Faculté de pharmacie de l’Université de Montréal. Les auteurs sont reconnaissants de la contribution des responsables et des collaborateurs. Une autorisation écrite a été obtenue des personnes à qui s’adressent ces remerciements.
1. Wright JT, Jr., Williamson JD, Whelton PK, Snyder JK, Sink KM, Rocco MV et coll. A randomized trial of intensive versus standard blood-pressure control. N Engl J Med 2015;373:2103–16.

2. Agence de la santé publique du Canada. Rapport du système national de surveillance des maladies chroniques : L’hypertension au Canada, 2010.[en ligne] http://publications.gc.ca/site/fra/9.502461/publication.html (site consulté le 9 avril 2016).
3. Lewington S, Clarke R, Qizilbash N, Peto R, Collins R. Age-specific relevance of usual blood pressure to vascular mortality: A meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002;360:1903–13.
4. Vishram JK, Borglykke A, Andreasen AH, Jeppesen J, Ibsen H, Jorgensen T et coll. Impact of age on the importance of systolic and diastolic blood pressures for stroke risk: The monica, risk, genetics, archiving, and monograph (morgam) project. Hypertension 2012;60:1117–23.
5. Chobanian AV, Bakris GL, Black HR, Cushman WC, Green LA, Izzo JL Jr et coll. The seventh report of the joint national committee on prevention, detection, evaluation, and treatment of high blood pressure: the JNC 7 report. JAMA 2003;289:2560–72.
6. Neal B, MacMahon S, Chapman N. Effects of ace inhibitors, calcium antagonists, and other blood-pressure-lowering drugs: Results of prospectively designed overviews of randomised trials. Blood pressure lowering treatment trialists’ collaboration. Lancet 2000;356:1955–64.
7. Psaty BM, Smith NL, Siscovick DS, Koepsell TD, Weiss NS, Heckbert SR et coll. Health outcomes associated with antihypertensive therapies used as first-line agents. A systematic review and meta-analysis. JAMA 1997;277:739–45.
8. Leung AA, Nerenberg K, Daskalopoulou SS, Mc-Brien K, Zarnke KB, Dasgupta K et coll. Hypertension Canada’s 2016 canadian hypertension education program guidelines for blood pressure measurement, diagnosis, assessment of risk, prevention, and treatment of hypertension. Can J Cardiol 2016;32:569–88.
9. Beckett NS, Peters R, Fletcher AE, Staessen JA, Liu L, Dumitrascu D et coll. Treatment of hypertension in patients 80 years of age or older. N Engl J Med 2008;358:1887–98.
10. Staessen JA, Fagard R, Thijs L, Celis H, Arabidze GG, Birkenhager WH et coll. Randomised double-blind comparison of placebo and active treatment for older patients with isolated systolic hypertension. Lancet 1997;350:757–64.
11. Arguedas JA, Perez MI, Wright JM. Treatment blood pressure targets for hypertension. Cochrane Database Syst Rev 2009;CD004349.
12. SHEP cooperative research group. Prevention of stroke by antihypertensive drug treatment in older persons with isolated systolic hypertension. Final results of the systolic hypertension in the elderly program (SHEP). JAMA 1991;265:3255–64.
13. JATOS study group. Principal results of the japanese trial to assess optimal systolic blood pressure in elderly hypertensive patients (JATOS). Hypertens Res 2008;31:2115–27.
14. Ogihara T, Saruta T, Rakugi H, Matsuoka H, Shimamoto K, Shimada K et coll. Target blood pressure for treatment of isolated systolic hypertension in the elderly: Valsartan in elderly isolated systolic hypertension study. Hypertension 2010;56:196–202.
15. Verdecchia P, Staessen JA, Angeli F, de Simone G, Achilli A, Ganau A et coll. Usual versus tight control of systolic blood pressure in non-diabetic patients with hypertension (cardio-sis): An open-label randomised trial. Lancet 2009;374:525–33.
16. National Heart, Lung, and Blood Institute. U.S. Department of Health & Human Services. Working group report: expert panel on a hypertension treatment trial initiative meeting summary. [en ligne] http://www.nhlbi.nih.gov/sites/www.nhlbi.nih.gov/files/hypertsnsion-full.pdf (site consulté le 9 avril 2016).
17. Cushman WC, Evans GW, Byington RP, Goff DC Jr, Grimm RH, Jr., Cutler JA et coll. Effects of intensive blood-pressure control in type 2 diabetes mellitus. N Engl J Med 2010;362:1575–85.

18. James PA, Oparil S, Carter BL, Cushman WC, Dennison-Himmelfarb C, Handler J et coll. 2014 evidence-based guideline for the management of high blood pressure in adults: Report from the panel members appointed to the eighth joint national committee (JNC 8). JAMA 2014;311:507–20.
19. Mancia G, Fagard R, Narkiewicz K, Redon J, Zanchetti A, Bohm M et coll. 2013 ESH/ESC guidelines for the management of arterial hypertension: The task force for the management of arterial hypertension of the european society of hypertension (ESH) and of the european society of cardiology (ESC). J Hypertens 2013;31:1281–357.
20. National institute of health and clinical excellence. Hypertension in adults: Diagnosis and management. NICE clinical guideline 127. [en ligne] http://guidance.nice.org.uk/CG127 (site consulté le 9 avril 2016).
21. Xie X, Atkins E, Lv J, Bennett A, Neal B, Ninomiya T et coll. Effects of intensive blood pressure lowering on cardiovascular and renal outcomes: Updated systematic review and meta-analysis. Lancet 2016;387:435–43.
22. Bress AP, Tanner RM, Hess R, Colantonio LD, Shimbo D, Muntner P. Generalizability of sprint results to the U.S. Adult population. J Am Coll Cardiol 2016;67:463–72.
23. Benetos A, Labat C, Rossignol P, Fay R, Rolland Y, Valbusa F et coll. Treatment with multiple blood pressure medications, achieved blood pressure, and mortality in older nursing home residents. The PARTAGE study. JAMA 2015;175:989–95.
24. Tinetti ME, Han L, Lee DSH, McAvay GJ, Peduzzi P, Gross CP et coll. Antihypertensive medications and serious fall injuries in a nationally representative sample of older adults. JAMA 2014;174:588–985.
25. Benetos A, Rossignol P, Cherubini A, Joly L, Grodzicki T, Rajkumar C et coll. Polypharmacy in the aging patient: Management of hypertension in octogenarians. JAMA 2015;314:170–80.
26. Bassler D, Briel M, Montori VM, Lane M, Glasziou P, Zhou Q et coll. Stopping randomized trials early for benefit and estimation of treatment effects: Systematic review and meta-regression analysis. JAMA 2010;303:1180–7.
27. Pierdomenico SD, Cuccurullo F. Prognostic value of white-coat and masked hypertension diagnosed by ambulatory monitoring in initially untreated subjects: An updated meta analysis. Am J Hypertens 2011;24:52–8.
28. Shimbo D, Barrett Bowling C, Levitan EB, Deng L, Sim JJ, Huang L et coll. Short-term risk of serious fall injuries in older adults initiating and intensifying treatment with antihypertensive medication. Circ Cardiovasc Qual Outcomes 2016;9:222–9.

PHARMACTUEL, Vol. 50, No. 1, 2017