Christine Hamel1,2,3,4, B.Pharm., M.Sc.
Reçu le 2 février 2018: Accepté après révision le 4 mai 2018
Résumé
Objectif : Décrire l’évolution des mesures de protection des pharmaciens et assistants techniques en pharmacie contre l’exposition aux médicaments dangereux au cours des 50 dernières années.
Description de la problématique : La rédaction de cet article thématique vise à souligner les 50 ans d’existence du Pharmactuel. Une revue de la littérature scientifique et un sondage ont permis de décrire l’évolution des connaissances, des lignes directrices et des méthodes de travail portant sur la manipulation des médicaments dangereux.
Résolution de la problématique : Les premières publications portant sur les risques potentiels d’exposition professionnelle aux antinéoplasiques ont eu lieu dans les années 1970. Les années 1980 ont quant à elles marqué l’apparition des premières lignes directrices et recommandations sur les méthodes de travail. Les connaissances dans le domaine des risques à plus long terme et de la reproduction posés par les médicaments dangereux se sont étoffées au cours des années 1990. L’alerte NIOSH, dans les années 2000, a entraîné un profond changement des pratiques, tandis que le raffinement des méthodes de détection des antinéoplasiques ont permis de perfectionner les moyens de surveillance environnementale dans les années 2010.
Conclusion : De 1967 à 2017, le pharmacien s’est investi pour améliorer la protection des travailleurs qui manipulent les médicaments dangereux. Les principaux défis à relever dans les 50 prochaines années résident dans l’amélioration de la connaissance des risques à long terme de l’exposition professionnelle aux cytotoxiques et de la conformité de la pratique aux lignes directrices.
Mots clés : Antinéoplasiques, cytotoxiques, évolution, exposition professionnelle, médicaments dangereux, protection, travailleur
Abstract
Objective : To describe the evolution, in the past 50 years, of methods for protecting pharmacists and pharmacy technical assistants from exposure to hazardous drugs.
Problem description : This article was written to highlight Pharmactuel’s 50 years of existence. A literature review and a survey were conducted to describe the changes in the knowledge, guidelines and work methods relating to the handling of hazardous drugs over the years.
Problem resolution : The first publications on the potential risks associated with occupational exposure to antineoplastics appeared in the 1970s, and the first guidelines and recommendations concerning work methods in the 1980s. Knowledge regarding the longer-term and reproductive risks posed by hazardous drugs increased in the 1990s. In the 2000s, the NIOSH Alert led to a profound change in practices, and the refinement of methods for detecting antineoplastics helped perfect environmental monitoring methods in the 2010s.
Conclusion : From 1967 to 2017, pharmacists were involved in protecting their employees as best possible during the handling of hazardous drugs. The main challenges for the next 50 years are to improve our knowledge of the long-term risks associated with occupational exposure to cytotoxic drugs and to enhance practice compliance with the guidelines.
Keywords : Antineoplastics, cytotoxic drugs, employee, evolution, hazardous drugs, occupational exposure, protection
Les effets indésirables et la toxicité de certains médicaments dangereux, dont les antinéoplasiques, étaient connus dès les premières administrations de ces agents aux patients1. Puisque ces médicaments servent à traiter des cancers qui ne seraient pas curables autrement, la balance entre les risques et les avantages est largement favorable aux patients. La situation des travailleurs de la santé est différente, car ils sont exposés de façon prolongée aux risques inhérents à cette classe de médicaments, sans en retirer d’avantages directs. Cependant, les risques exacts encourus sont encore sujets à controverse.
Falck et coll. ont été les premiers, en 1979, à détecter de la mutagénicité dans les urines de travailleurs manipulant des antinéoplasiques2. La mesure de la mutagénicité consiste à déterminer la présence de substances qui risquent d’induire des mutations. Elle s’effectue par l’exposition de l’urine à différentes souches bactériennes prédéterminées, ce qui permet de déterminer le pouvoir mutagène de l’urine3. Cette découverte a poussé plusieurs organisations et associations à recommander la rédaction de lignes directrices sur la manipulation des médicaments dangereux dans les années 1980 et 19904–8. La publication de lignes directrices a quant à elle entraîné de multiples changements de méthodes de travail et de moyens de protection des travailleurs9.
L’objectif de cet article consiste à décrire l’évolution de la littérature scientifique et des pratiques portant sur l’exposition des travailleurs aux médicaments dangereux au cours des 50 dernières années.
L’année 2017 marquait le 50e anniversaire de l’existence de la revue Pharmactuel. À cette occasion, le comité de rédaction a décidé de publier des articles thématiques.
La préparation des médicaments dangereux est l’un des domaines où la pratique des pharmaciens et assistants techniques a le plus évolué au cours du dernier demi-siècle. Afin de décrire l’évolution des connaissances et des pratiques à ce sujet, l’auteure a procédé à une revue de littérature à l’aide du moteur de recherche Pubmed, portant sur les années 1935 à 2018. Elle a en outre lancé aux membres actifs et retraités de l’Association des pharmaciens des établissements de santé du Québec (A.P.E.S.) ainsi qu’aux membres abonnés aux pages Facebook et Twitter du Pharmactuel une invitation à participer à un sondage. Le consentement implicite des participants à la publication des résultats a été soumis lors de l’invitation à remplir ce sondage.
Étant donné l’ampleur du sujet et l’espace restreint alloué à cette chronique, la littérature ainsi que le contenu des lignes directrices concernant l’exposition des travailleurs aux médicaments dangereux ne peuvent être traités de manière exhaustive. Certains aspects plus particuliers ont été choisis pour les besoins du manuscrit, soit l’historique de l’évolution de l’exposition des travailleurs qui manipulent les médicaments dangereux et celui des mesures de prévention instaurées au cours des 50 dernières années. Pour obtenir des données plus complètes, les lecteurs sont priés de se référer aux lignes directrices mentionnées ultérieurement dans le texte.
En 1970, Ng et coll. ont publié l’un des premiers articles répertoriés portant sur les risques possibles encourus par le travailleur manipulant des antinéoplasiques10. Ces auteurs faisaient état d’une décoloration intense brun foncé de la peau en présence du 1,3-bis (2-chloroéthyl)-1-nitrosuée (carmustine, BCNU)10. Par la suite, en 1975, Thomsen et coll. ont démontré que seuls les gants en polyvinylchloride (PVC) empêchaient la pénétration de la moutarde azotée à travers la peau11. Les gants en caoutchouc et en polyéthylène laissaient quant à eux passer cette molécule11.
Malgré ces publications préliminaires, le premier signal d’alarme important face au risque possible d’exposition professionnelle aux antinéoplasiques n’a été publié qu’en 19792. Falck et coll. ont comparé la mutagénicité d’échantillons d’urine de patients, d’infirmières pratiquant en oncologie et de travailleurs non exposés à des antinéoplasiques (psychologues, groupe témoin)2. Les mutations étaient inférieures chez les infirmières comparativement à celle des patients2. Cependant, il y avait une augmentation statistiquement significative de la mutagénicité chez les infirmières par rapport au groupe témoin1. Fait intéressant, la mutagénicité était supérieure en milieu de semaine comparativement au lundi matin2.
L’étude de Falck et coll. a conduit des organismes comme l’American Society of Hospital Pharmacists et l’Occupational Safety and Health administration (OSHA) à publier des lignes directrices sur la manipulation des médicaments dangereux2. En 1980, le Memorial Sloan Kettering Cancer Center ajoutait à ses politiques et procédures l’obligation d’utiliser une hotte à flux vertical laminaire et de porter des gants pour préparer de la chimiothérapie12. Ces politiques et procédures mentionnaient également l’utilisation de contenants spécifiques pour entreposer les déchets de produits cytotoxiques12. En 1980, Knowles et coll. ont publié une revue de la littérature médicale sur les risques connus associés à chaque antinéoplasique ainsi que des recommandations relatives à la manipulation spécifique de chacun d’entre eux émises par les manufacturiers13. À l’époque, les manufacturiers recommandaient le port de gants pour la préparation de la majorité des antinéoplasiques13. Cependant, il est intéressant de noter qu’ils ne recommandaient aucune précaution particulière pour la préparation du cyclophosphamide, de la cytarabine, du fluorouracile et de l’ifosfamide2.
Les lignes directrices d’Hoffman et coll. étaient avant-gardistes, étant donné qu’une étude comparant l’utilisation de hottes à flux laminaire horizontal et vertical pour la préparation d’agents cytotoxiques n’a été publiée qu’en 198214. Anderson et coll. ont démontré qu’il était possible de détecter de la mutagénicité dans les urines des travailleurs utilisant des hottes à flux laminaire horizontal, contrairement à ceux travaillant dans des hottes à flux laminaire vertical biologique de classe II14. Les résultats étaient similaires avec ou sans le port de gants et de masque, ce qui indique l’importance du type de hotte pour limiter l’exposition aux médicaments dangereux14.
Avant les années 1980, la voie principale présumée d’exposition aux antinéoplasiques, plus particulièrement au cyclophosphamide, était par pénétration percutanée2. En 1984, Hirsh et coll. ont publié une étude mentionnant que le cyclophosphamide était également absorbé par inhalation15. Cette publication renforçait davantage la nécessité d’utiliser une hotte biologique de classe II, mais concluait également à la nécessité de préparer la chimiothérapie dans une salle séparée15.
L’American Society of Hospital Pharmacists et l’Occupational Safety and Health administration (OSHA) ont émis respectivement en 1985 et 1986 des lignes directrices portant sur la préparation des antinéoplasiques4,5. Elles recommandaient le port de jaquettes destinées exclusivement à la préparation de la chimiothérapie4,5. OSHA recommandait le port de gants de latex, qui étaient moins perméables que les gants en PVC4. Il était même recommandé d’utiliser une double paire de gants si cela n’interférait pas avec la technique et de changer de gants toutes les heures4. Dans certains établissements qui ne possédaient pas de hotte biologique à cette époque, on recommandait de porter un écran facial et des lunettes en plastique et d’avoir une fontaine oculaire à portée de main4. À cette époque, on demandait déjà d’installer les hottes biologiques dans des pièces séparées, munies d’un système de ventilation permettant d’expulser l’air directement à l’extérieur4. On recommandait en outre le port de jaquettes à longues manches, jetables, hydrofuges et fermées dans le dos4. OSHA recommandait également le nettoyage quotidien et la décontamination hebdomadaire de la hotte biologique4. Finalement, selon ces lignes directrices, il fallait récupérer les fioles, les seringues et l’amorce de la tubulure sous la hotte pour les placer dans un contenant rigide4. Il est étonnant de constater que les lignes directrices des années 1980 contenaient déjà la majorité des recommandations toujours pertinentes en 2010. Par contre, il est à noter que seuls 27 produits étaient présents sur la liste des médicaments dangereux dans les lignes directrices d’OSHA, car plusieurs médicaments considérés comme dangereux actuellement étaient exclus de cette catégorie en 19804.
Les connaissances sur les conséquences de l’exposition des travailleurs aux antinéoplasiques se sont davantage développées dans les années 1990. En 1993, Valanis et coll. ont été les premiers à décrire les effets indésirables aigus pouvant survenir lors de ces manipulations16. Ils ont nommé les nausées, les céphalées, l’irritation des yeux et de la peau ainsi que des réactions allergiques16. Skov et coll. ont quant à eux souligné le fait que les antinéoplasiques puissent être à l’origine de dommages causés à l’acide désoxyribonucléique (ADN), de l’infertilité, d’avortements spontanés, de prématurité et de problèmes congénitaux17. Ces auteurs mentionnaient également une augmentation possible du risque de leucémies et d’autres cancers dans un groupe de 275 infirmières administrant les antinéoplasiques17. Par contre, cette étude a été effectuée en l’absence de groupe témoin. Il est donc difficile d’interpréter les résultats obtenus par ces auteurs, qui n’ont par ailleurs jamais été confirmés par des études de plus grande envergure jusqu’à maintenant.
En 1992, Valanis et coll. ont publié une étude évaluant la conformité des pratiques des travailleurs aux lignes directrices de l’OSHA18. Bien que les pratiques se soient améliorées significativement depuis la parution de ces directives, il existait un pourcentage important de non-conformité18. Par exemple, seuls 65 à 69 % des travailleurs du département de pharmacie préparaient les antinéoplasiques dans une hotte à flux vertical et 60 à 76 % d’entre eux portaient des jaquettes (type non précisé)18. En 1997, la Société canadienne des pharmaciens d’hôpitaux a émis à son tour des lignes directrices reprenant la majorité des thèmes abordés par OSHA6.
Les années 2000 ont marqué un tournant significatif en matière de manipulation des médicaments dangereux avec la publication en 2004 de l’alerte du National Institute for Occupational Safety and Health (NIOSH)7. Cette organisation a tout d’abord proposé une nouvelle définition de l’expression « médicament dangereux », qui inclut dorénavant les produits tératogènes, cancérogènes, génotoxiques, ceux affectant les fonctions reproductices ainsi que ceux causant à faible dose des dommages aux organes7. Cette nouvelle définition a fait grimper le nombre de médicaments dangereux à plus de 1307. De nouvelles recommandations ont également été émises, par exemple une évaluation complète de toutes les étapes du circuit du médicament : de la réception à l’administration et à la gestion des déchets pouvant être des sources de contamination7. Elles proposaient également de former adéquatement et régulièrement les travailleurs exposés aux cytotoxiques7. Ces recommandations préconisaient aussi de changer de gants aux 30 minutes maximum (ou lorsqu’ils étaient détériorés), d’utiliser des jaquettes hydrofuges, de mettre le produit final dans un sac de plastique et d’envisager l’utilisation de systèmes fermés. NIOSH a également émis des recommandations sur l’hygiène et la salubrité des locaux consacrés à la préparation de médicaments dangereux7. Finalement, NIOSH recommandait d’effectuer une surveillance médicale régulière des travailleurs exposés et de procéder à des échantillonnages afin d’évaluer la présence de contamination7.
En 2005, Dranitsaris et coll. publiaient une revue systématique et une méta-analyse portant sur le risque d’incidents toxiques touchant les travailleurs manipulant les médicaments dangereux19. Malheureusement, peu d’études ont été publiées sur les effets de tels incidents19. Dranitasris et coll. ne pouvaient donc émettre aucune conclusion en ce qui a trait au lien entre la manipulation des médicaments cytotoxiques et les effets indésirables toxiques aigus, le risque de développer un cancer à long terme, les malformations congénitales et la mortalité périnatale19. Par contre, le risque d’avortement spontané avait augmenté de 46 % chez les infirmières, pharmaciennes et assistantes techniques en pharmacie enceintes qui étaient en contact avec des produits cytotoxiques (rapport de risques [RR] : 1,46; intervalle de confiance à 95 % [IC 95 %] 1,11–1,92)19.
En 2006, Bédard et coll. ont publié une étude évaluant la conformité d’une pharmacie satellite d’hémato-oncologie9. À l’instar de plusieurs autres départements de pharmacie, le respect des recommandations émises par NIOSH a nécessité, d’une part, un réaménagement important des locaux consacrés à la préparation des médicaments dangereux et, d’autre part, l’ajout de personnel9.
En 2007, Bussières et coll. ont publié leur enquête québécoise sur la préparation et l’administration des médicaments dangereux, qui évaluait la situation prévalant dans les départements de pharmacie au 31 mars 200620. Les auteurs rapportent un taux de conformité inférieur à 50 % au 17 des 40 règles de pratiques qu’ils ont évaluées20. Les règles présentant le plus faible taux de conformité portaient sur la réception et le transport des médicaments dangereux du quai réception à la pharmacie (4 %), la surveillance de la contamination environnementale de la pharmacie (2 %), la surveillance de la contamination environnementale aux unités de soins ou aux cliniques externes (0 %) ainsi que la décontamination des médicaments dangereux avant leur entreposage à la pharmacie (4 %)20.
En 2008, l’Association paritaire pour la santé et la sécurité du travail du secteur des affaires sociales (ASSTSAS) a publié un guide concernant la manipulation des médicaments dangereux8. Ce document visait à décrire l’implantation de mesures préventives pour la manipulation sécuritaire des médicaments recommandés par NIOSH au sein des établissements de santé québécois8. Ce guide énonçait également des recommandations portant sur la gestion sécuritaire des médicaments dangereux lors de soins prodigués au domicile des patients8.
La révision de la liste initiale des médicaments dangereux émise par NIOSH a eu lieu en 2010, 2012, 2014 et 201621–24. Lors de cette dernière mise à jour, la liste comptait plus de 190 médicaments24. Il est à noter qu’une révision de la liste NIOSH est en cours en 2018.
L’évolution des méthodes et des limites de détection des antinéoplasiques dans les échantillons d’urine a permis à Sottani et coll. de publier en 2010 une étude portant sur la contamination environnementale par les antinéoplasiques dans des centres hospitaliers italiens, entre les années 1990 et les années 200025. Ces auteurs ont détecté la présence de cyclophosphamide, d’ifosfamide, de doxorubicine ou d’épirubicine dans les urines de 30 % des travailleurs évalués dans les années 199025. À la suite de ces résultats, les auteurs ont développé un programme de protection des travailleurs contre les antinéoplasiques25. Ce programme portait entre autres sur l’analyse complète de l’environnement de travail, la surveillance de la contamination environnementale à l’aide d’échantillons des surfaces intérieures et extérieures des hottes biologiques destinées à la préparation d’antinéoplasiques et des sondages biannuels25. À partir de 2003, année où les travailleurs de la santé oeuvrant à la préparation d’agents cytotoxiques ont commencé à respecter les recommandations (selon les résultats du sondage biannuel), la proportion d’échantillons d’urine contaminés par des antinéoplasiques a chuté à 2 %25. Aucun échantillon positif n’a été obtenu pour les années 2006 et 200725.
Il semble que les incitatifs au changement soient toujours pertinents dans les années 2010. De fait, Boinao et coll. ont effectué en 2015 une étude portant sur l’adhésion aux lignes directrices relatives à la manipulation d’antinéoplasiques par des assistants techniques en pharmacie, des pharmaciens et des infirmières américains26. Les résultats qu’ils ont obtenus étaient décevants : 47 % des travailleurs ne portaient pas toujours une double paire de gants, 10 % n’en portaient pas du tout, 20 % ne portaient pas toujours la jaquette recommandée, 15 % n’utilisaient pas toujours une hotte biologique, 13 % n’avaient suivi aucune formation particulière et 45 % des établissements n’avaient mis en place aucun programme de surveillance26.
L’investigatrice a reçu 63 réponses anonymes au sondage. Il n’est cependant pas possible de déterminer le taux exact de participation au sondage, puisque 1800 membres actifs de l’Association des pharmaciens des établissements de santé du Québec ainsi qu’un nombre indéterminé de membres retraités de cette même association et de personnes inscrites sur les pages Facebook et Twitter de Pharmactuel l’ont reçu. Un très faible nombre de répondants avaient fait l’expérience personnelle de la situation qui prévalait avant les années 1980. Par ailleurs, treize répondants ont mentionné spontanément que le début de leur pratique datait des années 2000, alors que cette question n’était pas spécifiquement posée dans le sondage.
Selon les résultats de ce sondage descriptif, il semble que les pratiques en oncologie au Québec ont évolué parallèlement à la découverte des nouvelles connaissances et à l’implantation des lignes directrices et recommandations des différents organismes.
Ainsi, un répondant mentionne que, dans les années 1960, il a été témoin de la préparation de médicaments dangereux sans aucune hotte biologique. Jusqu’à 10 % des participants indiquaient que, dans les années 1980, la hotte d’oncologie utilisée n’était pas située dans une salle de préparation stérile séparée. Les pratiques ont évolué quant à cet aspect de la préparation des médicaments dangereux, puisque 80,11 % des répondants ont mentionné que, dans les années 2010, ce type de préparation avait lieu dans une salle de préparation stérile (dont 68,25 % respectaient les normes de salubrité et de ventilation et 11,86 % ne les respectaient pas), séparée physiquement des locaux adjacents.
Les pratiques ont également évolué en ce qui a trait aux équipements de protection individuels. Jusqu’à 8,33 % des répondants ont mentionné avoir été témoins que, dans les années 1980, les gants utilisés pour la préparation des médicaments dangereux n’étaient pas exclusivement destinés à la chimiothérapie. La majorité des répondants ont indiqué que, durant la décennie 2010, le changement de gants de chimiothérapie avait lieu toutes les 30 minutes au maximum (70,97 %) ou à une ou deux reprises au cours d’une journée de travail (19,67 %). Une proportion de 20 % des répondants ont affirmé avoir été témoins de l’utilisation de jaquettes non hydrofuges pour la préparation de médicaments dangereux dans les années 1990 et celles antérieures à cette décennie. Un taux de 58,73 % des répondants ont mentionné l’utilisation, au cours des années 2000 à 2010, de jaquettes à manches longues fermant dans le dos et hydrofuges.
Finalement, les procédures d’entreposage des antinéoplasiques et d’entretien des hottes d’oncologie se sont également améliorées à travers le temps. Dans les années 1960 et 1970, le seul répondant ayant pratiqué à cette époque affirme avoir été témoin de l’entreposage des antinéoplasiques avec les autres produits de la pharmacie, alors que 61,02 % des sondés avaient toujours vu les antinéoplasiques entreposés séparément des autres médicaments. Le respect des recommandations portant sur le nettoyage et la désinfection quotidiens, la décontamination hebdomadaire et la décontamination des hottes d’oncologie lors d’un déversement est plus fréquent dans les années 2010 (respectivement 57,14 %, 66,13 % et 59,68 %) que dans les années 1980 (respectivement 3,17 %, 0 % et 3,23 %). Les résultats complets du sondage sont présentés aux tableaux I et II.
Tableau I Résultats du sondage soumis aux membres de l’A.P.E.S. en décembre 2017, portant sur l’évolution de la protection des travailleurs oeuvrant à la préparation des antinéoplasiques - Partie I : Salle stérile, hotte, technique utilisée et gants
Tableau II Résultats du sondage soumis aux membres de l’A.P.E.S. en décembre 2017, portant sur l’évolution de la protection des travailleurs oeuvrant à la préparation des antinéoplasiques - Partie II : Jaquette, entreposage, déchets, nettoyage et décontamination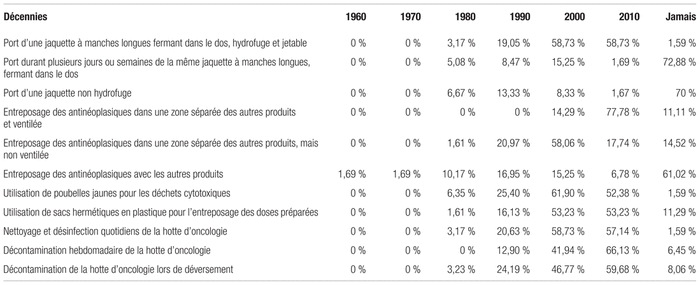
En 2017, Hall et coll. ont mené une étude visant à déterminer la proportion de travailleurs canadiens exposés professionnellement aux antinéoplasiques, tous secteurs d’activités confondus27. Ces auteurs estiment que 75 000 Canadiens, soit 0,42 % de la population active sont exposés aux antinéoplasiques27. Les femmes sont davantage exposées que les hommes, car elles représentent 75 % de ces travailleurs27. Une proportion importante de l’exposition aux antinéoplasiques survient en pharmacie communautaire (52 %) ou au sein du département de pharmacie d’établissements (17 %)27. Ce nombre important de travailleurs soumis à une telle exposition favorise la participation assidue des pharmaciens, des départements de pharmacie ainsi que de l’A.P.E.S. à l’élaboration et à la mise en place de recommandations visant à assurer la sécurité des travailleurs qui manipulent des médicaments dangereux.
Bien que certains aspects de ces risques soient toujours controversés en 2018, les connaissances sur les dangers de l’exposition des travailleurs aux antinéoplasiques se sont considérablement accrues au cours des 50 dernières années et ont entraîné, depuis 1967, une évolution importante des normes et lignes directrices entourant la manipulation des produits dangereux. Ces lignes directrices ont à leur tour permis de développer des méthodes de travail de plus en plus rigoureuses. L’importante difficulté qui demeure à l’heure actuelle consiste à combler l’écart qui existe toujours entre les recommandations émises par les organisations expertes, telles que NIOSH, et l’implantation de ces mêmes recommandations dans les départements de pharmacie. Le respect de normes aussi rigoureuses demande souvent une contribution financière non négligeable ainsi que l’ajout de personnel compétent. Étant donné les dépenses importantes nécessaires au bon fonctionnement des autres sphères des départements de pharmacie et la période d’austérité actuelle, il arrive que les actions à entreprendre pour se conformer aux normes soient reportées.
Il est important de rappeler que le respect des lignes directrices permet l’obtention de résultats concrets relatifs à la protection contre la contamination par les produits cytotoxiques. De plus, la surveillance environnementale de la contamination par les antinéoplasiques est un levier important pour encourager le changement de pratiques. L’étude de Sottani et coll. a révélé que les travailleurs qui constataient la présence d’antinéoplasiques dans leurs urines s’intéressaient davantage à modifier leur méthode de travail et manifestaient une plus grande ouverture à le faire25. Les auteurs ont par ailleurs mentionné que, pour que le programme de prévention fonctionne, il fallait rappeler périodiquement les procédures aux personnes concernées et procéder à des mesures annuelles d’antinéoplasiques dans leurs urines, afin de déterminer rapidement l’origine des problèmes et de les corriger immédiatement25.
Depuis 1967, les connaissances sur les risques de l’exposition professionnelle aux antinéoplasiques se sont considérablement accrues. Le pharmacien a été très proactif dans l’élaboration et l’application de lignes directrices. Cette importante contribution du pharmacien a permis de faire évoluer les pratiques et a contribué à la protection des travailleurs en pharmacie, mais aussi des autres professionnels de la santé manipulant des médicaments dangereux. Les difficultés qui attendent les acteurs du milieu durant les 50 prochaines années portent surtout sur la mise en oeuvre de moyens convaincants pour démontrer les risques de l’exposition professionnelle à long terme aux médicaments dangereux ainsi que l’amélioration de la conformité de la pratique aux lignes directrices.
Aucun financement en relation avec le présent article n’a été déclaré par l’auteure.
L’auteure a rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. L’auteure n’a déclaré aucun conflit d’intérêts en relation avec le présent article.
L’auteure remercie Jocelyne Perron, France St-Pierre et Shirley-Ann Lahue pour leur soutien lors du développement et de la diffusion du sondage utilisé pour cet article. Une autorisation écrite a été obtenue de ces personnes.
1. Cressy NL, Schell HW Jr. Effectiveness and toxicity of prolonged infusions of 5-flurouracil in the treatement of cancer. Am J Med Sci 1965;249:52–5.
2. Falck K, Gröhn P, Sorsa M, Vainio H, Heinonen E, Holsti LR. Mutagenicity in urine of nurses handling cytostatic drugs. Lancet 1979;1(8128):1250–1.
3. Institut National de Santé Publique (INSPQ). Évaluation quantitative des adduits à l’ADN dans des cellules endobuccales par immunofluorescence et de la mutagénécité urinaire par le test d’Ames. [en ligne] https://www.inspq.qc.ca/es/node/1041 (site visité le 3 mai 2018).
4. OSHA, 1986. Guidelines for cytotoxic (Antineoplastic) drugs. [en ligne] https://www.osha.gov/pls/oshaweb/owadisp.show_document?p_table=DIRECTIVES&p_id=1702 (site visité le 31 janvier 2018).
5. American Society of Hospital Pharmacists (ASHP). Technical assistance bulletin on handling cytotoxic drugs in hospitals. Am J Hosp Pharm 1985;42:131–7.
6. Société canadienne des pharmaciens d’hôpitaux. Lignes directrices sur la manutention et l’élimination des substances pharmaceutiques dangereuses (médicaments cytotoxiques compris). SCHP Publications officielles 2003/2004. 65–77.
7. Department of Health and Human Services. Centers for Disease Control and Prevention. National Institute for Occupational Safety and Health. Prevention occupational exposures to antineoplastic and other hazardous drugs in health care settings. DHHS (NIOSH) Publication Number 2004–165. 50 p.
8. Association paritaire pour la santé et la sécurité du travail du secteur affaires sociales (ASSTASS), 2008. Guide de prévention. Manipulation sécuritaire des médicaments dangereux. [en ligne] http://asstsas.qc.ca/publication/guide-de-prevention-manipulation-securitaire-desmedicaments-dangereux-gp65 (site visité le 31 janvier 2018).
9. Bédard V, Gagné E, Goulet D, Monfette G. Évaluation de la conformité d’une pharmacie satellite d’hémato-oncologie. Pharmactuel 2006;39:44–7.
10. Ng LM, Jaffe N. Possible hazards of handling antineoplastic drugs. Pediatrics 1970;46:648–9.
11. Thomsen K, Mikkelsen HI. Protective capacity of gloves used for handling of nitrogen mustard. Contact Dermatitis 1974;1:268–9.
12. Hoffman DM. The handling of antineoplastic drugs in a major cancer center. Hosp Pharm 1980;15:302–4.
13. Knowles RS, Virden JE. Handling of injectable antineoplastic agents. Br Med J 1980;281:589–91.

14. Anderson RW, Puckett WH, Dana WJ, Nguyen TV, Theiss JC, Matney TS. Risk of handling injectable antineoplastic agents. Am J Hosp Pharm 1982;39:1881–7.
15. Hirst M, Tse S, Mills DG, Levin L, White DF. Occupational exposure to cyclophosphamide. Lancet 1984;1(8370):186–8.
16. Valanis BG, Vollmer WM, Labuhn KT, Glass AG. Association of antineoplastic drug handling with acute adverse effects in pharmacy personnel. Am J Hosp Pharm 1993;50:455–62.
17. Skov T, Maarup B, Olsen J, Rorth M, Winthereik H, Lynge E. Leukaemia and reproductive outcome among nurses handling antineoplastic drugs. Br J Ind Med 1992;49:855–61.

18. Valanis B, Vollmer WM, Labuhn K, Glass A, Corelle C. Antineoplastic drug handling protection after OSHA guidelines. Comparison by profession, handling activity and work site. J Occup Med 1992;34:149–55.
19. Dranistaris G, Johnston M, Poirier S, Schueller T, Milliken D, Green E et coll. Are health care providers who work with cancer drugs at an increased risk for toxic events? A systematic review and meta-analysis of the literature. J Oncol Pharm Pract 2005;11:69–78.
20. Bussières JF, Gagnon K, Bérard G, Gallant C, Barret P. Enquête québécoise sur la préparation et l’administration de médicaments dangereux incluant les médicaments cytotoxiques. Pharmactuel 2007;40:37–42.
21. National Institute for Ocupational Safety and Health (NIOSH). NIOSH list of antineoplastic and other hazardous drugs in healthcare settings 2010. [en ligne] https://www.cdc.gov/niosh/docs/2010-167/pdfs/2010-167.pdf (site visité le 3 mai 2018).
22. National Institute for Ocupational Safety and Health (NIOSH). NIOSH list of antineoplastic and other hazardous drugs in healthcare settings 2012. [en ligne] https://www.cdc.gov/niosh/docs/2012-150/pdfs/2012-150.pdf (site visité le 3 mai 2018).
23. National Institute for Ocupational Safety and Health (NIOSH). NIOSH list of antineoplastic and other hazardous drugs in healthcare settings 2014. [en ligne] https://www.cdc.gov/niosh/docs/2014-138/pdfs/2014-138.pdf (site visité le 3 mai 2018).
24. National Institute for Ocupational Safety and Health (NIOSH). NIOSH list of antineoplastic and other hazardous drugs in healtcare settings 2016. [en ligne] https://www.cdc.gov/niosh/docket/review/docket233a/pdfs/2016-161final-publication.pdf (site visité le 3 mai 2018).
25. Sottani C, Porro B, Cornelli M, Imbriani M, Minoia C. An analysis to study trends in occupational exposure to antineoplastic drugs among health care workers. J Chromatogr B Analyt Technol Biomed Life Sci 2010;878:2593–60.
26. Boiano JM, Steege AL, Sweeney MH. Adherence to precautionary guidelines for compounding antineoplastic drugs : A survey of nuses and pharmacy practioners. J Occup Environ Hyg 2015;588–602.
27. Hall AL, Demers PA, Astrakianakis G, Ge C, Peters CE. Estimating national-level exposure to antineoplastic agents in the workpace: CAREX Canada findinds and future research needs. Ann Work Expo Health 2017;61:656–8.
PHARMACTUEL, Vol. 51, No. 3, 2018