L’efficacité et la sécurité cardiovasculaire de l’insuline dégludec comparativement à l’insuline glargine pour les patients souffrant de diabète de type 2: Étude DEVOTE
Charlie Li Lamoureux1,2*, Pharm.D., Jean-François Provencher1,3*, Pharm.D., Catherine Robert4, Pharm.D., Lyne Gauthier5, B.Pharm., M.Sc.
1Candidat à la maîtrise en pharmacothérapie avancée au moment de la rédaction, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
2Résidente en pharmacie au moment de la rédaction, Hôpital Maisonneuve-Rosemont, Centre intégré universitaire de santé et de services sociaux de l’Est-de-l’Île-de-Montréal, Montréal (Québec) Canada;
3Résident en pharmacie au moment de la rédaction, Hôpital général juif, Centre intégré universitaire de santé et de services sociaux du Centre-Ouest-de-l’Île-de-Montréal, Montréal (Québec) Canada;
4Pharmacienne, Pharmacie Charrette et Trudel, Saint-Tite (Québec) Canada;
5Pharmacienne, Centre de recherche du Centre hospitalier de l’Université de Montréal, Montréal (Québec) Canada
Reçu le 12 juillet 2018: Accepté après révision par les pairs le 29 novembre 2018
Titre de l’article : Efficacy and safety of degludec versus glargine in type 2 diabetes. N Engl J Med 2017;377:723-321.
Auteurs : Marso SP, McGuire DK, Zinman B, Poulter NR, Emerson SS, Pieber TR et coll. pour le groupe d’étude DEVOTE
Commanditaires : L’étude a été financée par Novo Nordisk et par la National Institutes of Health. La compagnie pharmaceutique Novo Nordisk a mené l’étude et participé à l’analyse des données.
Cadre de l’étude : L’insuline est un médicament fort utile pour le traitement du diabète de type 2 (DB2) lorsque les autres traitements antidiabétiques ne permettent plus d’atteindre les cibles glycémiques2. À la suite de problèmes d’innocuité cardiovasculaire (CV) causés par certains antidiabétiques oraux sur le marché, la Food and Drug Administration (FDA) exige depuis 2008 que soit évalué le risque CV des nouveaux médicaments pour le traitement du DB24. La nouvelle insuline dégludec, approuvée au Canada depuis août 2017, est une insuline basale à action ultraprolongée avec une demi-vie d’environ 25 heures, associée à une plus faible variabilité de l’effet hypoglycémiant et un risque moindre d’hypoglycémie comparativement à l’insuline glargine5–7. Afin de répondre aux exigences de la FDA, des investigateurs ont comparé l’insuline dégludec à la glargine, dont la sécurité CV a été démontrée dans l’étude ORIGIN, qui l’a comparée au traitement standard8. L’étude DEVOTE évalue donc le risque CV et l’innocuité de l’insuline dégludec comparativement à la glargine pour les personnes diabétiques de type 2.
Protocole de recherche : DEVOTE est une étude à répartition aléatoire, multicentrique (438 sites dans 20 pays), contrôlée avec comparateur actif, avec groupes parallèles et à double insu. Il s’agit d’une étude de non-infériorité avec une marge supérieure maximale prédéfinie à 1,3, comme le recommande la FDA4. Les analyses statistiques étaient effectuées en intention de traiter. En cas de non-infériorité, les investigateurs évaluaient sa supériorité selon le nombre d’épisodes et l’incidence d’hypoglycémies sévères entre les deux insulines. Après la répartition aléatoire, ils rencontraient les patients hebdomadairement pendant deux semaines, puis mensuellement durant six mois, puis aux trois mois jusqu’à la fin de l’étude. Un dernier suivi était prévu 30 jours après l’arrêt du médicament à l’étude. Les données des patients sans évènement étaient prises en compte jusqu’au dernier suivi réalisé. L’apparition d’effets indésirables graves et l’observance au médicament à l’étude étaient abordées à chaque suivi. L’étude était conçue pour se poursuivre jusqu’à la survenue de 633 événements relatifs à l’objectif primaire.
Patients : Les patients inclus dans l’étude avaient un diagnostic de DB2 et présentaient un risque CV élevé. Les critères d’inclusion et d’exclusion sont présentés au tableau I.
Tableau I Principaux critères d’inclusion et d’exclusiona

Interventions : Les patients ont été répartis aléatoirement selon le ratio 1:1 pour recevoir de l’insuline dégludec ou glargine une fois par jour entre le souper et le coucher, en plus de leurs traitements usuels. Les patients préalablement sous insuline prandiale ou qui devaient commencer à en prendre pendant l’étude étaient traités avec de l’insuline asparte fournie par Novo NordiskMD. Les doses d’insuline étaient ajustées hebdomadairement selon la valeur la plus basse de trois automesures de glycémie avant le petit déjeuner pour atteindre une glycémie à jeun entre 4 et 5 mmol/L. Chez les patients jugés vulnérables, la cible se situait entre 5 et 7 mmol/L.
Points évalués : L’objectif primaire était formé d’un ensemble composite, comportant la mort de cause CV, l’infarctus du myocarde non fatal et l’accident vasculaire cérébral (AVC) non fatal. Le nombre et l’incidence d’hypoglycémies sévères étaient mesurés dans les objectifs secondaires ajustés pour la multiplicité. Les objectifs secondaires prenaient en compte l’ensemble composite primaire avec des modifications (objectif primaire et angine instable nécessitant une hospitalisation), les hypoglycémies nocturnes sévères, le temps entre la répartition aléatoire et la mortalité toutes causes confondues, les effets indésirables sévères ou menant à un arrêt de traitement, l’hémoglobine glyquée (HbA1c), la glycémie à jeun, la pression artérielle, la fréquence cardiaque, le bilan lipidique, le poids, l’indice de masse corporelle, le débit de filtration glomérulaire estimé et les doses d’insuline basale et en bolus. Les tests de laboratoire étaient mesurés lors de la répartition aléatoire, puis annuellement, sauf l’HbA1c qui était mesurée aux trois mois pendant un an, puis annuellement. Un comité adjudicateur indépendant et à l’aveugle évaluait les événements cliniques inclus dans les objectifs composites et les hypoglycémies sévères en plus de classifier les néoplasies rapportées.
Résultats : Parmi les 8205 patients recrutés, 7637 ont été répartis aléatoirement, soit 3818 dans le groupe insuline dégludec et 3819 dans le groupe insuline glargine. Ces patients ont été traités en moyenne pendant 1,83 année et suivis pendant 1,99 année. Seuls 2 % des patients n’ont pas complété l’ensemble des suivis planifiés. Le statut vital de 0,1 % des patients n’était pas connu.
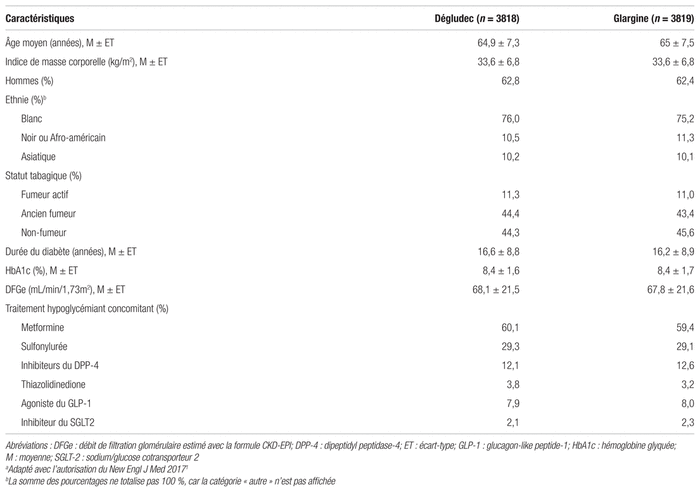
Seules les principales caractéristiques de base des patients sont présentées au tableau II par souci de concision. L’ensemble des caractéristiques de base documentées indique que les deux groupes étaient comparables. La majorité des patients provenaient d’Amérique du Nord (69 %) et avaient une maladie CV ou une maladie rénale chronique modérée préexistante (85,2 %). En moyenne, les patients souffraient de DB2 depuis 16,4 ans et avaient une HbA1c de 8,4 %. De plus, 83,9 % des patients étaient sous insuline, environ 80 % sous statine et 80 % sous inhibiteur du système rénine-angiotensine-aldostérone au moment de la répartition aléatoire. Les traitements concomitants ciblant le DB2 et les facteurs de risque CV n’étaient pas significativement différents entre les groupes, tant au recrutement qu’à la fin de l’étude.
Tableau II Caractéristiques principales de la population au début de l’étudea
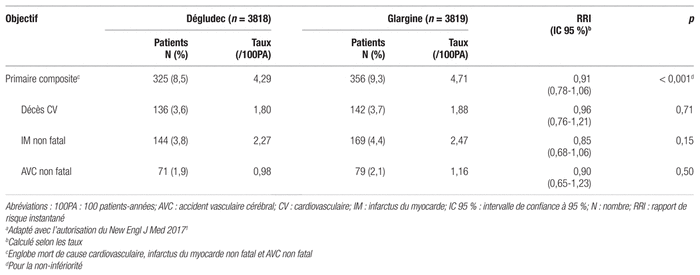
Les principaux résultats sont présentés au tableau III. L’objectif primaire a été atteint par 8,5 % des patients du groupe insuline dégludec, et 9,3 % des patients du groupe comparateur (ratio de risques instantanés [RRI]: 0,91; intervalle de confiance à 95 % [IC 95 %]: 0,78–1,06). Le résultat de l’objectif primaire était cohérent avec ceux des objectifs qui le composent analysés individuellement et avec le résultat de l’objectif composite secondaire. De plus, les résultats de non-infériorité pour l’objectif primaire étaient corroborés par les analyses de sensibilité, dont une analyse per protocole (RRI: 0,90; IC 95 %: 0,77–1,06).
Tableau III Résultats de l’objectif primairea
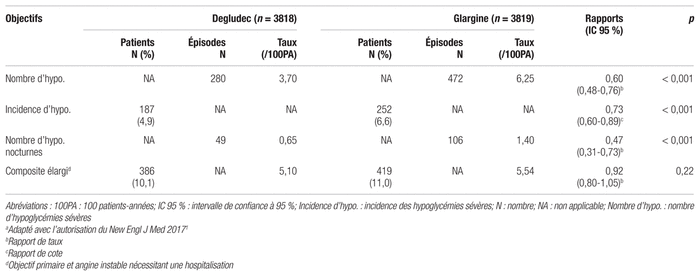
Pour ce qui est des objectifs secondaires, le taux d’hypoglycémies sévères était de 3,70 par 100 patients-années dans le groupe insuline dégludec comparativement à 6,25 par 100 patients-années dans le groupe insuline glargine. La proportion de patients ayant eu au moins un épisode d’hypoglycémie sévère a été de 4,9 % dans le groupe insuline dégludec et 6,6 % dans le groupe comparateur. Ces résultats sont présentés au tableau IV. De plus, la proportion de patients ayant eu au moins un épisode nocturne d’hypoglycémie sévère a été de 1 % dans le groupe insuline dégludec et 1,9 % dans le groupe comparateur.
Tableau IV Principaux résultats des objectifs secondairesa
Les analyses de sous-groupes montraient un nombre similaire ou inférieur d’hypoglycémies sévères avec l’insuline dégludec comparativement à la glargine. Les résultats d’autres objectifs secondaires pertinents sont rassurants, bien qu’exploratoires. Les taux d’effets secondaires agglomérés ont été de 44,7 par 100 patients-années dans le groupe insuline dégludec et de 50,1 par 100 patients-années dans le groupe insuline glargine. Les taux d’effets secondaires ayant mené à un arrêt de traitement ont été de 3,7 par 100 patients-années dans le groupe insuline dégludec et de 4,0 par 100 patients-années dans le groupe comparateur.
Grille d’évaluation critique

Discussion
Dans l’étude DEVOTE, composée de patients souffrant d’un DB2 et exposés à un risque CV élevé, l’insuline dégludec s’est montrée non inférieure à la glargine pour la survenue d’événements CV majeurs et supérieure pour le risque d’hypoglycémie sévère dans l’objectif secondaire.
Cette étude avait un protocole de recherche optimal. La taille de l’échantillon était suffisamment importante pour limiter le biais de confusion. Les caractéristiques de base colligées étaient pertinentes et exhaustives, ce qui permettait d’évaluer la similarité des groupes et de caractériser la population à l’étude. D’ailleurs, les différences entre les groupes concernant les résultats de l’HbA1c, l’amorce de nouveaux traitements antidiabétiques et les doses d’insulines utilisées n’étaient pas significatives, ce qui porte à croire que la similarité de la tolérance des deux insulines n’était pas influencée par un contrôle glycémique différent entre les groupes. Les patients vulnérables, soit 27 % des patients du groupe insuline dégludec et 26,2 % des patients du groupe glargine, avaient des cibles glycémiques plus flexibles. Bien que les critères de vulnérabilité n’aient pas été explicités, il est rassurant de constater que la proportion de patients vulnérables était similaire dans les deux groupes. Par ailleurs, aucune différence entre les groupes n’est apparue concernant l’utilisation d’antidiabétiques, dont ceux associés à une diminution du risque CV, soit les inhibiteurs du cotransporteur sodium/glucose de type 2 (SGLT2), les agonistes du récepteur du peptide-1 apparenté au glucagon humain (GLP-1) et la metformine, ce qui limite la présence d’une variable confondante. La population de DEVOTE est représentative des patients exposés à un risque CV élevé, mais elle ne représente pas la majorité des patients diabétiques rencontrés en clinique. Les objectifs CV visés et leur évaluation par un comité adjudicateur étaient appropriés et correspondaient aux recommandations de la FDA4. L’insuline glargine représentait un comparateur adéquat, puisqu’elle est considérée comme l’insuline basale de référence et que sa sécurité CV avait été évaluée au préalable8.
Les objectifs primaires étaient identiques dans DEVOTE et ORIGIN, l’étude qui a démontré la sécurité CV de l’insuline glargine par rapport au traitement standard, mais les populations étudiées n’étaient pas comparables8. ORIGIN étudiait des patients intolérants au glucose (11,5 %) et exposés à un risque CV plus faible, avec une durée moyenne de DB2 de 5,4 ans, une HbA1c médiane de 6,4 % et une proportion de patients sous statine de 53,7 %8. Bien que le suivi moyen de DEVOTE respectait les exigences de la FDA, il était beaucoup plus court que celui d’ORIGIN (deux ans comparativement à 6,4 ans), ce qui aurait pu limiter la détection d’effets CV tardifs4. Ces différences remettent donc en question la validité de la comparaison de non-infériorité8. Les auteurs rapportent un nombre nécessaire à traiter de 40, plutôt que 59, pour éviter une hypoglycémie sévère calculé à partir du taux d’évènements. Les hypoglycémies pouvant survenir à plusieurs reprises chez un même patient, le calcul des auteurs est statistiquement erroné et gonfle artificiellement les avantages de l’insuline dégludec9. Sur le plan éthique, bien que la compagnie ait participé à l’analyse des données, le protocole avait été publié antérieurement et les évènements ont été évalués par un comité adjudicateur.
L’étude BRIGHT, publiée après l’étude DEVOTE, a montré une efficacité et une sécurité similaires entre l’insuline dégludec et l’insuline glargine à 300 UI/mL10. D’ailleurs, les lignes directrices d’avril 2018 de Diabète Canada recommandent d’envisager l’insuline dégludec ou l’insuline glargine à 300 unités/mL, plutôt que la glargine à 100 unités/mL, pour réduire le risque global d’hypoglycémie et les hypoglycémies nocturnes2. Du point de vue de l’accessibilité aux traitements, seule l’insuline glargine à 300 unités/mL n’est pas remboursée par le régime général d’assurance médicaments du Québec11. Quant à l’insuline dégludec et à l’insuline glargine à 100 unités/mL, elles ont un statut de médicament d’exception pour le traitement du diabète lorsqu’une insuline à action intermédiaire n’a pas permis l’atteinte des cibles de glycémies sans causer des hypoglycémies sévères ou récurrentes11. L’Institut national d’excellence en santé et services sociaux a cependant jugé que l’insuline dégludec était non efficiente par rapport à l’insuline glargine biosimilaire (BasaglarMD) pour le traitement du DB212.
En somme, considérant son prix plus élevé et son efficacité similaire, l’insuline dégludec n’est présentement pas à prioriser pour tous les patients nécessitant une insuline basale, mais elle représente une option supplémentaire dans l’arsenal thérapeutique surtout pour les patients ayant des hypoglycémies sous insuline glargine. L’insuline dégludec serait une solution de remplacement particulièrement lors d’hypoglycémies globales sévères et même lors d’hypoglycémies nocturnes sévères, puisqu’elle s’est démarquée de l’insuline glargine dans ces situations.
Conclusion
L’étude DEVOTE démontre de façon adéquate l’efficacité et sécurité CV de l’insuline dégludec comparativement à l’insuline glargine. Chez les patients souffrant d’une maladie CV établie, les résultats des objectifs secondaires pointent vers une diminution du risque d’hypoglycémie en faveur de l’insuline dégludec, ce qui abonde dans le même sens que certaines études antérieures. Bien que cette insuline soit remboursée comme médicament d’exception, son coût supérieur et ses données de sécurité sur une période limitée pourraient justifier sa prescription uniquement pour une population dont on juge qu’elle est exposée à un risque élevé d’hypoglycémie.
Financement
Aucun financement en relation avec le présent article n’a été déclaré par les auteurs.
Conflits d’intérêts
Tous les auteurs ont rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts en relation avec le présent article.
Remerciements
Cet article a été réalisé dans le cadre du cours Communication scientifique de la Faculté de pharmacie de l’Université de Montréal. Les auteurs remercient les responsables. Une autorisation écrite a été obtenue de ces personnes.
Références
1. Marso SP, McGuire DK, Zinman B, Poulter NR, Emerson SS, Pieber TR et coll. Efficacy and safety of degludec versus glargine in type 2 diabetes. N Engl J Med 2017;377:723–32.


2. Diabetes Canada Clinical Practice Guidelines expert committee. Diabetes Canada 2018 clinical practice guidelines for the prevention and management of diabetes in Canada. Can J Diabetes 2018;42(Suppl 1):S1–S325.
3. Currie CJ, Johnson JA. The safety profile of exogenous insulin in people with type 2 diabetes: justification for concern. Diabetes Obes Metab 2012;14:1–4.

4. U.S. department of health and human services, food and drug administration, center for drug evaluation and research. Guidance for industry - diabetes mellitus-evaluating cardiovascular risk in new antidiabetic therapies to treat type 2 diabetes. [en ligne] https://www.fda.gov/downloads/Drugs/Guidances/ucm071627.pdf (site visité le 14 janvier 2018).
5. Novo Nordisk. Monographie du degludec (Tresiba). Mississauga, Ontario. Août 2017.
6. Ratner RE, Gough SC, Mathieu C, Del Prato S, Bode B, Mersebach H et coll. Hypoglycaemia risk with insulin degludec compared with insulin glargine in type 2 and type 1 diabetes: a preplanned meta-analysis of phase 3 trials. Diabetes Obes Metab 2013;15:175–84.

7. Heise T, Hermanski L, Nosek L, Feldman A, Rasmussen S, Haahr H. Insulin degludec: four times lower pharmacodynamic variability than insulin glargine under steady-state conditions in type 1 diabetes. Diabetes Obes Metab 2012;14:859–64.

8. Gerstein HC, Bosch J, Dagenais GR, Díaz R, Jung H, Maggioni AP et coll. Basal insulin and cardiovascular and other outcomes in dysglycemia. N Engl J Med 2012;367:319–28.

9. Aaron SD, Fergusson DA. Exaggeration of treatment benefits using the “event-based” number needed to treat. Can Med Assoc J 2008; 179:669–71.

10. Rosenstock J, Cheng A, Ritzel R, Bosnyak Z, Devisme C, Cali AM et coll. More similarities than differences testing insulin glargine 300 units/mL versus insulin degludec 100 units/mL in insulin-naïve type 2 diabetes: the randomized head-to-head BRIGHT trial. Diabetes Care 2018;41:2147–54.

11. Régie assurance maladie du Québec. Liste des médicaments mise à jour le 27 septembre 2018. [en ligne] http://www.ramq.gouv.qc.ca/SiteCollectionDocuments/liste_med/liste_med_2018_09_27_fr.pdf (site visité le 5 novembre 2018).
12. Institut national d’excellence en santé et en services sociaux. TresibaMC FlextouchMC - Avis transmis au ministre en mars 2018. [en ligne] https://www.inesss.qc.ca/fileadmin/doc/INESSS/Inscription_medicaments/Avis_au_ministre/Avril_2018/Tresiba_Flex_Touch_2018_03.pdf?sword_list%5B0%5D=tresiba&no_cache=1 (site visité le 10 novembre 2018).
Pour toute correspondance: Charlie Li Lamoureux, Hôpital Maisonneuve-Rosemont, 5415, boulevard de l’Assomption (Québec) H1T 2M4, CANADA; Téléphone: 514-883-8553; Courriel: charlieli.lamoureux@hotmail.com
*Charlie Li Lamoureux et Jean-François Provencher ont contribué de façon équivalente à la rédaction de cet article (
Return to Text
)
(Return to Top)
PHARMACTUEL, Vol. 52, No. 1, 2019