Prise en charge de l’extravasation de médicaments non cytotoxiques par voie intraveineuse périphérique
Joanie Turcotte1,2, B.Pharm., M.Sc., Julie Racicot1,2,3, B.Pharm., M.Sc.
1Pharmacienne, Institut universitaire de cardiologie et de pneumologie de Québec – Université Laval, Québec (Québec) Canada;
2Chargée d’enseignement clinique, Faculté de pharmacie, Université Laval, Québec (Québec) Canada;
3Professeure de clinique, Faculté de pharmacie, Université Laval, Québec (Québec) Canada
Reçu le 27 novembre 2018: Accepté le 16 janvier 2019
Exposé de la question
L’administration de médicaments par voie intraveineuse périphérique comporte certains risques, notamment le potentiel d’infiltration. L’infiltration d’un médicament peut impliquer un agent irritant, un agent vésicant ou un agent non vésicant et non irritant. L’extravasation correspond spécifiquement à l’infiltration d’un médicament au potentiel vésicant, c’est-à-dire pouvant causer des dommages cellulaires et tissulaires sous-cutanés ou périvasculaires1,2. Les signes et les symptômes initiaux caractéristiques comprennent l’absence ou la diminution du retour veineux, l’œdème, la décoloration, l’érythème, l’induration ainsi que la douleur, qui peut être décrite comme une sensation de brûlure, de démangeaison ou de picotement. La formation de cloques ou d’ulcères, la desquamation et la nécrose tissulaire peuvent en résulter1,3–5.
L’extravasation est une cause de morbidité iatrogénique, de prolongation de la durée d’hospitalisation ainsi que d’augmentation des coûts d’hospitalisation6–8. L’extravasation des médicaments cytotoxiques antinéoplasiques est la plus fréquente. Sa prévention et sa prise en charge font l’objet de guides de pratique clinique4. L’extravasation des médicaments non cytotoxiques est quant à elle moins bien documentée. En effet, aucun guide de pratique n’est publié sur le sujet et les données probantes appuyant les modalités de prise en charge reposent sur la publication de rapports de cas et de séries de cas ou d’études animales6–8.
Réponse à la question
Les facteurs de risque associés à l’extravasation sont liés au patient, à la technique d’administration, au personnel et au médicament. Ceux liés au patient comprennent l’âge, le poids, les comorbidités et l’état cognitif, alors que ceux liés à la technique regroupent la dilution, la vitesse et la durée d’administration, le choix du site et du calibre de la veine ainsi que celui du cathéter. Les facteurs de risque associés au personnel englobent la connaissance et l’application des mesures de prévention, de reconnaissance et de prise en charge de l’extravasation2–4,6,8.
Les facteurs de risque liés au médicament dépendent de ses propriétés pharmacologiques et de ses caractéristiques physico-chimiques. Ils incluent le potentiel vasoconstricteur, l’osmolarité et le pH3,6–8. Les médicaments ayant un potentiel vasoconstricteur regroupent les dérivés des catécholamines, le bleu de méthylène, la vasopressine et le calcium. Il n’existe pas de lien entre l’effet systémique attendu et l’effet local observé lors d’extravasation des catécholamines. Par exemple, il est attendu que la dopamine à faible dose produise peu de vasoconstriction périphérique, mais plutôt une vasodilatation rénale et mésentérique en plus d’un effet inotrope positif. Par contre, les rapports de cas de nécrose tissulaire à la suite de son extravasation font état de son potentiel vasoconstricteur local7,9–10. L’osmolarité sérique est d’environ 300 mOsm/L. L’infiltration d’un médicament ayant une osmolarité supérieure à 600 mOsm/L peut causer des dommages cellulaires et tissulaires. Les formulations hyperosmolaires regroupent principalement les agents de contraste, les électrolytes concentrés et la nutrition parentérale. Les agents hypo-osmolaires pourraient également causer ce type de dommages, mais de façon moins importante que les agents hyperosmolaires6. Le pH sérique se situe entre 7,35 et 7,45. L’infiltration d’un médicament ayant un pH inférieur à cinq ou supérieur à neuf peut causer des dommages cellulaires ou tissulaires2,8. Le potentiel de lésion des agents alcalins est plus important que celui des acides. Les médicaments acides et alcalins regroupent l’acyclovir, l’amiodarone, le ganciclovir, la pentamidine, le phénobarbital, la phénytoïne et la vancomycine. Par ailleurs, l’amphotéricine B, le diazépam, le lorazépam et le propofol sont également des médicaments pouvant causer des extravasations, malgré l’absence de facteur de risque sur le plan des propriétés pharmacologiques et des caractéristiques physico-chimiques. Pour certains d’entre eux, c’est la présence de propylène glycol dans la formulation qui serait en cause6.
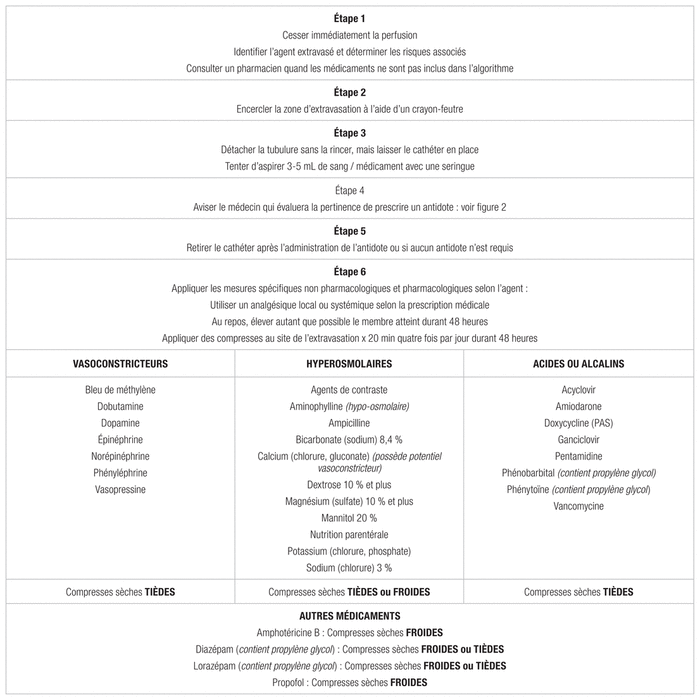
Un algorithme de prise en charge spécifique de l’extravasation de médicaments non cytotoxiques par voie périphérique est présenté à la figure 12–4.
| |
|
|
|
Figure 1 Algorithme pour la prise en charge de l’extravasation de médicaments non cytotoxiques par voie périphérique.
Abréviations : PAS : programme d’accès spécial
L’autorisation de reproduire cette figure a été obtenue du Dr Daniel Lefrançois, directeur des services professionnels, IUCPQ-UL
|
Cet algorithme propose une démarche incluant la reconnaissance des médicaments à risque ainsi que les modalités d’application des mesures non pharmacologiques et pharmacologiques. La liste de médicaments n’est pas exhaustive et ceux-ci ont été sélectionnés selon le risque d’extravasation documenté, la disponibilité au Canada et la possibilité de leur utilisation pour la patientèle adulte d’un centre hospitalier universitaire tertiaire axé sur la cardiologie et la pneumologie. Lors de la survenue d’une extravasation, la perfusion du médicament doit d’abord être suspendue. Avant de retirer le cathéter en place, l’aspiration du liquide contenu dans la zone d’extravasation doit être tentée. Le cathéter peut ensuite être retiré ou après l’administration de l’antidote. Une fois le cathéter retiré, l’élévation du membre affecté favorisera l’élimination du médicament par la circulation sanguine et lymphatique1,3,5–8.
Bien qu’il n’existe aucune démonstration des bienfaits cliniques des compresses, on recommande toujours d’en appliquer lors de la prise en charge d’une extravasation8. Les compresses humides doivent être évitées, car elles peuvent favoriser la macération et la desquamation de la peau2. Les compresses sèches sont donc à privilégier. De façon générale, l’application de compresses sèches et froides devrait permettre de réduire l’inflammation et la nécrose en plus de circonscrire la zone d’extravasation en limitant l’absorption et la distribution du produit grâce à la vasoconstriction. Quant à l’application de compresses sèches et tièdes, elle devrait d’abord promouvoir la vasodilatation, mais également la dilution, l’absorption et la distribution du médicament impliqué pour limiter les dommages cellulaires et tissulaires en réduisant la concentration du médicament et la durée d’exposition. Elles sont appropriées lors d’agents causaux, tels que les vasoconstricteurs, les hyperosmolaires, les acides ou les alcalins. L’application de compresses sèches et froides est une option lors d’une extravasation d’agents hyperosomolaires6,7.
On recommande l’administration d’un vasodilatateur comme antidote lors de l’extravasation d’un médicament vasoconstricteur. La phentolamine est l’antidote indiqué en présence des dérivés des catécholamines, tandis que les nitrates peuvent être utilisés lorsque le bleu de méthylène ou la vasopressine sont en cause6,7. Une controverse entoure l’utilisation de l’hyaluronidase pour l’extravasation de médicaments hyperosmolaires, acides ou alcalins6. L’hyaluronidase est une enzyme qui détruit l’acide hyaluronique, l’acide
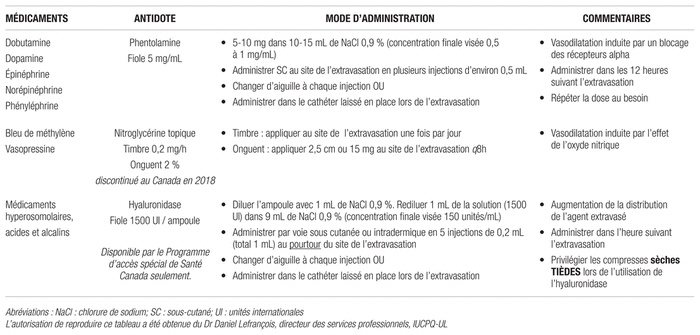
chondroïtique et le sulfate de mucoïtine des tissus conjonctifs, ce qui devrait permettre l’absorption et la dispersion du médicament extravasé. Son utilisation est décrite dans des rapports de cas et les avantages cliniques obtenus sont parfois contradictoires4. Pour ce qui est des médicaments cytotoxiques, on recommande l’hyaluronidase uniquement lors de l’extravasation des alcaloïdes de la vinca3,4. Son utilisation pourrait être restreinte à certaines situations impliquant principalement des médicaments hyperosmolaires et secondairement des acides et des alcalins, mais le professionnel de la santé doit aussi prendre en considération les autres éléments associés à l’extravasation, comme les caractéristiques du patient, le volume extravasé et le site touché. L’hyaluronidase n’est pas disponible au Canada et doit être obtenue par le Programme d’accès spécial de Santé Canada. L’administration d’agents neutralisant le pH n’est jamais recommandée, car elle peut aggraver les dommages cellulaires et tissulaires par la production de chaleur ou de gaz6. Les modalités d’administration des différents antidotes sont décrites au tableau I2,11,12.
Tableau I Antidotes pour l’extravasation de médicaments non cytotoxiques par voie périphérique
Conclusion
La prise en charge de l’extravasation d’un médicament non cytotoxique par voie périphérique repose sur la reconnaissance des médicaments qui risquent de causer des dommages cellulaires et tissulaires et sur l’application des mesures non pharmacologiques avec ou sans mesures pharmacologiques appropriées. L’algorithme proposé est un outil d’aide à la gestion de cette complication, mais ne remplace pas le jugement clinique. Par exemple, pour les cas complexes impliquant des médicaments non inclus dans l’algorithme, le pharmacien pourra proposer une démarche de prise en charge adaptée au contexte. Le pharmacien peut également participer à l’élaboration de protocoles favorisant la prévention et facilitant la prise en charge de cette complication de la thérapie intraveineuse en milieu hospitalier.
Financement
Aucun financement en relation avec le présent article n’a été déclaré par les auteurs.
Conflits d’intérêts
Tous les auteurs ont rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts en relation avec le présent article.
Références
1. Hadaway L. Infiltration and extravasation. Am J Nurs 2007;107:64–72.

2. Martin SM. Extravasation management of non-chemotherapeutic medications. J Infus Nurs 2013;36:392–6.

3. Al-Benna S, O’Boyle C, Holley J. Extravasation injuries in adults. ISRN Dermatol 2013;2013:856541.

4. Institut national d’excellence en santé et services sociaux. Prise en charge de l’extravasation associée aux traitements antinéoplasiques. [en ligne] https://www.inesss.qc.ca/fileadmin/doc/INESSS/Rapports/Oncologie/INESSS_Prise_en_charge_extravasation_associee_traitements_antineoplastiques.pdf (site visité le 6 octobre 2018).
5. Dougherty L. Extravasation: prevention, recognition and management. Nurs Stand 2010;24:48–55.

6. Reynolds PM, MacLaren R, Mueller SW, Fish DN, Kiser TH. Management of extravasation injuries: a focused evaluation of noncytotoxic medications. Pharmacotherapy 2014;34:617–32.

7. Le A, Patel S. Extravasation of Noncytotoxic Drugs: A Review of the Literature. Ann Pharma-cother 2014;48:870–86.

8. Doellman D, Hadaway L, Bowe-Geddes LA, Franklin M, LeDonne J, Papke-O’Donnell L et coll. Infiltration and extravasation: update on prevention and management. J Infus Nurs 2009;32:203–11.

9. Dugger B. Peripheral dopamine infusions: are they worth the risk of infiltration? J Intraven Nurs 1997;20:95–9.
10. Chen JL, O’Shea M. Extravasation injury associated with low-dose dopamine. Ann Pharmacother 1998;32:545–8.

11. Micromedex Healthcare series. Monographie de la phentolamine. Thomson Micromedex, 1974–2018. [en ligne] http://www.thomsonhc.com (site visité le 7 octobre 2018).
12. Micromedex Healthcare series. Monographie de l’hyaluronidase. Thomson Micromedex, 1974–2018. [en ligne] http://www.thomsonhc.com (site visité le 7 octobre 2018).
Pour toute correspondance : Julie Racicot, Institut universitaire de cardiologie et de pneumologie de Québec, 2725, chemin Sainte-Foy, Québec (Québec) G1X 0A3, CANADA; Téléphone : 418 656-8711 poste 3024; Courriel : julie.racicot@ssss.gouv.qc.ca
(Return to Top)
PHARMACTUEL, Vol. 52, No. 2, 2019