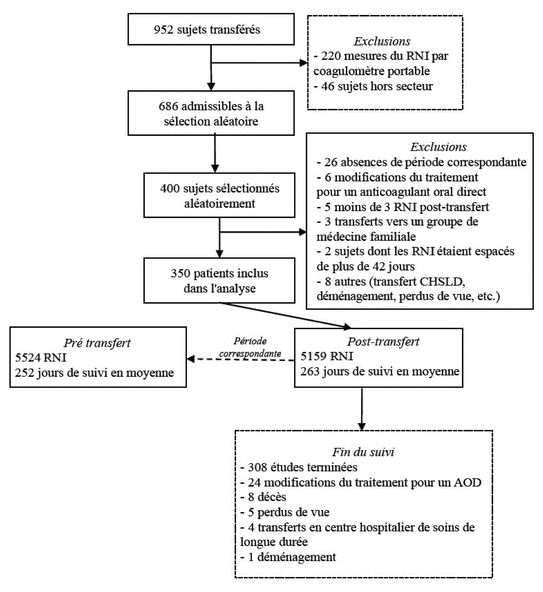
Figure 1 Sélection des sujets à l’étude
Abréviations : AOD : anticoagulant oral direct; CHSLD : centre hébergement et de soins longue durée; RNI : ratio normalisé international
Sophie Ruelland1,2,3, Pharm.D., M.Sc., Ann-Sophie Laberge1,2,4, Pharm.D., M.Sc., Louis-Étienne Marchand5, B.Pharm., M.Sc., Jean Bournival6, B.Pharm., M.Sc., Michel Dorval7,8, Ph.D.
Reçu le 8 mai 2020: Accepté après révision par les pairs le 1 septembre 2020
Résumé
Objectif : Cette étude rétrospective de dossiers vise à comparer le suivi de la warfarine effectué par le pharmacien communautaire avec celui assuré par le pharmacien d’une clinique d’anticoagulation spécialisée.
Méthodologie : Le suivi d’un même groupe de sujets stables a été comparé avant et après le transfert d’une clinique d’anticoagulation spécialisée vers le pharmacien communautaire de 2015 à 2018, pour une même période de l’année. Le temps dans l’intervalle thérapeutique, la variabilité du ratio normalisé international et la prévalence d’un ratio international normalisé extrême ont été utilisés comme indicateurs de la qualité du suivi. L’incidence des complications liées à l’anticoagulation a aussi été mesurée.
Résultats : Un total de 350 patients sous warfarine a été inclus dans les analyses, la majorité étaient anticoagulés pour de la fibrillation auriculaire. Les durées moyennes de suivi étaient respectivement de 263 jours pour le pharmacien communautaire et de 252 jours pour la clinique d’anticoagulation spécialisée. Le temps dans l’intervalle thérapeutique était de 81,2 % pour le suivi réalisé par le pharmacien communautaire et de 80,2 % à la clinique d’anticoagulation spécialisée (p = 0,38). La variabilité médiane du ratio international normalisé était de 0,13 dans le modèle pharmacien communautaire et de 0,12 dans le modèle clinique d’anticoagulation spécialisée (p = 0,14). Aucune différence quant à l’incidence des événements thromboemboliques n’a été observée.
Conclusion : Chez les sujets stables, le suivi de la warfarine par le pharmacien communautaire était de qualité comparable à celui d’une clinique d’anticoagulation spécialisée.
Mots clés : Anticoagulation, pharmacien communautaire, programme d’anticoagulothérapie, ratio international normalisé, temps dans l’intervalle thérapeutique, warfarine
Abstract
Objectif : The purpose of this retrospective chart review is to compare warfarin monitoring by community pharmacists and that by pharmacists at a specialized anticoagulation clinic.
Methodology : The monitoring of a given group of stable patients was compared before and after their transfer from a specialized anticoagulation clinic to community pharmacists from 2015 to 2018 for the same period of the year. Time within the therapeutic range, international normalized ratio variability and the prevalence of an extreme INR value were used as indicators of monitoring quality. The incidence of anticoagulation-related complications was also determined.
Results : A total of 350 patients on warfarin were included in the analyses, most of whom were being anticoagulated for atrial fibrillation. The mean duration of monitoring was 263 days for community pharmacists and 252 days for the specialized anticoagulation clinic. Time within the therapeutic range was 81.2% for monitoring by community pharmacists and 80.2% for monitoring by the specialized anticoagulation clinic (p = 0.38). Median INR variability was 0.13 in community pharmacists model and 0.12 in the specialized anticoagulation clinic model (p = 0.14). No difference in the incidence of thromboembolic events was observed.
Conclusion : In these stable patients, the quality of warfarin monitoring by community pharmacists was of comparable quality to that by a specialized anticoagulation clinic.
Keywords : Anticoagulation, anticoagulation therapy program, community pharmacist, international normalized ratio, time within the therapeutic range, warfarin
Découverte il y a plus de 60 ans, la warfarine occupe encore aujourd’hui une place importante dans le traitement et la prévention des événements thromboemboliques. La mise en marché des anticoagulants oraux directs (AOD) il y a une dizaine d’années a entraîné une diminution importante de l’usage de la warfarine1,2. Ces agents sont maintenant recommandés en première intention dans la prise en charge de la fibrillation auriculaire (FA) et des thromboembolies veineuses (TEV)3,4. Certains patients ont toutefois des contre-indications à l’utilisation des AOD et d’autres n’ont pas encore fait la transition vers ces nouvelles molécules. Selon un registre canadien, la warfarine représentait 99 % des prescriptions d’anticoagulants en 2010, comparativement à 67 % en 20145.
La warfarine requiert un suivi étroit pour assurer son efficacité et minimiser le risque de saignement6. De nombreux modèles d’ajustement sont documentés dans la littérature scientifique : suivi effectué par le médecin de famille, par une clinique spécialisée en anticoagulothérapie ou encore autogestion par le patient7. Les normes de pratique recommandent que les suivis devraient être effectués par les cliniques spécialisées en anticoagulothérapie, majoritairement intra-hospitalières au Québec8,9. Plusieurs études ont montré que la prise en charge par une clinique spécialisée en anticoagulothérapie est associée à de meilleurs indicateurs de la qualité du suivi lorsque comparée à d’autres modèles moins structurés9–12.
Au Québec, l’ajustement de la warfarine par le pharmacien communautaire est inclus dans le cadre légal depuis 2015 et est remboursé par le régime provincial d’assurance médicament13. Le transfert des suivis de la warfarine des cliniques spécialisées en anticoagulothérapie intra-hospitalières et des groupes de médecine de famille vers les pharmaciens communautaires représente une nouvelle forme de prise en charge du patient très répandue au Québec et dont la qualité du suivi est peu documentée14–16.
L’Hôtel-Dieu de Lévis (HDL) est un centre hospitalier tertiaire de 349 lits situé dans la région de Chaudière-Appalaches (Québec, Canada). De 2016 à 2017, parmi une cohorte de plus de 1500 patients, la clinique spécialisée en anticoagulothérapie de l’HDL a transféré le suivi de 952 patients stables aux pharmaciens communautaires de la région. Un patient était considéré comme stable lorsque ses résultats de ratio normalisé international (RNI) étaient espacés d’un minimum de deux semaines. L’objectif principal de cette étude était de comparer la qualité et la sécurité du suivi effectué par le pharmacien communautaire à celles du suivi réalisé à la clinique spécialisée en anticoagulothérapie de l’HDL.
Cette étude rétrospective sur dossiers médicaux compare le suivi de la warfarine réalisé par le pharmacien communautaire à celui effectué au préalable par la clinique spécialisée en anticoagulothérapie de septembre 2015 à février 2018. Les sujets étaient tous suivis initialement à la clinique spécialisée en anticoagulothérapie, puis transférés au pharmacien communautaire une fois leur RNI dans l’intervalle thérapeutique et les prélèvements espacés d’un minimum de deux semaines. Préalablement au transfert et dans l’optique de standardiser les pratiques locales, les pharmaciens de la région ont eu accès à une formation de trois heures sur l’ajustement de la warfarine (en plus des outils provinciaux déjà disponibles)17. Ils pouvaient également se référer à la clinique spécialisée en anticoagulothérapie au besoin. Le projet de recherche a été préalablement approuvé par le comité d’éthique de la recherche du Centre intégré de santé et de services sociaux de Chaudière-Appalaches.
Tous les sujets dont le suivi a été transféré de la clinique spécialisée en anticoagulothérapie au pharmacien communautaire pendant la période d’observation étaient admissibles à l’étude. Ces sujets avaient un risque hémorragique et/ou embolique faible à modéré, défini selon les paramètres suivants : FA non valvulaire avec score CHADS2 (insuffisance cardiaque, hypertension, âge de plus de 75 ans, diabète [un point chacun] et antécédent d’accident vasculaire cérébral [AVC] [deux points]) inférieur à cinq, absence de remplacement valvulaire mécanique en position mitrale ou aortique, absence de syndrome antiphospholipide, absence d’événement thromboembolique dans les trois mois précédant le transfert et absence de saignement majeur dans les 60 jours précédant le transfert. Le suivi des patients ne répondant pas à ces critères demeurait assuré par la clinique spécialisée en anticoagulothérapie. Les sujets dont la mesure du RNI était faite par prélèvement capillaire (CoaguchekMD) ou dont la durée de suivi à la clinique spécialisée en anticoagulothérapie ou par le pharmacien communautaire était inférieure à trois mois n’étaient pas admissibles. Les patients ont été sélectionnés par grappe, selon leur pharmacie communautaire. Par la suite, les patients de chaque pharmacie ont été choisis aléatoirement et stratifiés afin de bien représenter les pharmacies ayant un plus petit volume de patients (moins de 25 patients transférés). Le consentement des patients n’étant pas requis en raison du devis rétrospectif de l’étude, l’approbation du directeur des services professionnels a été obtenue avant de consulter leur dossier. Une lettre informative a été envoyée aux pharmacies communautaires pour les aviser et aucune pharmacie ne s’est retirée de l’étude.
La collecte de données a été réalisée à l’aide du dossier patient électronique qui regroupe les données démographiques, les antécédents médicaux, les hospitalisations et visites à l’urgence, ainsi que les valeurs de laboratoire des sujets. Ces dossiers électroniques sont ceux de l’HDL, le seul centre hospitalier tertiaire de la région. Les données démographiques et les antécédents médicaux sont le portrait des patients au moment du transfert. Tous les RNI de la région de Chaudière-Appalaches sont analysés de façon centralisée au laboratoire de l’HDL.
Les événements thromboemboliques et les saignements survenus pendant la période à l’étude ont été comptabilisés. Un événement thromboembolique est défini comme un nouveau diagnostic d’AVC, d’ischémie cérébrale transitoire (ICT), d’embolie pulmonaire, de thrombose veineuse profonde ou autre embolie artérielle. Les saignements sont classifiés comme majeurs, non majeurs cliniquement significatifs, ou mineurs selon la méthode de l’International Society on Thrombosis and Haemostasis pour les patients non chirurgicaux18. La classification des événements a été faite initialement par les deux chercheuses principales et a été révisée à l’aveugle par un cardiologue de l’HDL.
Les scores CHA2DS2-VASc (insuffisance cardiaque, hypertension, présence de maladie vasculaire, âge entre 65 et 74 ans, sexe féminin, diabète [un point chacun] et antécédent d’AVC et âge de 75 ans ou plus [deux points]) et HAS-BLED modifié (hypertension, insuffisance rénale et/ou hépatique, antécédent d’AVC, antécédent de saignement majeur ou prédisposition aux saignements, RNI labile, âge de plus de 65 ans, médication prédisposant aux saignements et consommation d’alcool [1 point chacun]) permettent de décrire le risque embolique et hémorragique des sujets à l’étude. Le score HAS-BLED modifié a été utilisé puisqu’il était difficile, dans un contexte rétrospectif, de connaître le contrôle de la pression artérielle du patient et sa consommation réelle d’alcool au moment du transfert. Un diagnostic d’hypertension noté au dossier ou la prise d’antihypertenseurs, ainsi qu’une prise d’alcool mentionnée dans le dossier ont été considérés pour le calcul19.
Le temps dans l’intervalle thérapeutique a été calculé selon la méthode de Rosendall et représente le pourcentage du temps passé dans l’intervalle de RNI visé en extrapolant de façon linéaire les RNI entre les résultats20. Le temps dans l’intervalle thérapeutique étendu a aussi été calculé par la même méthode en considérant une cible de RNI étendue correspondant à la cible réelle ± 0,2 unité. Les résultats de RNI espacés de plus de six semaines ont été exclus du calcul du temps dans l’intervalle thérapeutique. Les périodes où le patient était hospitalisé ont également été exclues du calcul. La variabilité du RNI a été évaluée selon la méthode B2 de Finh et représente le calcul de la variance entre chaque RNI pondérée par le temps. Un patient dont les RNI varient grandement est considéré comme moins stable, augmentant ainsi son risque d’événements thromboemboliques21. Les valeurs de RNI extrêmes, soit inférieures à 1,5 ou supérieures à cinq, ont aussi été collectées22.
Les analyses comparatives ont été effectuées sur le même groupe de patients, soit avant et après leur transfert au pharmacien communautaire. Le temps dans l’intervalle thérapeutique, le temps dans l’intervalle thérapeutique étendu, la variation du RNI et le nombre de RNI extrêmes ont été comparés pour la même période de l’année, à un an d’intervalle. Par exemple, pour un patient suivi par le pharmacien communautaire de juillet à décembre 2017, la période de juillet à décembre 2016 suivie par la clinique spécialisée en anticoagulothérapie servira de comparateur. Chaque patient était ainsi son propre comparateur, et des périodes de durée identique étaient comparées. Cette façon de procéder a permis de limiter l’impact que pourraient avoir les variations saisonnières sur la stabilité de l’anticoagulothérapie23. La période d’ajustement par la clinique spécialisée en anticoagulothérapie correspondant aux trois premiers mois de traitement par warfarine a été exclue en raison de la plus grande instabilité du RNI en début de traitement. La fin de la période d’observation correspond principalement à la date de fin d’étude, à un déménagement dans une autre région, au décès du sujet, à l’arrêt de l’anticoagulothérapie ou au remplacement de la warfarine par un AOD.
Les données démographiques sont présentées en termes de moyenne et de médiane. Des tests de Student pour données appariées ainsi que des tests de Wilcoxon ont été réalisés afin de comparer les moyennes et les médianes des temps dans l’intervalle thérapeutique, des temps dans l’intervalle thérapeutique étendus ainsi que la variabilité du RNI entre les deux modèles. Une taille d’échantillon de 350 patients permettait d’obtenir une puissance d’au moins 85 % et de détecter une différence de 5 % entre les temps dans l’intervalle thérapeutique des deux modèles. En estimant un taux d’exclusion de 10 %, 400 patients ont été sélectionnés dans l’étude24.
Des analyses de sous-groupe prédéfinies ont été réalisées afin d’observer si certaines covariables influençaient la qualité du suivi par le pharmacien communautaire. Les patients ont ainsi été stratifiés 1) selon le nombre de patients transférés par pharmacie (moins de 25 patients transférés vs 25 patients ou plus); et 2) selon la stabilité de leur RNI (temps dans l’intervalle thérapeutique inférieur à 70 % pendant le suivi avec la clinique spécialisée en anticoagulothérapie vs temps dans l’intervalle thérapeutique supérieur ou égal à 70 %). La période post hospitalisation a aussi fait l’objet d’analyses supplémentaires. Les indicateurs de la qualité du suivi (temps dans l’intervalle thérapeutique, temps dans l’intervalle thérapeutique étendu et variabilité du RNI) ont été calculés pour les 28 jours suivant chaque hospitalisation ou chaque visite à l’urgence survenue durant la période de l’étude.
Préalablement, 400 sujets répondant aux critères d’inclusion ont été sélectionnés aléatoirement. Parmi ceux-ci, 50 ont été exclus, principalement en raison d’une durée de suivi trop courte (moins de trois mois) suivant le transfert et lorsque la période de l’année correspondante pour les deux modèles de suivi incluait le début du traitement (figure 1). Un total de 350 patients a été inclus dans l’analyse avec une durée de suivi moyenne de 263 jours pour le pharmacien communautaire et de 252 jours pour la clinique d’anticoagulation spécialisée. Pour la période de suivi, 5159 RNI ont été réalisés par les différents pharmaciens communautaires et 5224 par la clinique d’anticoagulation spécialisée, soit une moyenne de 1,58 RNI par 28 jours pour le pharmacien communautaire et de 1,66 pour la clinique d’anticoagulation spécialisée. La grande majorité des sujets (72,9 %) étaient anticoagulés pour de la FA et 20 % étaient traités pour une TEV. L’intervalle de RNI ciblé pour 97,1 % des sujets était de 2 à 3. Le score CHADS2-VASC moyen était de 4,2, et 12,9 % des patients avaient une thérapie antiplaquettaire concomitante (tableau I).
|
|
||
|
Figure 1 Sélection des sujets à l’étude |
||
Tableau I Caractéristiques des patients à l’étude (n = 350)
Lorsque l’on compare les résultats des temps dans l’intervalle thérapeutique moyens et des temps dans l’intervalle thérapeutique étendus médians, on ne note aucune différence significative entre le suivi effectué par le pharmacien communautaire et celui réalisé par la clinique spécialisée en anticoagulothérapie (tableau II). Le temps moyen entre les RNI est similaire pour les deux modèles, soit 17,8 jours pour le pharmacien communautaire et 16,9 jours pour la clinique spécialisée en anticoagulothérapie. Le pharmacien communautaire et la clinique d’anticoagulation spécialisée obtiennent des pourcentages similaires de RNI extrêmes. Pour chaque modèle, il y a environ cinq fois plus de RNI inférieurs à 1,5 que de RNI supérieurs à 5,0. Le temps moyen passé en dessous l’intervalle thérapeutique est de 5,2 % lors du suivi réalisé par le pharmacien communautaire et de 5,3 % pour la clinique spécialisée en anticoagulothérapie (p = 0,92). La variabilité médiane du RNI est de 0,13 dans le modèle pharmacien communautaire et de 0,12 pour la clinique spécialisée en anticoagulothérapie (p = 0,14).
Tableau II Déterminants de la qualité du suivi pour le pharmacien communautaire et la clinique d’anticoagulation spécialisée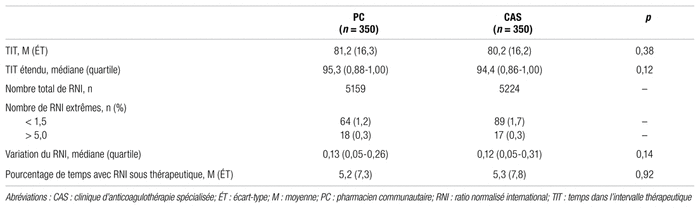
Un total de 72 patients, soit 21 % de la cohorte, avait un suivi considéré comme moins stable pendant la période de suivi réalisé par la clinique spécialisée en anticoagulothérapie (défini comme un temps dans l’intervalle thérapeutique inférieur à 70 %). Les temps dans l’intervalle thérapeutique moyens pour ce sous-groupe de patients étaient de 76,1 % pour le pharmacien communautaire et de 56,4 % pour la clinique d’anticoagulation spécialisée (p = 0,0001).
L’influence du volume de patients sous warfarine suivis dans chaque pharmacie communautaire a aussi été étudiée, soit les pharmacies communautaires suivant moins de 25 patients ou 25 patients ou plus. Aucune différence statistiquement significative n’a été décelée entre les temps dans l’intervalle thérapeutique moyens chez les deux groupes (81,3 % et 81,0 %, p = 0,61).
Pendant la période de l’étude, nous avons relevé 55 hospitalisations à l’HDL, soit 30 pendant la période de suivi par la clinique spécialisée en anticoagulothérapie et 25 par le pharmacien communautaire. Le nombre moyen de RNI par patient demandés dans les 28 jours suivant une hospitalisation était similaire selon les deux types de suivi, soit 6,2 par le pharmacien communautaire et 6,1 par la clinique spécialisée en anticoagulothérapie. Les temps dans l’intervalle thérapeutique moyens dans les 28 jours suivant une hospitalisation étaient de 55,4 % (écart-type [ÉT] = 31,2) pour le pharmacien communautaire et de 63,9 % (ÉT = 23,4) pour la clinique spécialisée en anticoagulothérapie (p = 0,27).
Six événements thromboemboliques et trois saignements majeurs ont eu lieu pendant l’étude. La répartition des événements est présentée au tableau III. Aucun de ces événements n’a entraîné un décès. Pendant la période de suivi, huit sujets sont décédés. La cause du décès n’était pas en lien avec l’anticoagulation ou demeurait inconnue dans tous les cas.
Tableau III Événements indésirables survenus pendant la période d’observation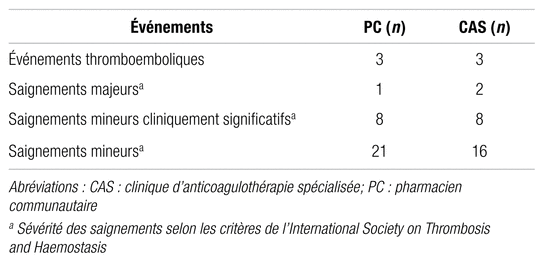
Trois événements thromboemboliques se sont produits pendant le suivi du pharmacien communautaire, soit deux ICT et un AVC. Deux des trois événements sont survenus malgré un RNI thérapeutique. Le troisième s’est présenté avec un ICT et un RNI sous-thérapeutique à 1,14. Le mauvais contrôle du RNI a été imputé à la mauvaise adhésion du patient à son traitement. Par ailleurs, trois événements thromboemboliques se sont produits pendant le suivi réalisé par la clinique spécialisée en anticoagulothérapie, soit un ICT, un AVC et une thrombose ilio-fémorale. Seule la thrombose artérielle s’est produite avec un RNI à 1,13. La cause du résultat sous-thérapeutique n’est pas connue. Un saignement majeur s’est produit pendant le suivi du pharmacien communautaire. Un sujet s’est présenté avec un RNI à 5,21 et une hémorragie digestive associée au syndrome de Mallory-Weiss. Lors du suivi à la clinique spécialisée en anticoagulothérapie, deux hémorragies digestives répondant au critère de saignement majeur se sont produites avec des RNI de 3,3 et 3,52.
Dans cette étude rétrospective de 350 sujets stables dont l’anticoagulation était ajustée par une clinique spécialisée en anticoagulothérapie, le transfert du suivi au pharmacien communautaire n’a pas affecté la qualité du contrôle du RNI. Les principaux indicateurs du suivi, c’est-à-dire le temps dans l’intervalle thérapeutique, le temps dans l’intervalle thérapeutique étendu et la variabilité du RNI sont demeurés similaires dans les deux modèles de suivi.
Des études rétrospectives ont associé un temps dans l’intervalle thérapeutique inférieur à 65 % à une augmentation des événements thromboemboliques25–27. Les temps dans l’intervalle thérapeutique calculés pour les deux modèles de suivi, soit 81,2 % pour le pharmacien communautaire et 80,2 % pour la clinique spécialisée en anticoagulothérapie, démontrent un suivi de qualité et reflètent le faible risque de la population étudiée. Peu d’études ont documenté la qualité du suivi de l’anticoagulothérapie réalisé par le pharmacien communautaire. Une étude québécoise de 222 sujets et une étude canadienne de 19 sujets ont obtenu des temps dans l’intervalle thérapeutique de 77,2 % et 84 % respectivement, ce qui est du même ordre de grandeur que ce qui est mesuré dans notre étude14,15. Aussi, deux groupes de chercheurs de la Nouvelle-Zélande ont calculé le temps dans l’intervalle thérapeutique du suivi effectué par le pharmacien communautaire et ont obtenu des résultats similaires, soit 74 % et 78,6 %16,28.
La variabilité du RNI est un autre marqueur important de la qualité du suivi. Elle est associée de façon indépendante au temps dans l’intervalle thérapeutique, à une augmentation des événements thromboemboliques, des saignements et de la mortalité dans la population atteinte de FA29. Dans la présente étude, la variabilité du RNI est inférieure à 0,14 pour chacun des modèles de suivi. Cette valeur est considérée comme excellente et reflète également la grande stabilité de la population à l’étude21.
Les temps dans l’intervalle thérapeutique pré et post-transfert de la population étudiée sont significativement supérieurs à ceux généralement décrits dans la littérature scientifique30,31. Cet écart s’explique principalement par le devis de l’étude qui ne permettait que l’inclusion de patients préalablement stables. Aussi, la population était à risque embolique et hémorragique plutôt faible (CHA2DS2-VASc moyen à 4,2 et HAS-BLED modifié moyen à 2,1), un facteur également associé à une plus grande stabilité du suivi30,32.
Nous avons regardé le sous-groupe de 72 patients plus difficiles à stabiliser (défini comme ayant un temps dans l’intervalle thérapeutique inférieur à 70 % pour la période prétransfert). Le temps dans l’intervalle thérapeutique moyen post-transfert de ce sous-groupe était statistiquement plus élevé que celui en prétransfert. Cela s’explique par le fait que les patients ont été transférés une fois que l’ajustement de la warfarine était mieux maîtrisé. Ce résultat indique également que la qualité du suivi des patients dont l’ajustement était initialement plus difficile a été préservée à la suite du transfert. Les résultats obtenus dans ce sous-groupe peuvent potentiellement s’appliquer à d’autres patients typiquement plus difficiles à stabiliser (p. ex., CHADS2-VASC élevés, porteurs de valves mécaniques, chirurgies bariatriques)31. Toutefois, d’autres études spécifiques à ces groupes de patients à risque seraient nécessaires pour confirmer les résultats.
Dans la région de Chaudière-Appalaches, le suivi de la majorité des patients hospitalisés à l’HDL est retourné au pharmacien communautaire (sans transition par la clinique spécialisée en anticoagulothérapie de l’hôpital au départ). Le suivi des patients sous warfarine est plus complexe en posthospitalisation et le nombre de RNI extrêmes mesurés y est plus élevé33. Parmi les 55 hospitalisations survenues pendant la période de l’étude, aucune différence n’est apparue entre les deux modèles quant à la qualité du suivi. Aussi, le nombre plus élevé de RNI mesurés dans les 28 jours suivant une hospitalisation (6,2 pour la clinique spécialisée en anticoagulothérapie vs 6,1 pour le pharmacien communautaire) reflète le suivi plus serré réalisé pendant cette période.
Le nombre de saignements et d’événements thromboemboliques est sensiblement le même dans chacun des modèles pendant la période à l’étude. Le faible nombre d’événements limite la puissance de l’étude à détecter une différence significative entre les groupes. De plus, puisque les dossiers des patients ne sont pas centralisés dans tous les hôpitaux du Québec, seules les hospitalisations et consultations à l’urgence de l’HDL et de l’Hôpital Paul-Gilbert ont été analysées. Un total de trois saignements majeurs est survenu, correspondant à une incidence annuelle estimée de 1,2 %, ce qui reflète le faible risque hémorragique de la population à l’étude. L’incidence rapportée dans la littérature scientifique se situe entre 2 et 5 %33.
Cette étude est vulnérable aux biais d’information en raison de son devis rétrospectif (p. ex., données manquantes dans les dossiers). Ce biais est en partie réduit grâce à la centralisation à l’HDL des analyses de laboratoire de tout le territoire de Chaudière-Appalaches. Aussi, l’HDL est le centre de référence régional où la majorité des consultations à l’urgence et des hospitalisations ont lieu. Le biais d’information est aussi diminué grâce aux analyses pré et post-transfert puisque les sujets sont leurs propres comparateurs. Par ailleurs, les indicateurs de la qualité du suivi choisis, soit le temps dans l’intervalle thérapeutique, le temps dans l’intervalle thérapeutique étendu et la variabilité du RNI, ne sont pas parfaits. Le temps dans l’intervalle thérapeutique ne reflète pas uniquement la qualité du suivi et est également influencé par le temps entre les RNI et les comorbidités des sujets24,32,34. Ces éléments ont été pris en considération lors de l’analyse des résultats (exclusion des RNI espacés de plus de six semaines, mesure du temps moyen entre les RNI et exclusion des RNI faits dans les trois premiers mois de traitement)35. D’autres indicateurs de la qualité du suivi sont recommandés dans la littérature, tels que l’utilisation d’un logiciel de suivi de l’anticoagulation, l’enseignement aux patients et le suivi effectué lors des désanticoagulations36. Ceux-ci permettent d’augmenter la qualité de la prise en charge de l’anticoagulation, mais n’ont pas été mesurés dans cette étude37.
Les résultats de l’étude pourraient être généralisables aux autres régions du Québec dans la mesure où plusieurs hôpitaux de la province ont aussi transféré leurs patients sous warfarine aux pharmaciens communautaires en suivant un modèle similaire de prise en charge. Les pharmaciens communautaires ont l’avantage d’être accessibles au public en plus de pouvoir réagir rapidement lorsqu’une interaction médicamenteuse survient dans le dossier des patients ou qu’un changement dans l’état de santé du patient se produit. De plus, cela permet aux pharmaciens communautaires d’exercer un plus grand rôle dans le suivi de leurs patients. Une crainte potentielle relative au transfert des cliniques spécialisées en anticoagulothérapie est la dilution de l’expertise parmi l’ensemble des pharmacies. Nous avons répondu à cette crainte en dispensant une formation théorique complémentaire aux pharmaciens communautaires afin d’optimiser leur habileté à ajuster la warfarine. De plus, les pharmacies faisant le suivi d’un plus petit nombre de patients sous warfarine (moins de 25) ont un temps dans l’intervalle thérapeutique moyen comparable à celui des pharmacies qui en suivent un plus grand volume. Cela indique que le pharmacien, même s’il ne fait pas le suivi d’un grand nombre de patients sous warfarine, est apte à fournir des soins de qualité.
Plusieurs sujets à l’étude auraient pu être traités par un AOD. Les AOD sont reconnus comme étant le traitement de choix en FA et en TEV depuis quelques années. Le grand nombre de patients demeurant sous warfarine dans cette présente étude s’explique par le contexte local. Les politiques de remboursement provinciales au moment de la collecte de données ne prévoyaient pas la couverture des AOD chez les patients déjà stables sous warfarine. Il y a aussi un délai entre les changements dans les lignes directrices et les modifications de pratique38.
Chez les sujets stables, le suivi de la warfarine par le pharmacien communautaire est de qualité comparable à celui d’une clinique spécialisée en anticoagulothérapie et semble tout aussi sécuritaire. Les résultats de cette étude permettent donc de considérer le pharmacien communautaire, en raison de son expertise et de sa disponibilité, comme un acteur de premier plan dans la gestion de l’anticoagulothérapie par la warfarine.
Aucun financement en relation avec le présent article n’a été déclaré par les auteurs.
Tous les auteurs ont rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels.
1. Yu AYX, Malo S, Svenson LW, Wilton SB, Hill MD. Temporal trends in the use and comparative effectiveness of direct oral anticoagulant agents versus warfarin for valvular atrial fibrillation : A Canadian population-based study. J Am Heart Assoc 2017;6:e007129.
2. Maura G, Billionnet C, Drouin J, Weill A, Neumann A, Pariente A. Oral anticoagulation therapy use in patients with atrial fibrillation after the introduction of non-vitamin K antagonist oral anticoagulants: findings from the French healthcare databases, 2011–2016. BMJ Open 2019;9:e026645.
3. Macle L, Cairns J, Leblanc K, Tsang T, Skanes A, Cox JL et coll. 2016 Focused update of the Canadian Cardiovascular Society guidelines for the management of atrial fibrillation. Can J Cardiol 2016;32:1170–85.

4. Kearon C, Akl EA, Ornelas J, Blaivas A, Jimenez D, Bounameaux H et coll. Antithrombotic therapy for VTE disease: CHEST guideline and expert panel report. Chest 2016;149:315–52.

5. Weitz JI, Semchuk W, Turpie AG, Fisher WD, Kong C, Ciaccia A et coll. Trends in prescribing oral anticoagulants in Canada, 2008–2014. Clin Ther 2015;37:2506–14.
6. Björck F, Renlund H, Lip GYH, Wester P, Svensson PJ, Själander A. Outcomes in a warfarin-treated population with atrial fibrillation. JAMA Cardiol 2016:172–180.

7. Canadian Agency for Drugs and Tehnologies in Health. Optimal warfarin management for the prevention of thromboembolic events in patients with atrial fibrillation: a systematic review of the clinical evidence. [en ligne] https://www.cadth.ca/sites/default/files/op0508_warfarin-science-report-1_clinical_e.pdf (site visité le 2 février 2018).
8. You JJ, Singer DE, Howard PA, Lane DA, Eckman MH, Fang MC et coll. Antithrombotic therapy for atrial fibrillation: antithrombotic therapy and prevention of thrombosis, 9th ed: American college of Chest physicians evidence-based clinical practice guidelines. Chest 2012;141(suppl. 2):e531S–75S.


9. Witt DM, Clark NP, Kaatz S, Schnurr T, Ansell JE. Guidance for the practical management of warfarin therapy in the treatment of venous thromboembolism. J Thromb Thrombolysis 2016;41:187–205.


10. Wilson SJ, Wells PS, Kovacs MJ, Lewis GM, Martin J, Burton E et coll. Comparing the quality of oral anticoagulant management by anticoagulation clinics and by family physicians: a randomized controlled trial. CMAJ 2003; 169:293–8.

11. Matchar DB, Samsa GP, Cohen SJ, Oddone EZ, Jurgelski AE. Improving the quality of anticoagulation of patients with atrial fibrillation in managed care organizations: results of the managing anticoagulation services trial. Am J Med 2002;113:42–51.

12. Holden J, Holden K. Comparative effectiveness of general practitioner versus pharmacist dosing of patients requiring anticoagulation in the community. J Clin Pharm Ther 2000;25:49–54.

13. Régie de l’assurance maladie du Québec. Modalités de facturation – Nouvelles activités professionnelles des pharmaciens. [en ligne] https://www.ramq.gouv.qc.ca/SiteCollectionDocuments/professionnels/infolettres/2015/info066-5.pdf (site visité le 10 février 2018).
14. Chartrand M, Lalonde L, Cantin A, Lahaie A, Odobasic B, Tremblay MP et coll. Anticoagulation management services in community pharmacy: Feasibility of implementing a quality improvement programme through a practice-based research network. J Clin Pharm Ther 2018;43:877–87.

15. Wilson JS, MacLellan, E., Meek, W. A pilot study evaluating the feasibility of monitoring oral anticoagulant therapy with point-of-care testing in a community pharmacy. Can J Hospit Pharm 2004;57:158–64.
16. Harrison J, Shaw JP, Harrison JE. Anticoagulation management by community pharmacists in New Zealand: an evaluation of a collaborative model in primary care. Int J Pharm Pract 2015;23:173–81.
17. Collège des médecins du Québec et Ordre des pharmaciens du Québec. Lignes directrices : Anticoagulothérapie en milieu ambulatoire. [en ligne] https://www.opq.org/doc/media/809_38_fr-ca_0_ld_anticoagulotherapie_pharm.pdf (site visité le 15 février 2018).
18. Schulman S, Kearon C. Definition of major bleeding in clinical investigations of antihemostatic medicinal products in non-surgical patients. J Thromb Haemost 2005;3:692–4.

19. Senoo K, Proietti M, Lane DA, Lip GY. Evaluation of the HAS-BLED, ATRIA, and ORBIT bleeding risk scores in patients with atrial fibrillation taking warfarin. Am J Med 2016;129: 600–7.
20. Rosendaal FR, Cannegieter SC, van der Meer FJ, Briet E. A method to determine the optimal intensity of oral anticoagulant therapy. Thromb Haemost 1993;69:236–9.

21. Ibrahim S, Jespersen J, Poller L, European Action on A. The clinical evaluation of international normalized ratio variability and control in conventional oral anticoagulant administration by use of the variance growth rate. J Thromb Haemost 2013;11:1540–6.

22. Hylek EM, Go AS, Chang Y, Jensvold NG, Henault LE, Selby JV et coll. Effect of intensity of oral anticoagulation on stroke severity and mortality in atrial fibrillation. N Engl J Med 2003; 349:1019–26.

23. Glasheen JJ, Fugit RV, Prochazka AV. The risk of overanticoagulation with antibiotic use in outpatients on stable warfarin regimens. J Gen Intern Med 2005;20:653–6.


24. Young S, Bishop L, Twells L, Dillon C, Hawboldt J, O’Shea P. Comparison of pharmacist managed anticoagulation with usual medical care in a family medicine clinic. BMC Fam Pract 2011;12:88.


25. Kaatz S. Determinants and measures of quality in oral anticoagulation therapy. J Thromb Thrombolysis 2008;25:61–6.
26. Heidbuchel H, Verhamme P, Alings M, Antz M, Diener HC, Hacke W et coll. Updated european heart rhythm association practical guide on the use of non-vitamin-K antagonist anticoagulants in patients with non-valvular atrial fibrillation: Executive summary. Eur Heart J 2017;38: 2137–49.
27. Liu S, Li X, Shi Q, Hamilton M, Friend K, Zhao Y et coll. Outcomes associated with warfarin time in therapeutic range among US veterans with nonvalvular atrial fibrillation. Curr Med Res Opin 2018;34:415–21.
28. Harper P, McMichael I, Griffiths D, Harper J, Hill C. The community pharmacy-based anticoagulation management service achieves a consistently high standard of anticoagulant care. N Z Med J 2015;128:31–41.
29. Lind M, Fahlen M, Kosiborod M, Eliasson B, Oden A. Variability of INR and its relationship with mortality, stroke, bleeding and hospitalisations in patients with atrial fibrillation. Thromb Res 2012;129:32–5.
30. Pokorney SD, Simon DN, Thomas L, Fonarow GC, Kowey PR, Chang P et coll. Patients’ time in therapeutic range on warfarin among US patients with atrial fibrillation: Results from ORBIT-AF registry. Am Heart J 2015;170:141–8.
31. Reiffel JA. Time in the therapeutic range for patients taking warfarin in clinical trials: Useful, but also misleading, misused, and overinterpreted. Circulation 2017;135:1475–7.

32. Nelson WW, Choi JC, Vanderpoel J, Damaraju CV, Wildgoose P, Fields LE et coll. Impact of co-morbidities and patient characteristics on international normalized ratio control over time in patients with nonvalvular atrial fibrillation. Am J Cardiol 2013;112:509–12.

33. McAlister FA, Wiebe N, Hemmelgarn BR. Time in therapeutic range and stability over time for warfarin users in clinical practice: a retrospective cohort study using linked routinely collected health data in Alberta, Canada. BMJ Open 2018;8:e016980.


34. Rubboli A, Becattini C, Verheugt FW. Incidence, clinical impact and risk of bleeding during oral anticoagulation therapy. World J Cardiol 2011;3:351–8.


35. Christensen TD. Self-management of oral anticoagulation therapy--methodological and clinical aspects. Dan Med Bull 2011;58:b4284.
36. Cantin A, Lahaie A, Odobasic B, Tremblay MP, Wazzan D, Caron S et coll. Evaluation of a continuous quality improvement program in anticoagulant therapy: Feasibility, satisfaction and perception. Can Pharm J (Ott) 2016;149: 352–61.
37. Nutescu EA, Wittkowsky AK, Burnett A, Merli GJ, Ansell JE, Garcia DA. Delivery of optimized inpatient anticoagulation therapy: consensus statement from the anticoagulation forum. Ann Pharmacother 2013;47:714–24.


38. Huynh, T, Bobrowski A, Montigny M, Ta V, Dion D, Breton R et coll. Adherence to the Canadian Cardiovascular Society atrial fibrillation guidelines by family medicine groups in Quebec: the I-FACILITER project. J Integr Cardiol Open Access 2019;2:1–7.
PHARMACTUEL, Vol. 54, No. 1, 2021