
Rébecca
Larouche
,
Pharm.D., M.Sc.
1,2,3,4,
Émilie
Bachand-Duval
,
B.Pharm., M.Sc.
3,4,
Sylvain
Côté
,
B.Pharm., M.Sc.
3,4,
Paul
Poirier
,
MD, Ph.D., FRCPC, FACC, FAHA, FCCS
5,6
Reçu le 15 mai 2020: Accepté après révision par les pairs le 19 février 2021
Résumé
Objectifs : Décrire les stratégies d’utilisation des antiplaquettaires et des anticoagulants oraux en postangioplastie chez le sous-groupe de patients sous hémodialyse chronique, connu pour fibrillation/flutter auriculaire, à l’Hôtel-Dieu de Québec. Comparer les résultats aux dernières recommandations canadiennes sur l’utilisation des médicaments antithrombotiques et aborder les événements et effets indésirables survenus à la suite de l’intervention.
Méthodologie : Étude descriptive longitudinale avec collecte de données rétrospective de février 2015 à mars 2019. Les données en lien avec les caractéristiques des patients, l’angioplastie coronarienne, les stratégies d’utilisation des antiplaquettaires et des anticoagulants oraux et les événements et effets indésirables survenus ont été colligés.
Résultats : Parmi 40 patients, huit (20 %) étaient sous triple thérapie à la suite de l’intervention. Huit autres sujets (20 %) avaient un régime qui prévoyait la reprise de l’anticoagulant après une durée de double thérapie antiplaquettaire d’un à six mois. Pour les 24 autres patients sans anticoagulation, une double thérapie antiplaquettaire était prévue pour un à trois mois (2 %), un an (48 %) ou à vie (10 %). Huit d’entre eux (33 %) étaient anticoagulés avant l’intervention. Six patients (15 %) ont expérimenté au moins un saignement majeur et neuf (23 %) au moins un saignement cliniquement non majeur. Aucune thrombose de tuteur et aucun événement thromboembolique n’ont été répertoriés.
Conclusion : La moitié des patients de cette étude n’ont pas été anticoagulés à la suite de l’intervention. De plus, seulement la moitié de ceux qui avaient été anticoagulés se sont fait prescrire un régime selon les recommandations actuelles. Choisir la thérapie antiplaquettaire et l’anticoagulothérapie optimale dans cette population est un problème clinique complexe pour lequel nous manquons de données probantes. Les choix thérapeutiques devraient être évalués individuellement.
Mots clés : Angioplastie coronarienne, anticoagulant, antiplaquettaire, fibrillation auriculaire, hémodialyse, insuffisance rénale terminale
Abstract
Objectives : To describe the strategies for using antiplatelet agents and oral anticoagulants postangioplasty in the subgroup of patients on long-term hemodialysis who have known atrial fibrillation/flutter at the Hôtel-Dieu de Québec; to compare the results with the latest Canadian recommendations on the use of antithrombotic drugs and to examine the adverse events and effects that occurred after the procedure.
Methodology : A longitudinal descriptive study with data collected retrospectively from February 2015 to March 2019. Data were collected on the patients’ characteristics, coronary angioplasty, the strategies for using antiplatelet agents and oral anticoagulants, and the adverse events and reactions that occurred.
Results : Of 40 patients, eight (20%) were on triple therapy after the procedure. Another eight subjects (20%) were on a regimen that called for the resumption of the anticoagulant after 1 to 6 months of dual antiplatelet therapy. For the remaining 24 patients without anticoagulation, dual antiplatelet therapy was planned for 1 to 3 months (2%), 1 year (48%) or for life (10%). Eight of them (33%) had been anticoagulated before the procedure. Six patients (15%) experienced at least one major bleed and nine (23%) at least one clinically nonmajor bleed. No stent thrombosis or thromboembolic events were noted.
Conclusion : Half of the patients in this study were not anticoagulated after the procedure. Furthermore, only half of those who had been anticoagulated were prescribed a regimen in accordance with the current recommendations. Choosing the optimal antiplatelet therapy and anticoagulation therapy in this population is a complex clinical challenge for which we lack scientific evidence. The treatment options should be evaluated on an case-by-case basis.
Keywords : Anticoagulant, antiplatelet agent, atrial fibrillation, coronary angioplasty, end-stage renal failure, hemodialysis
L’insuffisance rénale se définit comme l’atteinte progressive et irréversible de la fonction rénale. Il s’agit d’un facteur de risque important pour la mortalité de toutes causes et la maladie cardiovasculaire. La prévalence des patients au stade d’insuffisance rénale terminale (IRT) est en augmentation depuis 1990 en raison de l’amélioration des traitements cardiovasculaires et de la suppléance rénale1. Il existe plusieurs types de thérapie de suppléance rénale : hémodialyse, dialyse péritonéale et greffe rénale2. En ce qui a trait aux patients sous hémodialyse chronique, leur taux de survie à cinq ans est en moyenne de 44,3 % au Québec1. Il a été démontré qu’il s’agit d’une population avec plus de comorbidités, dont principalement les maladies cardiovasculaires et thromboemboliques1.
La fibrillation auriculaire (FA) est l’arythmie la plus fréquente dans la population générale; son incidence double tous les 10 ans après l’âge de 55 ans. Chez les personnes de plus de 60 ans, le tiers des accidents vasculaires cérébraux (AVC) thromboemboliques sont causés par la FA3. Chez les patients avec insuffisance rénale chronique (IRC), la prévalence de la FA augmente proportionnellement avec la diminution de la fonction rénale. En effet, celle-ci est de 3,5 % dans la population générale, passant à 27 % chez les patients en dialyse, ce qui augmente considérablement leur risque thromboembolique4. Afin de prévenir les risques d’AVC et de thromboembolie systémique dans cette population, les recommandations actuelles appuient l’anticoagulation basée sur une évaluation des risques thromboemboliques et hémorragiques4.
Les maladies cardiovasculaires représentent la première cause de morbidité et de mortalité chez les patients hémodialysés5. Il est donc fréquent qu’ils doivent subir une intervention telle qu’une angioplastie coronarienne. De plus, des études ont rapporté une incidence plus élevée de resténose chez les hémodialysés (35 % vs 16 %, p < 0,05)5. Par contre, il s’agit d’une population à plus haut risque de complications hémorragiques que la population générale4.
Les dernières recommandations canadiennes sur l’utilisation de la triple thérapie des antiplaquettaires et des anticoagulants oraux chez les patients qui présentent de la FA et qui doivent subir une angioplastie coronarienne reposent sur des données de faible qualité3. Celles-ci proposent des stratégies (durée plus courte, doses diminuées d’anticoagulants oraux directs [AOD], utilisation d’AOD plutôt que de warfarine, retrait de l’acide acétylsalicylique [AAS]) qui tentent d’équilibrer le plus possible les risques ischémiques, thrombotiques et hémorragiques3. L’Hôtel-Dieu de Québec est un centre tertiaire en cardiologie et quaternaire en néphrologie avec une clinique externe en dialyse. Il est donc fréquent que les cliniciens de ce milieu se retrouvent confrontés à cette problématique clinique. De plus, l’application des recommandations actuelles est limitée, celles-ci étant extrapolées à une population plus à risque de saignements et d’événements thromboemboliques.
Une recherche bibliographique exploratoire a été effectuée dans les différentes ressources de la littérature scientifique, telles que PubmedMD, CochraneMD et EmbaseMD. La conclusion est qu’il existe très peu de documentation sur l’utilisation des traitements antithrombotiques en postangioplastie coronarienne chez les patients hémodialysés qui présentent également de la FA. Les données actuelles se limitent à des études observationnelles et à des opinions d’experts. En effet, les hémodialysés ont été exclus de toutes les études ayant mené aux dernières recommandations canadiennes. Étant donné qu’il y a déjà peu données sur l’anticoagulation en FA chez les patients hémodialysés, il y en a encore moins dans un contexte d’angioplastie coronarienne.
L’objectif principal de l’étude est de décrire les stratégies d’utilisation des médicaments antithrombotiques chez les patients hémodialysés qui ont subi une angioplastie coronarienne et présentent également de la FA. Les objectifs secondaires sont les suivants : 1) comparer les stratégies utilisées en fonction des recommandations actuelles sur l’utilisation des médicaments antithrombotiques et des contre-indications s’appliquant à l’IRC terminale sous hémodialyse; et 2) décrire les effets indésirables et les complications (événements thromboemboliques, saignements de tous types, hospitalisations) survenus à la suite de l’intervention coronarienne en fonction du régime utilisé.
Il s’agit d’une étude descriptive de population longitudinale avec une collecte de données rétrospective qui a été effectuée du 6 mai 2019 au 7 juin 2019. Cette étude a été approuvée par le comité d’éthique de la recherche du Centre hospitalier universitaire de Québec. Avec l’aide des archivistes, nous avons sélectionné les patients par série consécutive. Les patients sous hémodialyse chronique qui avaient subi une intervention percutanée coronarienne à l’Hôtel-Dieu de Québec du Centre hospitalier universitaire de Québec – Université Laval entre février 2015 et mars 2019 et qui présentaient également de la FA ont tous été inclus, même s’ils avaient une indication d’anticoagulation supplémentaire ou n’étaient pas anticoagulés avant l’intervention. Les patients greffés, qui avaient été dialysés temporairement (pathologie aiguë) ou qui étaient en dialyse péritonéale, ont été exclus. Ce statut de suppléance rénale a été évalué au moment de l’intervention percutanée. Ceux qui présentaient de la FA longtemps après l’intervention ont également été exclus. Chaque dossier a été analysé à l’aide du Dossier patient électronique (DPE), du logiciel de pharmacie GespharRxMD, du logiciel d’anticoagulothérapie DAWNMD et du dossier parallèle de dialyse. Les données en lien avec les caractéristiques des patients et l’angioplastie coronarienne, les stratégies d’utilisation des antiplaquettaires et des anticoagulants oraux, et les événements et effets indésirables survenus ont été colligés. Des statistiques descriptives ont été effectuées. Les variables qualitatives sont exprimées sous forme de proportions et les variables quantitatives, sous forme de mesures de tendance centrale et de dispersion. La durée de suivi pour la collecte des événements a été établie à partir de la date de l’intervention jusqu’à la période de collecte.
Les dossiers retenus par le service des archives ont été révisés de façon rétrospective de la plus récente intervention percutanée à la plus ancienne. Les patients ont été identifiés au fur et à mesure jusqu’à ce que l’on constitue un échantillon de 40 d’entre eux répondant aux critères d’inclusion et d’exclusion établis. Ainsi, 71 dossiers ont été révisés et 21 patients ont été exclus parce qu’ils avaient présenté de la FA quelque temps après l’intervention percutanée coronarienne, qu’ils avaient été dialysés temporairement ou qu’ils étaient greffés. Dix patients n’ont pas été retenus puisque l’intervention datait de 2014. La procédure de sélection des sujets est présentée à l’annexe.
L’échantillon étudié comportait 65 % d’hommes. Les patients étaient tous hypertendus, une grande proportion était diabétique (78 %) et l’insuffisance cardiaque était présente chez 30 % d’entre eux. La majorité était sous inhibiteur de la pompe à protons (95 %). On note un score de risque annuel d’AVC CHADS2 (insuffisance cardiaque, hypertension, âge de 75 ans et plus et diabète valent un point, antécédent d’ischémie cérébrale transitoire ou d’AVC valent deux points) moyen de 3 (1–6) et un score de risque annuel hémorragique HASBLED (hypertension mal maîtrisée, insuffisance rénale ou hépatique, antécédent d’AVC, antécédent de saignement majeur ou prédisposition à un saignement, RNI labile, âge de 65 ans et plus, consommation d’alcool et consommation de médicaments prédisposant aux saignements valent un point) de 4,5 (3–6). Ce qui se traduit par un risque annuel d’AVC de 5,9 % et d’événement hémorragique de 12,5 %. Au total, 35 % des patients présentaient un antécédent d’ischémie cérébrale transitoire ou d’AVC, alors que 30 % avaient déjà présenté un saignement majeur. Le clopidogrel est l’antiplaquettaire de type P2Y12 le plus utilisé et la warfarine est l’anticoagulant le plus fréquemment employé. Les caractéristiques complètes des patients sont présentées au tableau I.
Tableau I
Caractéristiques des patients inclus dans l’étude

La majorité des patients ont subi leur intervention percutanée dans un contexte d’infarctus du myocarde sans élévation du segment ST (40 %) ou d’angine instable (37,5 %). On dénombre ainsi 33 patients sur 40 qui ont subi un syndrome coronarien aigu. Les caractéristiques des interventions percutanées sont présentées au tableau II.
Tableau II
Caractéristiques de l’angioplastie coronariennea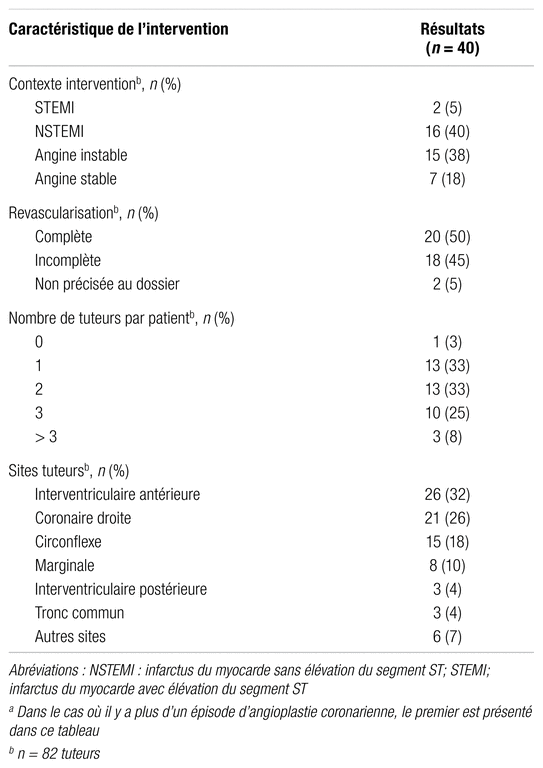
Tel que présenté dans la figure 2, près de la moitié des patients ont reçu une double thérapie antiplaquettaire (DTAP) pour un an, suivie d’un antiplaquettaire seul. De plus, 40 % des patients se sont vu prescrire un régime incluant un ACO (régime IV et V). Parmi ceux-ci, 20 % ont été sous triple thérapie pendant une période suivant leur intervention (régime V). On note également que 50 % des patients sous triple thérapie avaient une indication qui rendait impossible la suspension de l’anticoagulant oral, telle que remplacement de valve aortique, embolie pulmonaire récente et thrombose veineuse profonde récente. De plus, une autre proportion de ces patients (38 %) avait un ou deux facteurs de risque supplémentaires (AVC, CHADS 4, néoplasie,etc.). Les stratégies d’utilisation des médicaments antithrombotiques sont présentées aux figures 1 et 2.
|
|
||
|
Figure 1
Description des régimes de médicaments antithrombotiques prescrits à la suite d’une angioplastie coronarienne
|
||
|
|
||
|
Figure 2 Nombre de patients et pourcentage selon le régime de médicaments antithrombotiques prescrits |
||
Presque la moitié des patients étaient décédés au moment de la collecte des données. Seulement un patient a subi un AVC de type hémorragique, et aucun AVC ischémique n’a été répertorié entre le jour de l’intervention et le moment de la collecte ou du décès. En tout, 17 patients ont subi au moins un événement cardiaque (42,5 %), majoritairement un syndrome coronarien aigu.
Six patients ont présenté au moins un saignement majeur; deux d’entre eux en ont eu deux. Ceux-ci étaient des saignements d’origine gastro-intestinale (hémorragie digestive haute, hémorragie digestive basse, ischémie et perforation colique) et intracrânienne, ou associés à des hématomes. Pour ce qui est des médicaments antithrombotiques pris au moment de l’événement, un patient était sous triple thérapie, trois sous DTAP et deux sous association antiplaquettaire et anticoagulant. Un seul saignement fatal a été rapporté, soit un saignement intracrânien secondaire à un AVC hémorragique. Le temps médian entre le jour de l’intervention et l’événement hémorragique est de 45 jours, avec des valeurs allant de 0 à 1 080 jours (voir annexe).
Neuf patients ont subi au moins un saignement non majeur cliniquement significatif; deux d’entre eux en ont eu deux (voir annexe). L’origine de ces saignements était principalement gastro-intestinale (rectorragies, hémoptysie, méléna, adhérences sur subocclusion, ulcère duodénal), vaginale et cutanée (plaie, ecchymoses, trauma). En ce qui a trait aux médicaments antithrombotiques pris au moment de l’événement, quatre patients étaient sous triple thérapie, un sous association antiplaquettaire et anticoagulant et quatre sous DTAP. Le temps médian entre le jour de l’intervention et l’événement hémorragique est de 60 jours, avec des valeurs allant de 0 à 720 jours (voir annexe).
À la suite de l’intervention percutanée initiale, on a noté au moins un retour en hémodynamie pour sept patients, dont cinq pour lesquels une pose de tuteurs était nécessaire. Parmi ceux-ci, on comptait quatre cas de resténose. Deux patients ont également été adressés pour un pontage aortocoronarien (PAC). Aucun cas de thrombose de tuteur n’a été répertorié (annexe).
Les patients ayant un régime avec anticoagulant à la suite de l’intervention coronarienne (16/40) se sont fait prescrire soit une triple thérapie durant un à trois mois, suivie d’une association antiplaquettaire et anticoagulant pour un an et de l’anticoagulant seul par la suite (régime V), soit une DTAP pour un à trois mois, suivie d’un antiplaquettaire et de l’anticoagulant pour un an et de l’anticoagulant seul par la suite (régime IV). Ces deux régimes sont représentés à parts égales (8/16 pour chacun). Ainsi, nous avons la moitié des patients sous anticoagulant qui se sont fait prescrire un régime suivant les recommandations actuelles. Pour ce qui est de l’autre moitié, la conduite privilégiée peut s’expliquer par la détermination du risque hémorragique supérieur au risque thromboembolique et/ou au risque coronarien, justifiant une DTAP pour une durée supérieure.
Jusqu’à présent, à notre connaissance, aucune étude ne s’est penchée sur l’utilisation des antiplaquettaires et des anticoagulants oraux à la suite d’une angioplastie coronarienne dans la population hémodialysée chronique et connue pour FA. Des auteurs ont examiné l’impact de l’IRC sur les saignements majeurs et la mortalité de toutes causes chez 166 patients anticoagulés (104 pour FA) ayant subi une intervention coronarienne percutanée7. Ils en sont venus à la conclusion que l’IRC était un facteur de risque indépendant de saignement majeur (Rapport de risque [RR] = 3,44; p = 0,004) et de mortalité (RR = 3,5; p = 0,003). À leur avis, il serait donc préférable d’éviter la triple thérapie chez ces patients. Si celle-ci est vraiment nécessaire, ils recommandent d’en limiter le plus possible la durée et de favoriser l’association de clopidogrel et d’un anticogulant. Par contre, il ne s’agissait pas d’une population atteinte d’insuffisance rénale terminale sous suppléance rénale. En effet, la fonction rénale moyenne des patients admis dans l’étude était de 48 mL/min7.
Les recommandations de la Société canadienne de cardiologie émises en 2018 ont intégré les nouvelles données probantes depuis 2013 sur l’optimisation de l’utilisation des antiplaquettaires dans diverses situations3. Dans le sous-groupe de patients qui présentent de la FA et dont l’état nécessite une angioplastie coronarienne, en l’absence de documentation claire permettant de déterminer le meilleur régime thérapeutique pour prévenir la thrombose de tuteur ainsi que l’AVC thromboembolique, un régime composé d’une double thérapie antiplaquettaire et d’un anticoagulant est communément utilisé. Des analyses issues des principales études menées avec les AOD en FA (RELY, ROCKET AF, ARISTOTLE et ENGAGE-TIMI) révèlent une augmentation de 30 à 60 % des saignements chez les patients qui ont reçu un AOD et un antiplaquettaire8. Une étude danoise a également permis d’observer plus de saignements majeurs et fatals avec l’association AAS et warfarine. De plus, la triple thérapie AAS, warfarine et clopidogrel présentait trois fois plus de risques de saignements que la warfarine seule8. La Société canadienne de cardiologie propose des stratégies d’utilisation en lien avec le nombre de molécules, leur dose et leur durée d’emploi, dans le but d’aider les cliniciens à atteindre l’équilibre des risques ischémiques et hémorragiques du patient avec FA qui doivent subir une angioplastie coronarienne3.
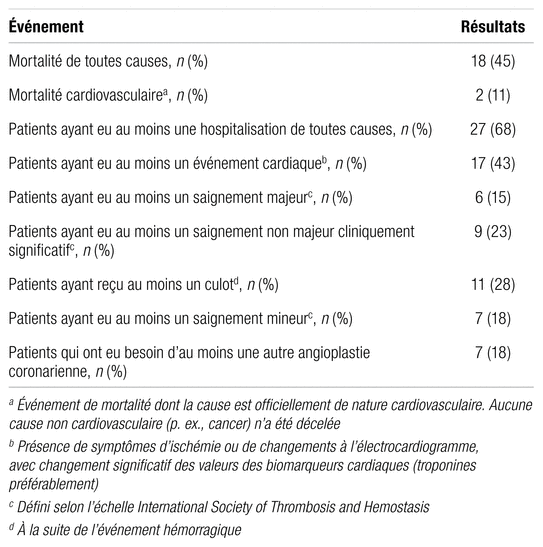
Tableau III
Types d’événements survenus à la suite de l’angioplastie coronarienne
L’étude AUGUSTUS a tenté de déterminer le traitement antithrombotique optimal chez les patients avec FA qui souffrent d’un infarctus du myocarde ou chez lesquels une angioplastie coronarienne est programmée10. Celle-ci nous révèle que les patients traités par un inhibiteur P2Y12 et l’apixaban avaient moins de saignements et qu’il n’y avait pas de différence significative avec les régimes warfarine en ce qui concerne les événements ischémiques. De plus, la triple thérapie avec un anticoagulant et de l’AAS augmente les risques de saignements sans diminuer les risques thrombotiques. Par contre, les patients avec IRC terminale ont été exclus de cette étude10.
L’étude ENTRUST AF-PCI a évalué l’association édoxaban et clopidogrel, comparativement à une triple thérapie par warfarine chez les patients avec FA qui ont subi une angioplastie coronarienne. Celle-ci a alors démontré que l’association édoxaban et clopidogrel est non inférieure à une triple thérapie à base de warfarine en ce qui a trait aux événements ischémiques et hémorragiques38. Il s’agit de la première étude où un AOD ne démontre pas de supériorité par rapport à la warfarine pour les saignements. Les patients avec IRC terminale ont été exclus de l’étude, la dose d’édoxaban a été réduite à 30 mg chez les patients avec une fonction rénale entre 15 et 50 mL/min.
Comme mentionné, il n’existe pas de documentation sur l’utilisation des médicaments antithrombotiques dans la population à l’étude dans le cadre de ce projet, soit la population hémodialysée. Il est difficile d’extrapoler et d’appliquer les données dont nous disposons actuellement à ces sujets, et ce, pour plusieurs raisons. Premièrement, les patients hémodialysés ont un risque coronarien et thromboembolique plus grand. En effet, on retrouve chez ces personnes des niveaux plus élevés de plusieurs facteurs procoagulants (thrombine-antithrombine III, ibrinopeptide A, D-dimère, facteur de Von Willebrand, fibrinogène, activateur du plasminogène, etc.) et un faible niveau de facteurs contribuant à limiter le processus de coagulation (antithrombine III). Il s’agit également d’une population dans laquelle on retrouve plus de dommages endothéliaux et d’athérosclérose. De plus, les patients hémodialysés ont une fonction endothéliale altérée par la dialyse11. Puisque les patients inclus dans ce projet présentent également de la FA, cela ajoute aux facteurs de risque thromboembolique.
Deuxièmement, ces patients sont également à très haut risque de saignements. En effet, on retrouve des interactions anormales au niveau de leurs vaisseaux sanguins ainsi que plusieurs facteurs contribuant à l’anomalie d’adhésion et d’agrégation plaquettaire (hormone parathyroïde élevée, cytokines inflammatoires, production de globules rouges réduite, toxines produites par l’ischémie, etc.). En plus des problèmes hémostatiques, l’anticoagulation intermittente du circuit de dialyse et la pharmacocinétique altérée des médicaments antithrombotiques contribuent également à l’augmentation du risque de saignements. Sans oublier la tendance chez ces patients à subir plus souvent des interventions médicales susceptibles de se compliquer (chirurgies, angioplasties, etc.)12.
Troisièmement, quand vient le temps d’évaluer les risques thromboemboliques et hémorragiques chez ces patients, il n’y a pas de score validé pour eux. En effet, la plupart des scores existants ne tiennent pas compte de la fonction rénale dans son entièreté en tant que facteur de risque de saignements. De plus, plusieurs autres facteurs de risque de saignements présents chez les patients avec IRC ont été définis à partir des valeurs de patients avec une fonction rénale normale. Pour l’instant, le score HAS-BLED serait celui qui aurait la meilleure valeur prédictive pour les patients avec IRC13. L’organisme KDIGO a émis des recommandations quant au contenu que devrait avoir un score bien adapté aux patients avec IRC. Celles-ci reposent principalement sur l’ajout de la fonction rénale et de l’hémoglobine dans le calcul du pointage et sur la diminution de la valeur pour l’HTA à 130/80 mmHg13. À la lumière de tout ceci, nous devons garder en tête que ces patients sont à plus haut risque de faire des événements coronariens, cardioemboliques et hémorragiques que la population générale. Toutefois, nous n’avons pas d’outil valide pour comparer ces risques et déterminer une conduite optimale pour l’utilisation des antiplaquettaires et de l’anticoagulothérapie orale.
Ainsi, si on compare les résultats de cette étude avec les recommandations actuelles, on remarque une tendance parallèle à celles-ci, avec des déviations justifiées. Ce choix de stratégie pourrait s’apparenter à la recommandation des lignes directrices canadiennes de réduire la dose de l’anticoagulant oral (rivaroxaban et dabigatran). Par contre, puisque ces molécules sont à ce jour contre-indiquées chez les patients en insuffisance rénale terminale, les cliniciens ont dû ajuster leur régime thérapeutique en conséquence. Presque la totalité de nos patients était sous warfarine. La réduction de la cible à 2,0–2,5 a été citée à quelques reprises dans les rapports des cardiologues pour les patients qui ont bénéficié du régime V; ce qui pourrait être interprété comme étant une réduction de dose. On remarque aussi que la majorité des patients sous triple thérapie avait une indication supplémentaire d’anticoagulation (valve mécanique, embolie pulmonaire, thrombose veineuse profonde, etc.). De plus, aucun patient n’a reçu une triple thérapie pour une période inférieure à un mois.
Il est à noter qu’au moment de la collecte de données, il y avait un patient sous apixaban et quatre autres pour lesquels on avait opté pour cette molécule à la suite de l’intervention. Cette approche fait suite à une publication d’auteurs qui ont rassemblé les données d’utilisation de l’apixaban chez les patients avec IRT et les hémodialysés atteints de FA aux États-Unis ( n = 25 523)14. Les auteurs ont rapporté moins de saignements majeurs (30 %) et une efficacité similaire chez les utilisateurs d’apixaban en comparaison avec la warfarine. De plus, il n’y avait aucune différence entre les deux dosages (2,5 et 5 mg deux fois par jour) pour les saignements majeurs gastro-intestinaux et intracrâniens. Par contre, ils ont observé une incidence plus faible d’AVC ischémique, d’embolie systémique et de décès avec la dose complète (5 mg deux fois par jour); ce qui laisse penser que le fait d’être en hémodialyse ne serait pas un facteur suffisant pour réduire la dose14. Notons aussi que, dans cette étude, l’incidence de saignements était tout de même plus élevée dans les deux groupes que dans l’étude ARISTOTLE14. Contrairement aux résultats de cet article, certains experts suggèrent d’utiliser d’emblée la dose réduite chez les hémodialysés. En effet, des données pharmacocinétiques récentes sont en faveur d’une concentration suprathérapeutique avec une dose de 5 mg deux fois par jour, ce qui va à contresens de ce que l’article semble indiquer14–16. Une méta-analyse récente a évalué l’anticoagulation orale chez les patients hémodialysés. Celle-ci a révélé que l’anticoagulation orale ne diminuait pas significativement le risque d’AVC ou d’événement thromboembolique. De plus, la warfarine, le dabigatran et le rivaroxaban étaient associés à une augmentation significative du risque de saignements majeurs, contrairement à l’apixaban. On a également fait état d’une diminution significative de la mortalité chez les patients sous apixaban 5 mg deux fois par jour17. La Food and Drug Administration américaine a approuvé l’utilisation de cette molécule à la dose de 5 mg deux fois par jour chez les patients hémodialysés18. Elle représente maintenant le quart des prescriptions d’anticoagulants oraux chez les hémodialysés aux États-Unis. L’American Heart Association a récemment publié une mise à jour des recommandations sur la gestion des patients atteints de FA. Dans celles-ci, elle positionne maintenant l’apixaban comme une option raisonnable pour l’anticoagulation chez les patients sous hémodialyse18. Cette évaluation favorable repose toutefois sur des données de faible qualité (une étude de dose unique avec 10 patients), et l’apixaban demeure contre-indiqué chez les patients avec une fonction rénale inférieure à 25 mL/min.
L’étude RENAL-AF a évalué l’apixaban comparativement à la warfarine chez les patients hémodialysés. L’étude a été interrompue en raison d’un faible taux d’inclusion et d’un faible échantillonnage. Les résultats n’ont pas montré de différence significative quant aux saignements majeurs ou cliniquement non majeurs (31,5 % groupe apixaban vs 25,5 % groupe warfarine). Par ailleurs, le taux d’AVC n’est pas statistiquement différent (2,4 % vs 2,8 %). Aucune différence quant à la mortalité n’a été détectée. De plus, le temps dans l’intervalle thérapeutique des patients sous warfarine était de 44 %, ce qui témoigne de la difficulté à obtenir une anticoagulation optimale et sécuritaire avec la warfarine chez ces patients18.
Concernant le dabigatran et le rivaroxaban, quelques études ont évalué ces molécules dans la population hémodialysée17,19–21. Les auteurs suggèrent d’être prudent, car on a remarqué une augmentation de l’utilisation de ces deux molécules chez ces patients malgré les avis de précaution de la Food and Drug Administration. Les résultats indiquent une augmentation de la morbidité et de la mortalité due à des saignements en comparaison avec la warfarine22.
Pour ce qui est de la warfarine, aucune étude comparative à répartition aléatoire n’a non plus évalué cette molécule chez les patients hémodialysés avec FA. Étant donné son élimination hépatique, sa liaison aux protéines plasmatiques et le suivi des niveaux d’anticoagulation, la warfarine était l’anticogugulant le plus utilisé et le seul à être recommandé dans cette population26. Par contre, les dernières données d’utilisation dans cette population laissent entrevoir un manque d’efficacité et une augmentation potentielle du risque d’AVC ischémique16,17,21,25–27. De plus, elles ont démontré une incidence plus élevée de saignements (intracrâniens, AVC hémorragiques, etc.)26. Le suivi du rapport normalisé international est également plus difficile, car ces patients sont beaucoup moins souvent dans l’intervalle thérapeutique26. D’ailleurs, le temps dans l’intervalle thérapeutique moyen des patients sous warfarine dans cette étude était de 63 % (30–96 %), ce qui est considéré comme labile23. On observe aussi plus de calciphylaxie chez ces patients, car la warfarine interfère avec la vitamine K, essentielle à l’activation de l’enzyme carboxylase glutamine Y. Cette enzyme est nécessaire à l’activation de la protéine G1a qui inhibe la calcification vasculaire26. Cela pourrait peut-être alors expliquer l’incidence augmentée d’AVC chez les patients sous warfarine26. La calcification peut aussi exposer le patient à de graves infections et à un plus haut risque de mortalité. Une revue rétrospective ayant évalué l’impact du remplacement de la warfarine par l’apixaban chez 20 hémodialysés qui présentaient de la calciphylaxie a permis de noter une amélioration clinique des lésions et de la douleur associée, en plus d’une efficacité antithrombotique similaire28. Des données ont également démontré que la warfarine peut induire des saignements microglomérulaires induisant une obstruction tubulaire et des maladies rénales26. Ce phénomène est particulièrement important dans la population hémodialysée puisque le maintien d’une certaine fonction rénale résiduelle peut conférer des bénéfices quant à la mortalité28. Les récentes méta-analyses des données observationnelles réalisées avec les anticoagulants oraux ont conclu qu’il n’y avait pas d’association significative entre la warfarine et la réduction des AVC cardio-emboliques, mais elles ont établi une différence significative entre la warfarine et l’augmentation de l’incidence des saignements. En lien avec ceux-ci, on observait alors 20 événements pour 100 patients avec apixaban, 23 à 36 avec la warfarine, 68 avec le rivaroxaban et 83 avec le dabigatran6,15,23,25.
Les résultats de notre étude révèlent que 60 % des patients n’étaient pas anticoagulés malgré la présence de FA. Bien que chaque patient soit différent, cela démontre tout de même une certaine tendance chez les cliniciens de L’Hôtel-Dieu de Québec à évaluer que les risques hémorragiques sont supérieurs aux risques emboliques. De plus, parmi les patients anticoagulés, une grande proportion (62,5 %) avait une indication et/ou des facteurs de risque thromboemboliques supplémentaires par rapport à la FA (valve mécanique, embolie pulmonaire récidivante, thrombose veineuse profonde, thrombose de fistule artério-veineuse, AVC, néoplasie, thrombus dans le ventricule gauche).
Pour ce qui est des événements survenus pendant l’étude, aucun AVC n’a été observé, ce qui est rassurant quand on sait que 60 % des patients n’étaient pas anticoagulés. De plus, aucune thrombose de tuteur n’a été relevée. Cela démontre que nos patients ont été bien couverts par les traitements antiplaquettaires. Plus de la moitié des sujets a reçu une DTAP pour minimalement un an. On remarque qu’il y a autant de saignements majeurs chez les patients avec ou sans anticoagulant oral. Par contre, on compte une plus grande proportion de saignements non majeurs mais cliniquement significatifs chez les patients avec anticoagulant oral. On remarque que, dans la majorité des cas, ces événements hémorragiques ont entraîné une modification du régime antithrombotique, soit principalement le retrait ou la diminution de la dose de l’anticoagulant oral ou la cessation d’un antiplaquettaire.
Avec le suivi des événements, on compte maintenant 65 % des patients qui ne sont plus anticoagulés. On voit alors une certaine tendance à éviter l’anticoagulation le plus possible. De plus, si celle-ci s’avère nécessaire (risque thromboembolique élevé, autre indication d’anticoagulation, etc.), la warfarine ne serait peut-être pas l’option idéale pour les raisons déjà discutées. Au début de la collecte, il y avait 15 patients sous warfarine et un patient sous apixaban. À la fin, on a relevé cinq patients sur 16 (31 %) sous apixaban et non sous warfarine. Par contre, des études supplémentaires sont nécessaires avant de statuer sur l’utilisation de l’apixaban dans cette population. Bien sûr, il reste encore des problèmes cliniques (p. ex., valve mécanique, thrombus apical) pour lesquels la warfarine est le seul anticoagulant oral qui puisse être utilisé.
Cette étude comporte plusieurs limites. Tout d’abord, la taille réduite de l’échantillon ne permet pas de généraliser les résultats. De plus, le fait d’inclure des patients d’un seul milieu peut avoir contribué à un biais de sélection. Un biais d’entrevue est aussi possible puisque les informations ont été colligées dans les dossiers antérieurs et qu’elles étaient issues des consultations de différents intervenants. Un biais d’information est également probable vu les données parfois manquantes dans les dossiers et la possibilité que les patients aient subi un épisode hémorragique ou ischémique dans un autre centre. Les outils des professionnels et leurs méthodes d’évaluation ont également pu varier. Nous avons aussi dû remonter jusqu’en 2015 pour avoir suffisamment de patients, ce qui peut avoir influé sur les résultats, car les pratiques étaient différentes et les recommandations actuelles n’étaient pas encore en vigueur. En continuité, la majorité des patients avec une triple thérapie avait une indication d’anticoagulation supplémentaire pour la FA, ce qui donne moins de générabilité à ces résultats pour une population de patients hémodialysés avec FA seulement. Enfin, puisqu’il s’agit d’une étude de nature observationnelle, il n’est pas possible d’établir un lien causal entre les événements survenus et les types de régimes utilisés.
Pour les points forts de l’étude, mentionnons la méthode d’échantillonnage par série consécutive qui a permis de minimiser le biais de sélection. Le fait d’avoir recueilli les données dans les dossiers a également limité la possibilité d’un biais de rappel. L’utilisation du même outil de cueillette des données a aussi favorisé une procédure de collecte unifiée et, par conséquent, l’évitement d’un biais d’informations. Enfin, nous sommes d’avis que les résultats de cette étude pourront être utilisés pour la prise en charge des patients en postangioplastie coronarienne qui sont hémodialysés et présentent de la FA. Il serait donc adéquat que les cliniciens qui traitent une population similaire à celle de l’étude les appliquent.
En conclusion, le choix de la stratégie d’utilisation des antiplaquettaires et des anticoagulants oraux chez les patients hémodialysés qui ont subi une intervention coronarienne percutanée et présentent également de la FA est une problématique fréquente en clinique, pour laquelle nous manquons considérablement de données probantes. C’est une situation clinique très complexe qui demande une analyse rigoureuse du risque coronarien, embolique et hémorragique du patient. Plus de la moitié des sujets de cette étude n’était pas anticoagulée et a reçu une DTAP pour une durée d’un mois à un an. De plus, ceux qui étaient anticoagulés avaient, la plupart du temps, une indication et/ou des facteurs de risque thromboembolique supplémentaires. Lorsque le régime comprenait un anticoagulant oral, la moitié des patients a eu une cessation temporaire de cet anticoagulant durant la période de DTAP. Aucun événement thromboembolique ni de thrombose de tuteur n’a été relevé. Par contre, 38 % des patients ont expérimenté au moins un saignement majeur ou non majeur, mais cliniquement significatif. Les événements hémorragiques survenus ont, la plupart du temps, engendré des modifications des régimes antithrombotiques. On établit donc à 50 % le pourcentage de patients qui se sont fait prescrire un régime selon les recommandations. Pour ce qui est des autres patients, les divergences avec les recommandations peuvent s’expliquer par leur risque hémorragique et/ou thrombotique plus élevé. Enfin, il serait intéressant de mener une étude dans plusieurs centres hospitaliers qui prennent en charge ce type de population afin d’avoir une meilleure généralisation des résultats et peut-être même d’en faire une étude prospective. Actuellement, deux autres études sont toujours en recrutement : AXADIA et AVK-DIAL. L’étude AXADIA évaluera l’apixaban comparativement à la warfarine chez les patients avec FA atteints d’IRT et/ou hémodialysés. Quant à l’étude AVK-DIA, elle comparera la warfarine à l’absence d’anticoagulation chez les patients hémodialysés.
Cet article comporte une annexe; elle est disponible sur le site de Pharmactuel (www.pharmactuel.com).
Aucun financement en relation avec le présent article n’a été déclaré par les auteurs.
Tous les auteurs ont rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts en relation avec le présent article.
1. Institut national d’excellence en santé et en services sociaux. Analyse d’impact budgétaire d’une augmentation de la transplantation rénale au Québec. 2012. [en ligne] https://www.inesss.qc.ca/fileadmin/doc/INESSS/Rapports/EtudeEconomique/INESSS_Analyse_impact_budgetaire_transplantation_renale.pdf (site visité le 19 février 2021).
2. Andrassy KM. Comments on « KDIGO 2012 Clinical practice guideline for the evaluation and management of chronic kidney disease ». Kidney Int 2013;84:622–3.
3. Mehta SR, Bainey KR, Cantor WJ, Lordkipanidze M, Marquis-Gravel G, Robinson SD et al. 2018 Canadian Cardiovascular Society/Canadian Association of Interventional Cardiology focused update of the guidelines for the use of antiplatelet therapy. Can J Cardiol 2018;34:214–33.
4. McCullough PA, Ball T, Cox KM, Assar MD. Use of oral anticoagulation in the management of atrial fibrillation in patients with ESRD: Pro. Clin J Am Soc Nephrol 2016;11:2079–84.
5. Azar RR, Prpic R, Ho KK, Kiernan FJ, Shubrooks SJ, Jr., Baim DS et al. Impact of end-stage renal disease on clinical and angiographic outcomes after coronary stenting. Am J Cardiol 2000;86:485–9.
6. Bansal N. Use of oral anticoagulation for patients with ESRD on hemodialysis with atrial fibrillation: Verdict 1. Clin J Am Soc Nephrol 2016;11:2093–4.
7. Manzano-Fernandez S, Marin F, Pastor-Perez FJ, Caro C, Cambronero F, Lacunza J et al. Impact of chronic kidney disease on major bleeding complications and mortality in patients with indication for oral anticoagulation undergoing coronary stenting. Chest 2009;135:983–90.
8. Hansen ML, Sorensen R, Clausen MT, Fog-Petersen ML, Raunso J, Gadsboll N et al. Risk of bleeding with single, dual, or triple therapy with warfarin, aspirin, and clopidogrel in patients with atrial fibrillation. Arch Intern Med 2010;170:1433–41.
9. Cavallari I, Patti G. Meta-Analysis comparing the safety and dfficacy of dual versus triple antithrombotic therapy in patients with atrial fibrillation undergoing percutaneous coronary intervention. Am J Cardiol 2018;121:718–24.
10. Lopes RD, Heizer G, Aronson R, Vora AN, Massaro T, Mehran R et al. Antithrombotic therapy after acute coronary syndrome or PCI in atrial fibrillation. N Engl J Med 2019;380: 1509–24.
11. Massimiliano Migliori VC, Alessia Scatena, Vincenzo Panichi. Antiplatelets agents in hemodialysis. Ital J Nephrol 2016;11.
12. Burlacu A, Genovesi S, Goldsmith D, Rossignol P, Ortiz A, Kalra PA et al. Bleeding in advanced CKD patients on antithrombotic medication – A critical appraisal. Pharmacol Res 2018;129: 535–43.
13. Ravera M, Bussalino E, Paoletti E, Bellasi A, Di Lullo L, Fusaro M. Haemorragic and thromboembolic risk in CKD patients with non valvular atrial fibrillation: Do we need a novel risk score calculator? Int J Cardiol 2019;274:179–85.
14. Siontis KC, Zhang X, Eckard A, Bhave N, Schaubel DE, He K et al. Outcomes associated with apixaban use in patients with end-stage kidney disease and atrial fibrillation in the United States. Circulation 2018;138: 1519–29.
15. Reed D, Palkimas S, Hockman R, Abraham S, Le T, Maitland H. Safety and effectiveness of apixaban compared to warfarin in dialysis patients. Res Pract Thromb Haemost 2018; 2:291–8.
16. Schafer JH, Casey AL, Dupre KA, Staubes BA. Safety and efficacy of apixaban versus warfarin in patients with advanced chronic kidney disease. Ann Pharmacother 2018;52:1078–84.
17. Kuno T, Takagi H, Ando T, Sugiyama T, Miyashita S, Valentin N et al. Oral anticoagulation for patients with atrial fibrillation on long-term hemodialysis. J Am Coll Cardio 2020;75: 273–85.
18. Writing Group M, January CT, Wann LS, Calkins H, Chen LY, Cigarroa JE et al. 2019 AHA/ACC/HRS focused update of the 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: A report of the American College of Cardiology/American Heart Association Task Force on clinical practice guidelines and the Heart Rhythm Society. Heart Rhythm 2019;16:e66–e93.
19. Dans AL, Connolly SJ, Wallentin L, Yang S, Nakamya J, Brueckmann M et al. Concomitant use of antiplatelet therapy with dabigatran or warfarin in the Randomized Evaluation of Long-Term Anticoagulation Therapy (RE-LY) trial. Circulation 2013;127: 634–40.
20. Muster H, Alcorn H, Jr. Rivaroxaban in chronic hemodialysis patients. Am J Nephrol 2016; 43:227–8.
21. Di Lullo L, Tripepi G, Ronco C, De Pascalis A, Barbera V, Granata A et al. Safety and effectiveness of rivaroxaban and warfarin in moderate-to-advanced CKD: real world data. J Nephrol 2018;31:751–6.
22. Chan KE, Edelman ER, Wenger JB, Thadhani RI, Maddux FW. Dabigatran and rivaroxaban use in atrial fibrillation patients on hemodialysis. Circulation 2015;131:972–9.
23. Chan KE, Giugliano RP, Patel MR, Abramson S, Jardine M, Zhao S et al. Nonvitamin K anticoagulant agents in patients with advanced chronic kidney disease or on dialysis with AF. J Am Coll Cardiol 2016;67:2888–99.
24. Bowie M, Valencia V, Perez-Alvarez I, Tran MH. Safety analysis of apixaban versus warfarin in patients with advanced kidney disease. J Thromb Thrombolysis 2018;46:246–52.
25. Hu A, Niu J, Winkelmayer WC. Oral anticoagulation in patients with end-stage kidney disease on dialysis and atrial fibrillation. Semin Nephrol 2018; 38:618–28.
26. Kalra PA, Burlacu A, Ferro CJ, Covic A. Which anticoagulants should be used for stroke prevention in non-valvular atrial fibrillation and severe chronic kidney disease? Curr Opin Nephrol Hypertens 2018;27:420–5.
27. Lopes RD, Steffel J, Di Fusco M, Keshishian A, Luo X, Li X et al. Effectiveness and safety of anticoagulants in adults with non-valvular atrial fibrillation and concomitant coronary/peripheral artery disease. Am J Med 2018;131:1075–85.
28. Garza-Mayers AC, Shah R, Sykes DB, Nigwekar SU, Kroshinsky D. The successful use of apixaban in dialysis patients with calciphylaxis who require anticoagulation: a retrospective analysis. Am J Nephrol 2018;48:168–71.
29. McCullough PA, Sandberg KR, Borzak S, Hudson MP, Garg M, Manley HJ. Benefits of aspirin and beta-blockade after myocardial infarction in patients with chronic kidney disease. Am Heart J 2002;144:226–32.
30. Berger AK, Duval S, Krumholz HM. Aspirin, beta-blocker, and angiotensin-converting enzyme inhibitor therapy in patients with end-stage renal disease and an acute myocardial infarction. J Am Coll Cardiol 2003;42:201–8.
31. Teng R, Muldowney S, Zhao Y, Berg JK, Lu J, Khan ND. Pharmacokinetics and pharmacodynamics of ticagrelor in subjects on hemodialysis and subjects with normal renal function. Eur J Clin Pharmacol 2018;74:1141–8.
32. Nigwekar SU, Thadhani R. Long-term anticoagulation for patients receiving dialysis. Circulation 2018;138:1530–3.
33. Dewilde WJ, Oirbans T, Verheugt FW, Kelder JC, De Smet BJ, Herrman JP et al. Use of clopidogrel with or without aspirin in patients taking oral anticoagulant therapy and undergoing percutaneous coronary intervention: an open-label, randomised, controlled trial. Lancet 2013;381:1107–15.
34. Fiedler KA, Maeng M, Mehilli J, Schulz-Schupke S, Byrne RA, Sibbing D et al. Duration of triple therapy in patients requiring oral anticoagulation after drug-eluting stent implantation: The ISAR-TRIPLE Trial. J Am Coll Cardiol 2015;65:1619–29.
35. Gibson CM, Mehran R, Bode C, Halperin J, Verheugt FW, Wildgoose P et al. Prevention of bleeding in patients with atrial fibrillation undergoing PCI. N Engl J Med 2016;375:2423–34.
36. Piccini JP, Jones WS. Dual antithrombotic therapy with dabigatran after PCI in atrial fibrillation. N Engl J Med 2018;378:486.
37. Lopes RD, Vora AN, Liaw D, Granger CB, Darius H, Goodman SG et al. An open-Label, 2 x 2 factorial, randomized controlled trial to evaluate the safety of apixaban vs vitamin K antagonist and aspirin vs placebo in patients with atrial fibrillation and acute coronary syndrome and/or percutaneous coronary intervention: Rationale and design of the AUGUSTUS trial. Am Heart J 2018;200:17–23.
38. Vranckx P, Lewalter T, Valgimigli M, Tijssen JG, Reimitz PE, Eckardt L et al. Evaluation of the safety and efficacy of an edoxaban-based antithrombotic regimen in patients with atrial fibrillation following successful percutaneous coronary intervention (PCI) with stent placement: Rationale and design of the ENTRUST-AF PCI trial. Am Heart J 2018;196:105–12.
39. Kerneis M, Talib U, Nafee T, Daaboul Y, Pahlavani S, Pitliya A et al. Triple antithrombotic therapy for patients with atrial fibrillation undergoing percutaneous coronary intervention. Prog Cardiovasc Dis 2018;60:524–30.
40. TSchopp M, Pfiffner P. MedCalX calculateur médical inc (2008) [Application mobile]. Disponible sur : http://itunes.apple.com.
PHARMACTUEL , Vol. 54 , No. 3, 2021