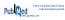Étude THEMIS : le ticagrélor en association avec l’acide acétylsalicylique est-il efficace et sécuritaire pour prévenir les événements cardiovasculaires ischémiques chez les patients diabétiques ayant une maladie coronarienne stable?
Lorence
St-Pierre
,
Pharm.D., M.Sc.
1,2,3,
Jade
Landry
,
Pharm.D., M.Sc.
1,2,4,
Mireille
Plante
,
Pharm.D.
1,2,5,6,
Maude
Plante
,
Pharm.D., M.Sc.
1,2,7,
Julie
Méthot
,
B.Pharm., M.Sc., Ph.D.
8,9
1
Candidat à la maîtrise en pharmacothérapie avancée au moment de la rédaction, Faculté de pharmacie, Université Laval, Québec (Québec) Canada
;
2
Résidente en pharmacie au moment de la rédaction, Centre intégré de santé et de services sociaux de Chaudières-Appalaches, Hôtel-Dieu de Lévis, Lévis (Québec) Canada
;
3
Pharmacienne, Centre intégré de santé et de services sociaux de Chaudière-Appalaches, Hôpital de Thetford Mines, Thetford Mines (Québec) Canada
;
4
Pharmacienne, Centre intégré de santé et de services sociaux de la Côte-Nord, Minganie, Havre-Saint-Pierre (Québec) Canada
;
5
Pharmacienne, Uniprix J. Bergeron et C. Dupuis-Brousseau, Lévis (Québec) Canada
;
6
Pharmacienne, Clinique médicale Saint-Louis, Québec (Québec) Canada
;
7
Pharmacienne, Centre intégré universitaire de santé et de services sociaux de la Capitale-Nationale, Québec (Québec) Canada
;
8
Pharmacienne et chercheure associée, Institut universitaire de cardiologie et de pneumologie de Québec
–
Université Laval, Québec (Québec) Canada
;
9
Professeure agrégée et directrice du programme de maîtrise en pharmacothérapie avancée, Faculté de pharmacie, Université Laval, Québec (Québec) Canada
Reçu le 30 septembre 2020: Accepté après révision par les pairs le 20 décembre 2020
Titre de l’article: Ticagrelor in patients with stable coronary disease and diabetes. N Engl J Med 2019;381:1309-201.
Auteurs : Steg PG, Bhatt DL, Simon T, Fox K, Mehta SR, Harrington RA et coll.
Commanditaires : Cette étude a été financée par la compagnie biopharmaceutique AstraZeneca.
Cadre de l’étude
: Les événements cardiovasculaires, l’une des graves complications du diabète, sont majoritairement causés par de l’athérosclérose et des thromboses vasculaires qui impliquent les plaquettes sanguines2–5. Puisqu’il a été démontré
in vitro
que l’activation et l’agrégation plaquettaire sont plus importantes chez les personnes diabétiques, on pourrait penser que, dans cette population, l’ajout d’un agent antiplaquettaire comme l’acide acétylsalicylique (AAS), surtout en présence de maladie coronarienne stable, est bénéfique6. Toutefois, des études
in vivo
ont démontré que les plaquettes des patients diabétiques sont plus susceptibles d’être résistantes à l’effet de l’AAS, ce qui permet de s’interroger sur son utilisation en monothérapie7,8.
Par ailleurs, il a été démontré que le ticagrélor aurait un effet antiplaquettaire plus constant que l’AAS ou le clopidogrel9. Son utilisation en association avec l’AAS en prévention secondaire a aussi fait largement ses preuves, et ce, indépendamment du statut de diabète10–14. Toutefois, la littérature scientifique actuelle ne permet pas de déterminer clairement si les patients diabétiques ayant une maladie coronarienne stable bénéficieraient également de cette association d’antiplaquettaires. Cette piste demeure donc à explorer, étant donné le risque plus élevé d’événements cardiovasculaires chez les patients diabétiques et leur plus grande susceptibilité à présenter une résistance à l’AAS.
Protocole de recherche
: L’étude THEMIS vise à évaluer l’efficacité et la sécurité du ticagrélor en association avec l’AAS à faible dose chez les patients diabétiques ayant une maladie coronarienne stable. Il s’agit d’une étude à répartition aléatoire contrôlée à double insu comparant le ticagrélor au placebo, en association avec l’AAS. Cet essai clinique a été mené auprès de 1315 sites localisés dans 42 pays, dont le Canada.
Patients
: La population à l’étude était composée de patients de 50 ans et plus qui avaient une maladie coronarienne stable et un diabète de type 2, sans antécédent d’événements ischémiques. La présence d’une maladie coronarienne stable a été définie comme suit : intervention coronarienne percutanée (ICP) antérieure, pontage aorto-coronarien (PAC) antérieur ou sténose documentée d’une artère coronaire d’au moins 50 %. La présence d’un diabète de type 2 a été définie par la prise d’une médication antihyperglycémique depuis au moins six mois. Les patients ayant déjà fait un infarctus du myocarde (IM) ou un accident vasculaire cérébral (AVC) étaient exclus. Plusieurs autres critères d’exclusion étaient pris en considération, notamment : prise concomitante d’un anticoagulant, d’un autre antiplaquettaire, d’AAS à une dose journalière supérieure à 150 mg ou d’un inhibiteur fort du CYP3A4, prédisposition aux saignements, trouble de la coagulation, antécédent de saignement intracrânien, saignement gastro-intestinal dans les six mois précédant la répartition aléatoire, dialyse.
Interventions
: La répartition aléatoire s’est effectuée en blocs selon un ratio 1:1 pour les deux traitements à l’étude, soit le ticagrélor 90 mg deux fois par jour ou le placebo. Tous les patients ont également reçu de l’AAS à faible dose (75 à 150 mg), à moins d’une contre-indication ou d’une intolérance importante. La durée médiane de suivi a été de 39,9 mois. En mai 2015, un amendement au protocole a été réalisé en diminuant la dose de ticagrélor à 60 mg deux fois par jour à la suite de la publication des résultats de l’étude PEGASUS-TIMI 5412. Cette étude avait pour objectif de comparer deux doses de ticagrélor (60 et 90 mg) en association avec de l’AAS à un placebo chez les patients ayant subi un IM il y a un à trois ans. Les résultats ont démontré une efficacité similaire, mais un profil de tolérabilité supérieur pour la plus faible dose.
Points évalués
: L’objectif primaire d’efficacité était la survenue combinée de décès cardiovasculaires, d’IM ou d’AVC. Des objectifs secondaires d’efficacité ont été évalués, soit chacun des éléments de l’objectif primaire mesuré individuellement ainsi que la survenue de décès de toutes causes. L’objectif exploratoire de bénéfice net, regroupant la mortalité de toutes causes, l’IM, l’AVC et le saignement mortel ou l’hémorragie intracrânienne, a été évalué. Quant à l’objectif primaire de sécurité, il s’agissait de la survenue de saignements majeurs, définis selon la classification du Thrombolysis in Myocardial Infarction (TIMI)11.
Résultats
: Du 10 février 2014 au 24 mai 2016, 19 271 patients ont été initialement répartis aléatoirement dans les deux groupes à l’étude. Un site de l’étude a été fermé en raison du non-respect des bonnes pratiques cliniques lors d’un autre projet de recherche. Au final, 19 220 patients ont été répartis aléatoirement et inclus dans les analyses d’efficacité en intention de traiter modifiée : 9619 dans le groupe ticagrélor et 9601 dans le groupe placebo. Les analyses de sécurité ont été effectuées sur les patients qui avaient reçu au moins une dose de ticagrélor ou de placebo : 9562 dans le groupe ticagrélor et 9531 dans le groupe placebo.
Le tableau I décrit les principales caractéristiques des patients à l’étude. Elles étaient similaires entre les deux groupes.
Tableau I
Caractéristiques de base des patients inclus dans l’étude THEMISa
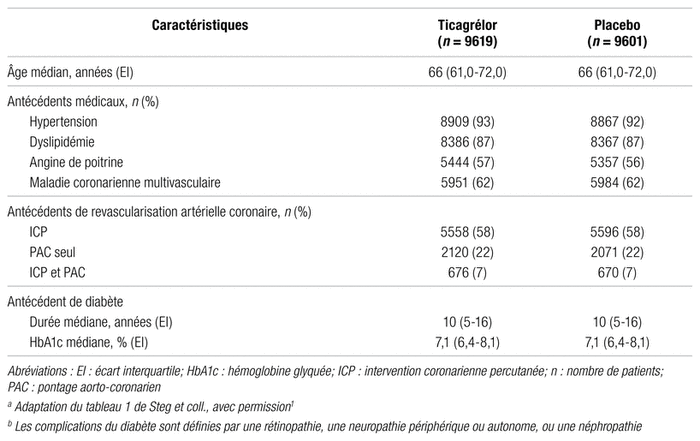
Le tableau II présente les principaux résultats liés aux objectifs d’efficacité de l’étude. L’ajout du ticagrélor à l’AAS a été associé à une diminution significative de la survenue de l’objectif primaire combiné de décès cardiovasculaires, d’IM ou d’AVC. En effet, 736 patients du groupe ticagrélor (7,7 %) ont présenté un événement, comparativement à 818 patients du groupe placebo (8,5 %), avec rapport de risques [RR] : 0,90; intervalle de confiance : 95 % [IC 95 %] 0,81–0,99;
p
= 0,04. Cela découle d’une incidence d’IM et d’AVC plus faible que dans le groupe placebo. L’analyse des résultats des objectifs secondaires a été effectuée hiérarchiquement. Puisqu’aucune différence significative ne ressortait entre les deux groupes pour les décès cardiovasculaires, l’analyse a pris fin. Le nombre nécessaire de patients à traiter pour prévenir un événement de l’objectif primaire
à
36 mois est de 138. Les patients sous ticagrélor et sous placebo ont présenté l’objectif exploratoire regroupant la mortalité de toutes causes, l’IM, l’AVC et le saignement mortel ou l’hémorragie intracrânienne de façon similaire (10,1 %
vs
10,8 % respectivement, avec RR : 0,93; IC 95 % 0,86–1,02).
Tableau II
Principaux résultats d’efficacité de l’étude THEMISa,b
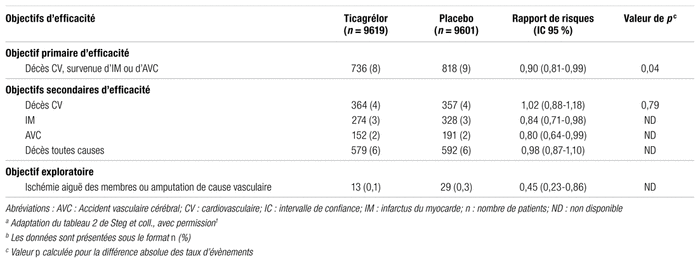
Le tableau III inclut les principaux résultats relatifs aux objectifs de sécurité. Les patients sous ticagrélor ont eu davantage de saignements majeurs TIMI que les patients du groupe placebo (2,2 %
vs
1,0 % avec RR : 2,32; IC 95 %, 1,82–2,94;
p
< 0,001). Cependant, il n’y a eu aucune différence significative entre les deux groupes quant à la survenue de saignements fatals. Le nombre nécessaire de patients à traiter sur une période de 36 mois pour que se produisent des saignements majeurs est de 93. Les saignements intracrâniens ont été plus fréquents dans le groupe ticagrélor. Cette différence a été entraînée par des saignements intracrâniens causés par des traumas, et non à la survenue de saignements spontanés ou causés par des procédures.
Tableau III
Principaux résultats de sécurité de l’étude THEMISa,b
Grille d’évaluation critique

Discussion
L’étude THEMIS, présentée initialement au congrès de l’European Society of Cardiology à Paris, en 2019, possède plusieurs forces1,15. D’abord, plusieurs caractéristiques de la population à l’étude sont représentatives des patients diabétiques rencontrés dans notre pratique, et leur prise en charge reflète la pratique actuelle. En effet, le choix des molécules utilisées pour traiter le diabète et les autres facteurs de risque concomitants étaient laissés à la discrétion des médecins traitants selon les lignes directrices en vigueur, rendant ainsi les résultats généralisables à une grande partie de la population diabétique sans antécédent d’évènement ischémique. Par ailleurs, la répartition aléatoire dans les différents groupes ainsi que la réalisation de l’étude en double aveugle, contrôlée par placebo, ont permis de limiter, respectivement, les biais de confusion et les biais d’information. La taille de l’étude est également une force en raison de la précision qu’elle procure aux intervalles de confiance. De plus, les objectifs de l’étude étaient pertinents et adaptés à la pratique actuelle, permettant de répondre à une interrogation réelle du monde médical : l’intensification du régime antiplaquettaire chez les diabétiques ayant une maladie coronarienne stable réduit-elle le risque d’événements cardiovasculaires?
Par ailleurs, plusieurs limites ont été établies. L’utilisation d’une analyse en intention de traiter modifiée pour l’efficacité est une faiblesse en raison de l’exclusion d’un certain nombre de patients. La diminution de la dose de ticagrélor au cours de l’essai pourrait avoir influé sur les résultats de l’étude. Tel que démontré dans l’étude PEGASUS TIMI-54, l’efficacité globale des deux doses s’est révélée similaire. Ainsi, la diminution de la dose de ticagrélor dans l’étude THEMIS devrait avoir eu un effet négligeable sur l’efficacité, mais elle pourrait avoir surestimé le risque de saignement total rapporté vu l’utilisation d’une dose plus élevée non nécessaire durant une partie de l’étude. Quant à l’arrêt définitif du traitement, il a été plus fréquent dans le groupe ticagrélor que dans le groupe placebo (34,5 %
vs
25,4 %), ce qui s’explique par la présence d’effets indésirables, notamment la dyspnée. Il est également reconnu qu’un taux d’Hb1Ac supérieur à 7,0 % est associé à une augmentation considérable du risque de complications cardiovasculaires16. Bien que l’Hb1Ac médiane des patients à l’étude soit comparable à celle que l’on rencontre dans la pratique canadienne, il aurait été intéressant de catégoriser les résultats d’efficacité selon l’Hb1Ac des patients17. En effet, il convient de se demander si les bénéfices quant à la prévention des évènements ischémiques du ticagrélor seraient plus importants chez les patients dont l’Hb1Ac est de 8 à 9 %. Enfin, des représentants de la compagnie biopharmaceutique AstraZeneca, qui a financé l’étude et commercialisé le ticagrélor, ont été prenantes dans les diverses étapes de l’étude. Une institution indépendante a validé toutes les données rapportées, mais celle-ci a été financée par AstraZeneca.
Très peu d’études se sont penchées sur les thérapies antiplaquettaires optimales pour la prévention des événements ischémiques chez les patients diabétiques souffrant d’une maladie coronarienne stable. Tout d’abord, THEMIS-PCI a analysé un sous-groupe de ses patients, soit ceux ayant déjà subi une ICP. L’ajout de ticagrélor à l’aspirine dans cette population a entraîné une réduction statistiquement significative de 15 % du risque relatif de survenue du composite d’AVC, d’IM et de mortalité cardiovasculaire, sans cependant diminuer la mortalité cardiovasculaire seule. Cette double thérapie antiplaquettaire (DTAP) semble offrir un bénéfice clinique net dans cette cohorte de patients, et ce, même lorsque l’on prend en considération les dommages irréversibles pouvant y être associés, tels que les saignements mortels ou intracrâniens qui n’étaient pas augmentés de manière statistiquement significative dans l’étude. Ce bénéfice est présent indépendamment du temps qui s’est écoulé depuis la dernière ICP. L’étude THEMIS-PCI porte à croire que l’association de ticagrélor et d’aspirine à faible dose pourrait être envisagée chez les patients diabétiques souffrant d’une maladie coronarienne stable qui ont subi une ICP et présentant un faible risque de saignement18. Une stratégie différente a été explorée dans les études GLOBAL LEADERS et TWILIGHT. En effet, étant donné qu’une élévation de l’incidence d’hémorragie intracrânienne a été rapportée avec l’administration d’une DTAP, il a été suggéré que la prise d’aspirine ne serait pas toujours requise en concomitance avec un inhibiteur du récepteur P2Y12 et qu’elle pourrait augmenter le risque de saignement sans pour autant contribuer de façon importante à l’efficacité. Les résultats de l’étude TWILIGHT tendent à confirmer cette hypothèse, alors que ceux de l’étude GLOBAL LEADERS sont peu concluants19–21. L’étude COMPASS a quant à elle évalué des patients atteints de maladie coronarienne stable ou de maladie artérielle périphérique22. L’association du rivaroxaban 2,5 mg deux fois par jour à de l’aspirine 100 mg par jour a entraîné une réduction de l’objectif primaire d’efficacité combinant la mortalité cardiovasculaire, l’IM et l’AVC, tout en réduisant la mortalité toutes causes. La réduction de l’objectif primaire était maintenue en présence de diabète et était indépendante d’une maladie vasculaire périphérique concomitante. La posologie du rivaroxaban utilisé dans l’étude COMPASS est remboursée au Québec selon certains critères23. La population de l’étude THEMIS comprenant des patients coronariens et diabétiques se retrouvait dans l’étude COMPASS. Cette dernière a démontré des bénéfices cliniques supérieurs à ceux de l’étude THEMIS1,22. L’étude THEMIS démontre donc que l’ajout de ticagrélor à l’aspirine à faible dose entraîne une réduction modeste du risque de subir un événement cardiovasculaire ischémique dans la population à l’étude. Toutefois, cette diminution du risque ne se traduit pas par une diminution de l’incidence de la mortalité cardiovasculaire, et les risques de saignements sont supérieurs aux bénéfices. L’impact clinique de cette étude dans la pratique est donc faible, en plus que le ticagrélor à la dose de 60 mg n’est pas remboursé au Québec, ce qui diminue nettement l’applicabilité des résultats à cette population23.
Conclusion
En conclusion, l’étude THEMIS a démontré que chez les patients atteints de diabète de type 2, ayant une maladie coronarienne stable sans antécédent d’IM ou d’AVC, l’association du ticagrélor avec l’aspirine à faible dose a diminué le risque d’événements ischémiques, aux dépens toutefois d’une augmentation du risque de saignement majeur. Les risques étant plus importants que les bénéfices, un changement de pratique n’est pas attendu à la suite de la publication de ces résultats. Peut-être qu’une monothérapie à base de ticagrélor, plutôt que combinée à l’aspirine, aurait pu se traduire par un ratio risques-bénéfices plus intéressant. D’autres études seront nécessaires pour évaluer cette question.
Financement
Aucun financement en relation avec le présent article n’a été déclaré par les auteurs.
Conflits d’intérêts
Tous les auteurs ont rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. Julie Méthot est rédactrice adjointe de
Pharmactuel
. Les auteurs n’ont déclaré aucun autre conflit d’intérêts en relation avec le présent article.
Références
1. Steg PG, Bhatt DL, Simon T, Fox K, Mehta SR, Harrington RA et al. Ticagrelor in patients with stable coronary disease and diabetes. N Engl J Med 2019;381:1309–20.

2. Haffner SM, Lehto S, Ronnemaa T, Pyorala K et Laakso M. Mortality from coronary heart disease in subjects with type 2 diabetes and in nondiabetic subjects with and without prior myocardial infarction. N Engl J Med 1998;339: 229–34.

3. Krempf M, Parhofer KG, Steg PG, Bhatt DL, Ohman EM, Rother J et al. Cardiovascular event rates in diabetic and nondiabetic individuals with and without established atherothrombosis (from the reduction of atherothrombosis for continued health [REACH] Registry). Am J Cardiol 2010;105:667–71.

4. Sarwar N, Gao P, Seshasai SR, Gobin R, Kaptoge S, Di Angelantonio E et al. Diabetes mellitus, fasting blood glucose concentration, and risk of vascular disease: a collaborative meta-analysis of 102 prospective studies. Lancet 2010;375:2215–22.

5. Cavender MA, Steg PG, Smith SC, Jr., Eagle K, Ohman EM, Goto S et al. Impact of diabetes mellitus on hospitalization for heart failure, cardiovascular events, and death: outcomes at 4 Years from the reduction of atherothrombosis for continued health (REACH) registry. Circulation 2015;132:923–31.

6. Patti G, Proscia C et Di Sciascio G. Antiplatelet therapy in patients with diabetes mellitus and acute coronary syndrome. Circ J 2014;78:33–41.

7. Angiolillo DJ, Fernandez-Ortiz A, Bernardo E, Ramirez C, Sabate M, Jimenez-Quevedo P et al. Influence of aspirin resistance on platelet function profiles in patients on long-term aspirin and clopidogrel after percutaneous coronary intervention. Am J Cardiol 2006;97:38–43.

8. Angiolillo DJ et Suryadevara S. Aspirin and clopidogrel: efficacy and resistance in diabetes mellitus. Best Pract Res Clin Endocrinol Metab 2009;23:375–88.

9. Husted S, van Giezen JJJ. Ticagrelor: the first reversibly binding oral P2Y12 receptor antagonist. Cardiovasc Ther 2009;27: 259–74..

10. Wang D, Yang XH, Zhang JD, Li RB, Jia M et Cui XR. Compared efficacy of clopidogrel and ticagrelor in treating acute coronary syndrome: a meta-analysis. BMC Cardiovasc Disord 2018;18:217.

11. Wallentin L, Becker RC, Budaj A, Cannon CP, Emanuelsson H, Held C et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009;361:1045–57.

12. Bonaca MP, Bhatt DL, Cohen M, Steg PG, Storey RF, Jensen EC et al. Long-term use of ticagrelor in patients with prior myocardial infarction. N Engl J Med 2015;372:1791–800.

13. Bhatt DL, Bonaca MP, Bansilal S, Angiolillo DJ, Cohen M, Storey RF et al. Reduction in ischemic events with ticagrelor in diabetic patients with prior myocardial infarction in PEGASUS-TIMI 54. J Am Coll Cardiol 2016;67: 2732–40.

14. James S, Angiolillo DJ, Cornel JH, Erlinge D, Husted S, Kontny F et al. Ticagrelor vs clopidogrel in patients with acute coronary syndromes and diabetes: a substudy from the platelet inhibition and patient outcomes (PLATO) trial. Eur Heart J 2010;31:3006–16.

15. European Society of Cardiology. Ticagrelor reduces ischaemic events in patients with diabetes and prior coronary intervention: results from THEMIS. ESC Congress News 2019 - Paris, France. 2 sep 2019. [en ligne] https://www.escardio.org/Congresses-&-Events/ESC-Congress/Congress-resources/Congress-news/ticagrelor-reduces-ischaemic-events-in-patients-with-diabetes-and-prior-coronary-intervention-results-from-themis (site visité le 13 décembre 2020).
16. Imran SA, Agarwal G, Bajaj HS et Ross S. Targets for glycemic control. Can J Diabetes 2018;42(suppl. 1):S42–6.

17. Harris SB, Ekoé JM, Zdanowicz Y et Webster-Bogaert S. Glycemic control and morbidity in the Canadian primary care setting (results of the diabetes in Canada evaluation study). Diabetes Res Clin Pract 2005;70:90–7.

18. Bhatt DL, Steg PG, Mehta SR, Leiter LA, Simon T, Fox K et al. Ticagrelor in patients with diabetes and stable coronary artery disease with a history of previous percutaneous coronary intervention (THEMIS-PCI): a phase 3, placebo-controlled, randomised trial. Lancet 2019;394: 1169–80.

19. Mehran R, Baber U, Sharma SK, Cohen DJ, Angiolillo DJ, Briguori C et al. Ticagrelor with or without aspirin in high-risk patients after PCI. N Engl J Med 2019;381:2032–42.

20. Chichareon P, Modolo R, Kogame N, Takahashi K, Chang CC, Tomaniak M et al. Association of diabetes with outcomes in patients undergoing contemporary percutaneous coronary intervention: Pre-specified subgroup analysis from the randomized GLOBAL LEADERS study. Atherosclerosis 2020;295:45–53.

21. Vranckx P, Valgimigli M, Jüni P, Hamm C, Steg PG, Heg D et al. Ticagrelor plus aspirin for 1 month, followed by ticagrelor monotherapy for 23 months vs aspirin plus clopidogrel or ticagrelor for 12 months, followed by aspirin monotherapy for 12 months after implantation of a drug-eluting stent: a multicentre, open-label, randomised superiority trial. Lancet 2018;392:940–9.

22. Eikelboom JW, Connolly SJ, Bosch J, Dagenais GR, Hart RG, Shestakovska O et al. Rivaroxaban with or without aspirin in stable cardiovascular disease. N Engl J Med. 2017; 377:1319–30.

23. Régie de l’assurance maladie du Québec. Liste des médicaments du 11 novembre 2020. [en ligne] https://www.ramq.gouv.qc.ca/SiteCollectionDocuments/professionnels/medicaments/liste-med_2020-11/Liste_medicaments_fr_2020-11.pdf (site visité le 13 décembre 2020).
Pour toute correspondance : Lorence St-Pierre, Centre intégré de santé et de services sociaux de Chaudières-Appalaches – Hôpital de Thetford Mines, 1717, rue Notre-Dame Est, Thetford Mines (Québec) G6G 2V4, CANADA; Téléphone : 418 338-7777; Courriel :
lorence.st-pierre.1@ulaval.ca
(Return to Top)
PHARMACTUEL
, Vol.
54
, No.
3,
2021