Pierre
Lemieux
,
B.Pharm., M.Sc., BCOP
1,
Mélanie
Masse
,
B.Pharm., M.Sc.
1
Reçu le 4 décembre 2020: Accepté après révision le 25 mars 2021
Résumé
Objectif : Présenter les économies réalisées au Centre intégré universitaire de santé et services sociaux de la Mauricie–et–du–Centre-du-Québec grâce à l’implantation de la stratégie posologique, pour le pembrolizumab, d’une dose en fonction du poids (mg/kg), jusqu’à la dose maximale.
Mise en contexte : Devant l’explosion des dépenses de médicaments avec l’arrivée de l’immunothérapie en oncologie, plusieurs cliniciens et regroupement d’experts se sont questionnés sur la stratégie posologique à privilégier pour le pembrolizumab. L’approche consistant à administrer un dosage mixte en mg/kg jusqu’à la dose maximale serait une stratégie acceptable en matière d’efficacité et permettrait de générer d’importantes économies.
Résultats : L’implantation de la stratégie posologique, pour le pembrolizumab, d’une dose en fonction du poids (mg/kg) jusqu’à la dose maximale au sein du Centre intégré universitaire de santé et services sociaux de la Mauricie–et–du–Centre-du-Québec a permis de réaliser des économies substantielles de plus de 1,5 million de dollars sur un an, ce qui correspond à une réduction des coûts de 25,5 % pour ce médicament.
Conclusion : L’approche consistant à administrer du pembrolizumab à un dosage mixte en mg/kg, jusqu’à atteindre la dose maximale est une méthode éprouvée pour réduire significativement les coûts par rapport à la dose recommandée dans la monographie de produit, tout en permettant de traiter aussi efficacement les patients atteints de cancer. Des analyses supplémentaires sont nécessaires afin de vérifier si l’emploi de stratégies visant à réduire les pertes de produits permettraient d’optimiser davantage les économies réalisées.
Mots clés : Dépenses de médicaments, pembrolizumab, pharmacoéconomie, stratégie posologique
Abstract
Objective : To describe the savings realized at the Centre intégré universitaire de santé et services sociaux de la Mauricie-et-du-Centre-du-Québec (CIUSSS MCQ) following the implementation of pembrolizumab dosing strategy of weight-based dosing (mg/kg), up to the maximum dose.
Background : Because of the increase in drug expenditures with the use of immunotherapy in oncology, many clinicians and groups of experts are questioning what the preferred dosing strategy should be for pembrolizumab. The mixed mg/kg approach to dosing up to the maximum dose appears to be an acceptable strategy in terms of efficacy and to generate considerable savings.
Results : The implementation of the pembrolizumab dosing strategy of weight-based dosing (mg/kg) up to the maximum dose at the CIUSSS MCQ has resulted in substantial savings of more than $1.5 million over one year, which corresponds to a 25.5% reduction in costs for this drug.
Conclusion : The mixed mg/kg approach to dosing up to the maximum dose is a proven method for significantly reducing costs compared to the dose recommended in the product monograph, while still treating cancer patients as effectively. Additional analysis is required to determine whether the use of strategies aimed at reducing product wastage would further optimize the savings.
Keywords : Dosing strategy, drug expenditures, pembrolizumab, pharmacoeconomics
Le pembrolizumab est un inhibiteur du point de contrôle immunitaire. En inhibant l’interaction entre le récepteur du ligand de mort cellulaire programmée 1 (de l’anglais programmed death ligand 1 [PD-1]) et ses ligands (PD-L1 et PD-L2), il réactive les lymphocytes T cytotoxiques spécifiques à la tumeur dans le microenvironnement tumoral, ce qui, par conséquent, réactive l’immunité antitumorale1. Il est actuellement approuvé au Canada pour le traitement des cancers suivants : mélanome adjuvant et métastatique, cancer du poumon non à petites cellules (CPNPC) métastatique, lymphome de Hodgkin, lymphome médiastinal primitif à cellules B, carcinome urothélial, adénocarcinome rénal, cancer associé à une forte instabilité microsatellitaire, carcinome de l’endomètre et carcinome épidermoïde de la tête et du cou métastatique1. Les schémas posologiques du pembrolizumab approuvés par Santé Canada ont évolué au fil du temps et dépendent des indications.
Les premières indications approuvées au Canada pour le pembrolizumab (en 2015) sont le mélanome métastatique et le traitement de deuxième intention du CPNPC métastatique dont les tumeurs expriment le PD-L1 (pourcentage de cellules tumorales [PCT] ≥ 1 %). Pour ces indications, la dose approuvée initialement était de 2 mg/kg toutes les trois semaines conformément aux études Keynote-002 et Keynote-0102–4. Toutefois, depuis le 31 août 2018, la posologie recommandée dans la monographie a été modifiée pour une dose fixe de 200 mg toutes les trois semaines, et ce, pour toutes les indications5. Cette modification fait suite à la publication par le fabricant des résultats d’évaluations pharmacocinétiques des schémas posologiques étudiés dans les essais cliniques sur le pembrolizumab, qui ont conclu que les doses de 200 mg et de 2 mg/kg toutes les trois semaines permettaient d’obtenir une exposition similaire au pembrolizumab6. La dose fixe de 200 mg toutes les trois semaines était celle utilisée dans les essais cliniques subséquents qui ont menés à l’approbation des nouvelles indications du pembrolizumab.
Au moment de réaliser notre étude, on reconnaissait quatre indications au pembrolizumab sur la Liste des médicaments – Établissements , soit le mélanome métastatique (première et deuxième intentions) et le CPNPC métastatique (deuxième intention PCT ≥ 1 % et première intention PCT ≥ 50 %)7. Les critères de la liste québécoise ne précisaient pas le schéma posologique recommandé pour le pembrolizumab.
Dans son évaluation du pembrolizumab pour le traitement initial du CPNPC métastatique PCT ≥ 50 % publiée en août 2018, le pan-Canadian Oncology Drug Review (PCODR) souligne, quant à lui, qu’il serait raisonnable d’utiliser une dose de 2 mg/kg jusqu’à la dose maximale de 200 mg toutes les trois semaines plutôt qu’une dose fixe de 200 mg8. Cet élément a été souligné également dans les évaluations subséquentes publiées par le PCODR pour les nouvelles indications du pembrolizumab (par exemple, carcinome urothélial réfractaire au sel de platine, CPNPC métastatique en association avec un sel de platine, mélanome adjuvant)9–11.
Le Programme de gestion thérapeutique des médicaments (PGTM) s’est également questionné sur la stratégie posologique à privilégier pour le pembrolizumab12. Ses participants ont procédé à une évaluation exhaustive des données d’efficacité clinique et pharmacocinétique en plus de faire une évaluation pharmaco-économique des stratégies de dosage du pembrolizumab, soit celle de la dose en fonction du poids (mg/kg) et de la dose fixe ou de la dose en fonction du poids (mg/kg) avec une dose maximale. Le PGTM estime que les deux schémas posologiques sont d’une efficacité comparable (dose de 2 mg/kg toutes les trois semaines et dose fixe de 200 mg toutes les trois semaines). Par conséquent, ils estiment qu’il serait acceptable de donner 2 mg/kg jusqu’à un maximum de 200 mg toutes les trois semaines, et que cette stratégie posologique permettrait de générer d’importantes économies, soit une réduction des dépenses des Centres hospitaliers universitaires (CHU) d’environ 30 %12.
Enfin, l’Institut national d’excellence en santé et en services sociaux (INESSS) a publié récemment un outil d’aide à la décision afin de guider les cliniciens dans le choix de la posologie du nivolumab et du pembrolizumab13. Ils recommandent à leur tour l’utilisation d’une dose calculée selon le poids, la dose fixe constituant la dose maximale, pour toutes les indications du nivolumab (en monothérapie) et du pembrolizumab.
Au Centre intégré universitaire de santé et de services sociaux de la Mauricie–et–du–Centre-du-Québec (CIUSSS MCQ), l’implantation de la stratégie posologique pour le pembrolizumab de la dose en fonction du poids (mg/kg) jusqu’à atteindre la dose maximale a eu lieu le 9 novembre 2018. Les économies réalisées grâce à l’application de cette mesure ont été mesurées et sont présentées ici.
À l’aide d’une revue d’utilisation médicamenteuse, les patients ayant reçu au moins une dose de pembrolizumab entre le 16 novembre 2018 et le 15 novembre 2019 dans l’une des cinq installations d’oncologie du CIUSSS MCQ ont été identifiés. Ces cinq installations sont le Centre hospitalier affilié universitaire régional de Trois-Rivières, l’Hôpital du Centre de la Mauricie de Shawinigan, l’Hôtel-Dieu d’Arthabaska de Victoriaville, l’Hôpital Sainte-Croix de Drummondville et l’Hôpital du Haut Saint-Maurice de La Tuque. Les patients ayant reçu le pembrolizumab dans le cadre d’un programme d’accès de la compagnie ou d’un protocole de recherche ont été exclus. Les informations quant à l’indication, au poids, à la dose utilisée et au nombre de doses reçues durant la période à l’étude ont été compilées.
Le calcul des économies réalisées (ER) par l’établissement de santé a été réalisé selon deux méthodes distinctes. Tout d’abord, une première analyse a été effectuée en fonction de la stratégie posologique étudiée dans les études cliniques pivots. Pour les indications dont la dose était fixe à 200 mg, nous avons multiplié le nombre de doses reçues ( n ) par la différence entre 200 mg et la dose réellement reçue (dr), le tout multiplié par le prix par milligramme. Aucune économie n’a été attribuée aux patients de plus de 100 kg. Pour les indications avec une dose évaluée en mg/kg, seules les doses utilisées pour les patients de plus de 100 kg ont été comptabilisées. Le nombre de doses reçues ( n ) a alors été multiplié par la différence entre la dose théoriquement indiquée (di) et 200 mg, le tout multiplié par le prix par milligramme. Le prix du pembrolizumab utilisé est basé sur le coût réel d’acquisition par l’établissement au moment de l’étude, soit 44 $/mg.
Calcul des économies réalisées – analyse en fonction de la stratégie posologique étudiée dans les études cliniques pivots :
Indications avec dose fixe de 200 mg
si <100 kg : ER = n × (200-dr) × 44
si ≥ 100 kg : ER = 0
Indications avec dose en mg/kg
si ≤ 100 kg : ER = 0
si > 100 kg : ER = n × (di-200) × 44
Une seconde analyse d’économie a été effectuée en fonction de la stratégie posologique recommandée dans la monographie actuelle, soit l’utilisation d’une dose fixe de 200 mg pour l’ensemble des indications du pembrolizumab. Dans cette analyse, nous avons utilisé la même formule que pour les indications à dose fixe de 200 mg (telle que décrite ci-haut) afin d’effectuer le calcul des économies réalisées, formule que nous avons appliquée à tous les patients.
Par ailleurs, les économies réalisées ont été comptabilisées en pourcentage des dépenses anticipées (économies réalisées + dépenses réelles) afin d’éviter de gonfler artificiellement la proportion d’économie réalisée en se basant seulement sur les dépenses réelles. Une autorisation a été obtenue du Directeur des services professionnels du CIUSSS MCQ pour la publication de cette étude.
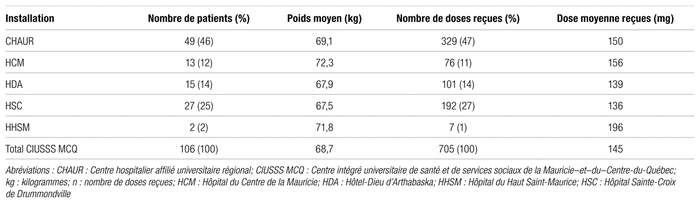
La répartition des doses de pembrolizumab reçues parmi les installations du CIUSSS MCQ est présentée au tableau I. La répartition des indications pour lesquelles le pembrolizumab a été utilisé est, quant à elle, illustrée à la figure 1, où l’on constate que la majeure partie de son utilisation est destinée au traitement du CPNPC métastatique en première intention PCT ≥ 50 %. Au cours de l’année à l’étude, les économies mesurées ont été supérieures à 1 million $, bien qu’elles aient été inférieures lorsque calculées en fonction de la stratégie posologique utilisée dans les études pivots (1,29 million $) plutôt qu’en fonction des recommandations actuelles de la monographie de produit (1,58 million $) (tableau II).
Tableau I
Répartition du nombre de patients et dedoses reçues par installation du CIUSSS MCQ

|
|
||
|
Figure 1
Répartition des indications par patient
|
||
Tableau II
Économies réalisées grâce à l’implantation de la stratégie posologique de la dose en fonction du poids (mg/kg) pour le pembrolizumab, jusqu’à atteindre la dose maximale de 200 mg, selon deux méthodes d’analyse
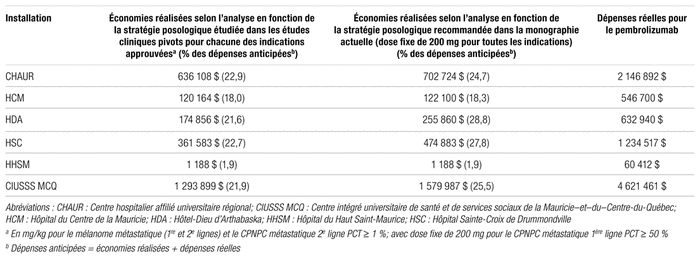
Au moment de la collecte des données, nous avons observé que la stratégie posologique du pembrolizumab en fonction du poids n’avait pas été appliquée chez tous les patients. En effet, le changement de posologie n’a pas été effectué pour 14 patients chez qui le traitement avait été instauré à la dose fixe de 200 mg. Des économies additionnelles de 206 730 $ auraient pu être réalisées si l’application de la stratégie posologique en fonction du poids avait eu lieu de façon systématique pour tous les patients.
L’implantation de la stratégie posologique de la dose en fonction du poids (mg/kg) pour le pembrolizumab, et ce, jusqu’à la dose maximale, au sein du CIUSSS MCQ a permis de réaliser des économies substantielles de plus de 1,5 million $ sur un an, ce qui correspond à une réduction des coûts pour le pembrolizumab de 25,5 %. Cette importante réduction s’explique entre autres par le fait que la dose fixe de 200 mg proposée par le fabricant est basée sur un poids moyen de 100 kg. Or le poids moyen des patients du CIUSSS MCQ recevant du pembrolizumab était de 68,7 kg. Les résultats de cette étude permettent par ailleurs de répondre à un des enjeux soulevés par Bérard et coll. concernant l’évaluation dans des conditions réelles d’utilisation de stratégies d’optimisation des doses des inhibiteurs du point de contrôle immunitaire14.
Dans sa publication, le PGTM estimait pour sa part les économies potentielles grâce à la mise en place de cette stratégie posologique à près de 30 %. L’écart entre nos résultats et les prévisions du PGTM peut s’expliquer en partie par le montant attribuable aux patients chez qui le changement de posologie n’a pas été appliqué (dose de 200 mg non modifiée), qui représente 3,3 % du montant total des économies anticipées. De plus, l’utilisation préférentielle du nivolumab pour le traitement de deuxième ligne du CPNPC métastatique au CIUSSS MCQ explique l’apparente disproportion de patients traités par pembrolizumab pour un CPNPC métastatique en première ligne par rapport aux autres indications.
Le pembrolizumab est conditionné en fiole à usage unique de 200 mg. L’utilisation d’une dose en fonction du poids (mg/kg) engendre l’utilisation incomplète des fioles disponibles pour les patients de moins de 100 kg. Les fioles ne contenant aucun agent de conservation, la norme 2014.02 de l’Ordre des pharmaciens du Québec (OPQ) impose une date limite d’utilisation (DLU) de 24 heures15. Cette limite d’utilisation entraîne des pertes de médicaments puisque la quantité résiduelle des fioles ne peut pas être utilisée ultérieurement. Ces pertes viennent donc influencer significativement à la baisse les économies réalisées. Les pertes de médicaments sont difficiles à quantifier, car elles ne sont pas documentées de façon uniforme dans les différentes installations de notre établissement. Pour l’installation du CHAUR, les pertes de pembrolizumab sont estimées à partir des ajustements d’inventaires réalisés une fois par semaine. Pour la période à l’étude, les ajustements d”inventaires se chiffrent à 294 997 $ pour le CHAUR, soit 13,7 % des dépenses totales de pembrolizumab dans cette installation et une réduction de 48,1 % des économies réalisées.
Une équipe de la Colombie-Britannique s’est elle aussi penchée sur la question des pertes de pembrolizumab et du schéma posologique à privilégier16. Bien que la période à l’étude soit antérieure à la nôtre, les résultats concordent fortement. En effet, lorsqu’on examine les résultats obtenus en ce qui concerne les coûts de l’approche par dosage mixte (dose en fonction du poids [mg/kg] jusqu’à la dose maximale) par rapport à la dose fixe, il est possible de constater que le dosage en mg/kg jusqu’à un maximum de 200 mg aurait permis à l’équipe de réduire les coûts de 26,4 % par rapport à la dose fixe de 200 mg. Une différence apparaît toutefois au sujet des pertes de médicaments, se situant à 8,65 % de ses dépenses totales de pembrolizumab. Ce taux plus faible par rapport à nos résultats peut s’expliquer notamment par la méthode de documentation des pertes reposant sur un registre, pouvant entraîner une sous-déclaration par rapport à notre méthode d’ajustement des inventaires, ainsi que par l’existence de fioles de 50 mg durant une partie importante de leur période d’étude.
Le pourcentage d’économie mesuré dans notre étude entre la dose fixe et l’approche par dosage mixte est supérieur à celui présenté par une équipe américaine (19 %)17. Cet écart peut notamment s’expliquer par le poids moyen des sujets plus élevé de 4,6 kg. Il est aussi important de mentionner que le calcul d’économie que nous avons établi est basé sur une utilisation à 100 % de la quantité résiduelle des fioles, contrairement à l’analyse américaine. Les auteurs ont d’ailleurs observé une relation directe entre le volume de patients et les économies réalisées en raison de la plus grande capacité des centres ayant un grand volume de patients à utiliser la quantité résiduelle des fioles.
Bien que les économies réalisées et documentées dans le cadre de notre étude soient importantes, nous croyons qu’elles sont sous-estimées. En effet, l’utilisation du pembrolizumab s’est étendue dans la dernière année avec l’ajout de plusieurs indications à la Liste des médicaments – Établissements , soit le CPNPC métastatique (première intention PCT ≥ 1 %), le mélanome adjuvant, le lymphome de Hodgkin récidivant et le carcinome urothélial métastatique en deuxième ligne18. Les économies anticipées avec l’implantation de la stratégie posologique de la dose en fonction du poids jusqu’à la dose maximale, et ce, pour toutes ces indications, seront donc encore plus imposantes.
Par ailleurs, la compagnie Merck a également inclus dans la monographie du pembrolizumab de nouvelles données de stabilité pour les fioles allant jusqu’à 96 heures au réfrigérateur. La prolongation de la date limite d’utilisation a pour effet de réduire les pertes de médicaments, puisque la quantité résiduelle des fioles peut être utilisée. On peut donc supposer que, dorénavant, les économies réalisées seront beaucoup plus près de celles présentées au tableau II, sans être amputées de près de la moitié par des pertes de médicaments. Ces économies sont encore plus grandes pour les établissements avec un gros volume d’utilisation de pembrolizumab. Les établissements ayant un faible volume d’utilisation devraient d’ailleurs envisager de concentrer les administrations de pembrolizumab sur une ou deux journée(s) dans la semaine de façon à maximiser l’utilisation des fioles.
Malgré l’ampleur des économies réalisées avec l’approche d’un dosage mixte en mg/kg toutes les trois semaines jusqu’à l’atteinte d’une dose maximale de 200 mg, son impact final est certainement moindre en raison des ententes d’inscription entre le ministre de la Santé et des Services sociaux et les compagnies pharmaceutiques. Le montant de 1,5 million $ est calculé ici à partir du coût d’acquisition du pembrolizumab plutôt qu’à partir du prix négocié, qui est confidentiel. Il est donc impossible de connaître l’impact budgétaire réel des efforts déployés par les pharmaciens d’établissement pour minimiser l’augmentation fulgurante de la charge financière que représentent les médicaments d’oncologie.
L’approche portant sur un dosage mixte de pembrolizumab en mg/kg jusqu’à atteindre la dose maximale est une méthode éprouvée pour réduire significativement les coûts par rapport à la dose recommandée dans la monographie de produit, tout en permettant de traiter aussi efficacement les patients atteints de cancer. Toutefois, la durée de stabilité de la fiole entamée et les formats de fioles disponibles peuvent grandement réduire les économies réalisées. Des analyses supplémentaires sont nécessaires afin de vérifier si le recours à une stratégie visant à réduire les pertes de produits, par exemple l’application d’une stabilité prolongée ou le regroupement des rendez-vous de patients recevant le pembrolizumab, permettra d’atteindre les objectifs visés.
Aucun financement en relation avec le présent article n’a été déclaré par les auteurs.
Les auteurs ont rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. M. Pierre Lemieux a donné des conférences pour Janssen et pour Abbvie dans le domaine de l’oncologie, et a été consultant pour Merck, Lundbeck, Janssen et Sandoz dans le domaine de l’oncologie. Mme Mélanie Masse a donné des conférences pour Astra Zeneca et Merck dans le domaine de l’oncologie, et a été consultante pour Roche, BMS et Otsuka Canada dans le domaine de l’oncologie.
1. Merck Canada. Monographie du pembrolizumab (KeytrudaMD). Toronto, Ontario. 9 octobre 2020.
2. Ribas A, Puzanov I, Dummer R, Schadendorf D, Hamid O, Robert C et al. Pembrolizumab versus investigator-choice chemotherapy for ipilimumab-refractory melanoma (Keynote-002MD): a randomised, controlled, phase 2 trial. Lancet Oncol 2015;16:908–18.
3. Herbst RS, Baas P, Kim DW, Felip E, Pérez-Gracia JL, Han JY et al. Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (Keynote-010MD): a randomised controlled trial. Lancet 2016;387:1540–50.
4. Merck Canada. Monographie du pembrolizumab (KeytrudaMD). Toronto, Ontario. Juillet 2018.
5. Merck Canada. Monographie du pembrolizumab (KeytrudaMD). Toronto, Ontario. Août 2018.
6. Freshwater T, Kondic A, Ahamadi M, Li CH, de Greef R, de Alwis D et al. Evaluation of dosing strategy for pembrolizumab for oncology indications. J Immunother Cancer 2017;5:43.

7. Régie de l’assurance maladie du Québec (RAMQ). Liste des médicaments fournis en établissement. 15 novembre 2018. [en ligne] https://www.ramq.gouv.qc.ca/sites/default/files/documents/liste_med_etab_2018_11_15_fr.pdf (site visité le 30 octobre 2020).
8. Pan-Canadian Oncology Drug Review (pCODR). Final recommandation for pembrolizumab (KeytrudaMD) for non-small cell lung cancer (first line). [en ligne] https://www.cadth.ca/sites/default/files/pcodr/pcodr_pembrolizumab_keytruda_nsclc_1stln_fn_rec.pdf (site visité le 30 octobre 2020).
9. Pan-Canadian Oncology Drug Review (pCODR). Final recommandation for pembrolizumab (KeytrudaMD) for metastatic urothelial carcinoma. [en ligne] https://www.cadth.ca/sites/default/files/pcodr/pcodr_pembrolizumab_keytruda_muc_fn_rec.pdf (site visité le 30 octobre 2020).
10. Pan-Canadian Oncology Drug Review (pCODR). Final recommandation for pembrolizumab (KeytrudaMD) for non-squamous non-small cell ling cancer. [en ligne] https://www.cadth.ca/sites/default/files/pcodr/Reviews2019/10153PembroNSQ-NSCLC_FnRec_approvedbyChair_Post_NOREDACT_31May2019_final.pdf (site visité le 30 octobre 2020).
11. Pan-Canadian Oncology Drug Review (pCODR). Final recommandation for pembrolizumab (KeytrudaMD) for melanoma adjuvant therapy. [en ligne] https://www.cadth.ca/sites/default/files/pcodr/Reviews2019/10168PembrolizumabMAT_FnRec_31%20July%202019__Post_01Aug2019_final.pdf (site visité le 30 octobre 2020).
12. Programme de gestion thérapeutique des médicaments (PGTM). PEMBROLIZUMAB (KEYTRUDAMD) Quelle stratégie posologique devrait-on privilégier : dose en fonction du poids, dose fixe ou dose en fonction du poids avec une dose maximale ? [en ligne] http://pgtm.org/documentation/FSW/Pembrolizumab_Strat%C3%A9gie%20posologique.pdf (site visité le 30 octobre 2020).
13. Institut national d’excellence en santé et services sociaux (INESSS). Choix de la posologie du nivolumab et du pembrolizumab. Rapport en soutien à l’outil d’aide à la décision. [en ligne] https://www.inesss.qc.ca/fileadmin/doc/INESSS/Rapports/Medicaments/INESSS_Nivolumab_Pembrolizumab_rapport.pdf (site visité le 30 octobre 2020).
14. Bérard G, Guèvremont C, Marcotte N, Michel MC, Varin F, Bonnici A et al. Les inhibiteurs du point de contrôle immunitaire : une stratégie de dosage à privilégier. Pharmactuel 2021;54:133–5.
15. Ordre des pharmaciens du Québec (OPQ). Norme 2014.02 - Préparation de produits stériles dangereux en pharmacie. [en ligne] https://www.opq.org/wp-content/uploads/2020/03/1847_38_fr-ca_0_norme201402_prod_striles_dang_oct2017.pdf (site visité le 30 octobre 2020).
16. Jang A, Nakashima L, Ng T, Fung M, Jiwani S, Schaff K et al. A real-world data approach to determine the optimal dosing strategy for pembrolizumab. J Oncol Pharm Pract 2021;27: 635–43.
17. Hall E, Zhang J, Kim EJ, Hwang G, Chu G, Bhatia S et al. Economics of alternative dosing strategies for pembrolizumab and nivolumab at a single academic cancer center. Cancer Med 2020;9:2106–12.

18. Régie de l’assurance maladie du Québec (RAMQ). Liste des médicaments fournis en établissement. September 30, 2020. [en ligne] https://www.ramq.gouv.qc.ca/sites/default/files/documents/liste-med-etab-2020-09-30-fr.pdf (site visité le 30 octobre 2020).
PHARMACTUEL , Vol. 55 , No. 1 , 2022