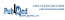Elizabeth Delisle, Pharm.D., M.Sc.1,2,3*, Kym Archambault, Pharm.D., M.Sc.1,4,5*, Laurence Doré, Pharm.D., M.Sc.1,2,3*, Sandra Arencibia Cubas, Pharm.D., M.Sc.1,2,6*, Annie Charbonneau, B.Pharm., M.Sc.7
2Résidente en pharmacie au moment de la rédaction, Centre intégré universitaire de santé et de services sociaux du Nord-de-l’île-de-Montréal, Hôpital du Sacré-Cœur, Montréal (Québec) Canada;
3Pharmacienne, Centre intégré universitaire de santé et de services sociaux du Nord-de-l’Île-de-Montréal, Hôpital du Sacré-Cœur de Montréal, Montréal (Québec) Canada;
4Résidente en pharmacie au moment de la rédaction, Centre universitaire de santé McGill, Montréal (Québec) Canada;
5Pharmacienne, Centre universitaire de Santé McGill, Hôpital Royal-Victoria, Montréal (Québec) Canada;
6Pharmacienne, Centre intégré de santé et de services sociaux de la Montérégie-Ouest, Hôpital Anna Laberge, Châteauguay (Québec) Canada;
7Pharmacienne, Centre universitaire de santé McGill, Site Glen, Montréal (Québec) Canada
Reçu le 25 avril 2021: Accepté après révision par 25 décembre 2021
Titre : Colchicine in patients with chronic coronary disease. N Engl J Med 2020;383:1838-471.
Auteurs : Nidorf SM, Fiolet ATL, Mosterd A, Eikelboom JW, Schut A, Opstal TSJ et coll. pour le groupe de chercheurs LoDoCo2.
Commanditaires : Cette étude a été financée par plusieurs contributeurs : National Health Medical Research Council of Australia, Sir Charles Gairdner Research Advisory Committee, Withering Foundation the Netherlands, Netherlands Heart Foundation, Netherlands Organization for Health Research and Development et un regroupement de Teva, Disphar et Tiofarma aux Pays-Bas. Les commanditaires n’ont participé ni à la rédaction du protocole de recherche, ni à la conduite de l’étude, ni à l’analyse des résultats.
Cadre de l’étude : Au Canada, la maladie coronarienne athérosclérotique demeure une cause de décès et d’hospitalisation importante. Malgré les traitements de prévention secondaire et la maîtrise des facteurs de risque, on constate une récurrence élevée d’événements2–4. Il est donc pertinent d’explorer de nouvelles avenues en prévention secondaire des maladies cardiovasculaires.
L’athérosclérose et les maladies cardiaques sont d’origine multifactorielle. Parmi les facteurs contributifs, une cascade inflammatoire pourrait être un facteur important5. En 2017, les résultats de l’étude CANTOS ont contribué à créer un engouement pour l’utilisation de molécules anti-inflammatoires6. Ridker et coll. ont en effet montré que, comparativement au placebo, le canakinumab, un anticorps monoclonal inhibant l’interleukine 1B, a réduit le risque composite d’infarctus du myocarde, d’accident vasculaire cérébral (AVC) ou de mort d’origine cardiovasculaire de 15 % chez les patients ayant un taux de protéine C réactive supérieur à deux, mais augmente toutefois le risque d’infections mortelles6.
La colchicine, un traitement répandu et peu coûteux étudié à quelques reprises dans les dernières années, réduit le taux de protéine C réactive7,8. Par son action sur les microtubules cellulaires et son effet inhibiteur sur la fonction des neutrophiles, la colchicine présente des propriétés anti-inflammatoires9. L’étude COLCOT a étudié cette molécule dans un contexte de maladie coronarienne aiguë et a révélé que son critère d’évaluation principal (mort d’origine cardiovasculaire, réanimation suivant un arrêt cardiaque, infarctus du myocarde, AVC ou hospitalisation pour cause d’angine) était moins fréquent chez les patients recevant la colchicine (0,5 mg une fois par jour) que chez ceux prenant le placebo10. Tong et coll. ont cependant obtenu des résultats contraires avec une dose de 0,5 mg, à raison de deux fois par jour. En effet, le traitement n’a pas réduit significativement l’occurrence du critère d’évaluation principal regroupant le syndrome coronarien aigu, l’arrêt cardiaque extrahospitalier ou l’AVC ischémique non cardio-embolique (Rapport de risques [RR] : 0,65; intervalle de confiance à 95 % [IC 95 %] : 0,38–1,09, p = 0,10). L’étude COPS a également soulevé une inquiétude concernant l’innocuité de la colchicine, évoquant un risque de mortalité toutes causes confondues supérieur au placebo11.
Dans la foulée de cet intérêt pour la colchicine, le groupe d’étude LoDoCo2 a tenté d’évaluer l’effet de ce traitement en prévention cardiovasculaire secondaire chez les patients atteints de maladie coronarienne chronique. Cette recherche se veut la suite de l’étude LoDoCo, une étude ouverte incluant 500 sujets qui a montré une supériorité de la colchicine sur le placebo pour le critère d’évaluation composite de syndrome coronarien aigu, d’arrêt cardiaque extrahospitalier ou d’AVC ischémique non cardio-embolique12.
Protocole de recherche : L’étude LoDoCo2 est un essai à répartition aléatoire contrôlé stratifié, à double insu contre placebo. C’est une étude multicentrique menée dans 13 hôpitaux publics et privés d’Australie et dans 30 centres des Pays-Bas. Le calcul de la taille de l’échantillon s’est basé sur celui de l’étude LoDoCo12. L’analyse du critère d’évaluation principal a été effectuée en fonction du délai d’apparition d’un événement, avec 331 événements à atteindre. Les critères d’évaluation secondaires ont été analysés de façon hiérarchique. Les chercheurs ont prévu une puissance de 90 % et une capacité à détecter une différence de 30 % (RR = 0,70) entre les deux groupes pour le critère principal, avec une valeur alpha de 0,05. Le protocole d’étude a été révisé et approuvé par un conseil institutionnel centralisé dans chaque pays. À la suite d’un recrutement plus lent qu’anticipé, les chercheurs ont modifié la taille de l’échantillon ainsi que le critère d’évaluation principal composite afin d’y inclure les revascularisations.
Patients : L’étude regroupait des patients de 35 à 82 ans souffrant d’une maladie coronarienne détectée par une coronarographie, une angiotomodensitométrie ou un score calcique coronaire d’au moins 400 unités d’Agatson mesuré par tomodensitométrie. Pour être admissibles à l’étude, les sujets potentiels devaient être dans un état clinique stable depuis six mois. Les critères d’exclusion étaient les suivants : insuffisance rénale modérée à sévère (clairance de la créatinine de moins 50 mL/min selon la classification du Kidney Disease : Improving Global Outcomes), insuffisance cardiaque sévère (New York Heart Association III ou IV), valvulopathie sévère, espérance de vie de moins de cinq ans ou effets indésirables connus à la prise de colchicine12,13.
Interventions : Avant la répartition aléatoire, tous les sujets ont fait une période d’essai avec la prise quotidienne de 0,5 mg de colchicine pendant un mois. Cette première phase a permis de s’assurer que l’état cardiovasculaire des patients demeurant dans l’étude était stable, que le traitement était bien toléré et que les sujets étaient motivés à poursuivre leur participation dans l’étude. Par la suite, les sujets toujours admissibles qui avaient bien toléré le traitement et qui l’avaient respecté ont été répartis aléatoirement dans deux groupes dans une proportion de 1:1, soit dans le groupe recevant quotidiennement 0,5 mg de colchicine, soit dans le placebo, avec stratification en fonction du pays. Les évaluations cliniques étaient prévues avant la période d’essai, au moment de la répartition aléatoire, puis à tous les six mois jusqu’à la fin de l’étude. Les suivis cliniques étaient poursuivis, nonobstant l’arrêt prématuré du traitement.
Points évalués : Le critère d’évaluation principal était un composite de mort cardiovasculaire, d’infarctus spontané non procédural du myocarde, d’AVC ischémique ou d’une revascularisation coronarienne après une ischémie aiguë. Le critère secondaire clé était un composite comprenant la mort d’origine cardiovasculaire, un infarctus spontané du myocarde ou un AVC ischémique. Les autres critères secondaires évalués étaient, dans l’ordre : un composite d’infarctus du myocarde ou de revascularisation coronarienne après une ischémie aiguë, un composite de mort d’origine cardiovasculaire ou d’infarctus spontané du myocarde, une revascularisation coronarienne après un événement ischémique aigu, un infarctus du myocarde, la mort toutes causes confondues ou la mort d’origine cardiovasculaire. Divers effets indésirables d’intérêt ont été évalués, dont la neutropénie, la dysesthésie, les myalgies, la myotoxicité et les cancers.
Résultats : Le recrutement s’est terminé en décembre 2018 et l’étude, le 22 mai 2020. Les caractéristiques de base des patients au début de l’étude étaient globalement similaires. Après la période d’essai, 15,4 % des patients n’ont pas toléré la colchicine et n’ont donc pas été répartis aléatoirement. Les caractéristiques de base des sujets étudiés sont présentées dans le tableau I. Une minorité de femmes ont été incluses (16,5 % pour le groupe colchicine et 14,1 % pour le groupe témoin). Parmi les 6528 patients qui ont consenti à participer à l’étude et qui ont commencé la période d’essai, 5522 ont été répartis aléatoirement et 5478 ont au moins reçu une dose de colchicine ou de placebo. Le suivi médian a été de 28,6 mois, et 10,5 % des patients dans chaque groupe ont terminé le traitement prématurément. Les résultats pour les points évalués sont présentés dans le tableau II. Le critère principal a été évalué en intention de traiter et les critères secondaires, selon une méthode hiérarchique. Un des événements du critère d’évaluation composite principal s’est produit chez 6,8 % des patients du groupe colchicine et chez 9,6 % des patients du groupe témoin (RR : 0,69; IC 95 % : 0,57–0,83, p < 0,001). Le critère secondaire clé a quant à lui été observé chez 4,2 % des patients du groupe colchicine et chez 5,7 % des patients du groupe témoin (RR : 0,72; IC 95 % : 0,57–0,92, p = 0,007). Les cinq premiers points évalués selon la hiérarchie prédéfinie ont montré des différences significatives favorisant le groupe colchicine. Cependant, la colchicine n’a pas permis de réduire la mort toutes causes confondues après la hiérarchisation des analyses. Les données d’innocuité dans les deux groupes à l’étude sont présentées dans le tableau III. Les décès qui n’étaient pas d’origine cardiovasculaire étaient plus fréquents chez les sujets recevant la colchicine (RR : 1,51; IC 95 % : 0,99–2,31). Toutefois, en absolu, il s’agissait d’une augmentation de 0,6 %, soit 0,2 événement pour 100 patients-années. Un effet protecteur de la colchicine a été noté sur les symptômes de goutte. Des taux similaires de cancer, d’hospitalisation pour infection, de pneumonie ou de problème digestif ont été obtenus dans les deux groupes.
Tableau I Caractéristiques des patients lors de l’entrée dans l’étudea
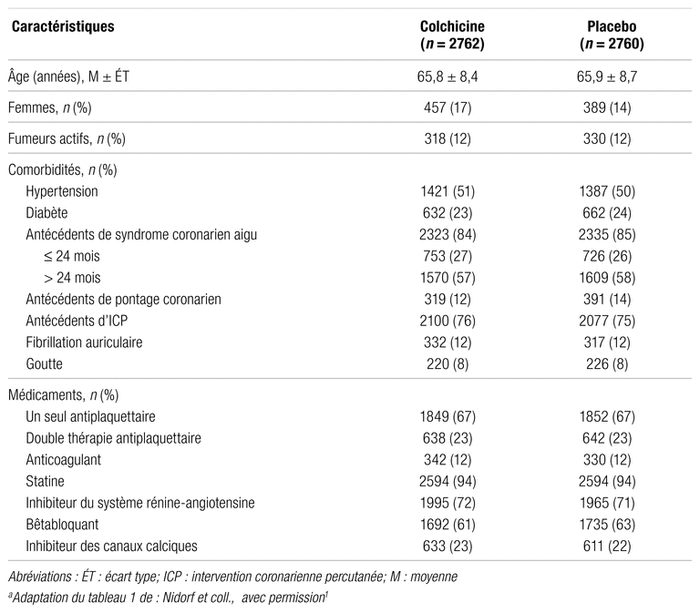
Tableau II Résultats pour les éléments évaluésa
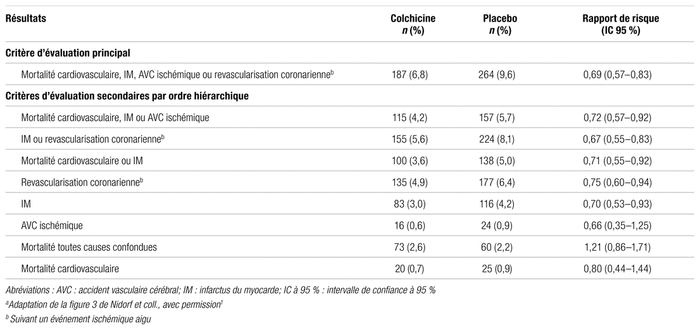
Tableau III Données d’innocuité pour les groupes à l’étudea