Exploration d’un test de détection des endotoxines dans les préparations magistrales stériles à risque élevé en centre hospitalier universitaire
Marc-Olivier Pilon, Pharm.D.1,2,3, Jean-Marc Forest, B.Pharm., DPH, M.Sc.4, Thomas Sullivan, B.Sc., Pharm.D.5
1Candidat à la maîtrise en sciences pharmaceutiques au moment de la rédaction, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
2Candidat au doctorat en sciences pharmaceutiques, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
3Pharmacien, Pharmacie André et Daniel Kayal, L’Île-Perrot (Québec) Canada;
4Pharmacien, secteur fabrication, Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada;
5Pharmacien, Centre intégré universitaire de santé et de services sociaux du Centre-Ouest-de-l’Île-de-Montréal, Hôpital général juif, Montréal (Québec) Canada
Reçu le 27 janvier 2022: Accepté après révision le 30 août 2022
Résumé
Objectif : Évaluer une méthode de détection des endotoxines dans les préparations stériles à risque élevé, respectant la norme 2014.01, dans les départements de pharmacie des centres hospitaliers québécois.
Mise en contexte : Actuellement, il n’existe aucune recommandation claire concernant les méthodes de détection des endotoxines dans les départements de pharmacie des centres hospitaliers du Québec. Les échantillons à analyser sont parfois envoyés à l’extérieur de l’hôpital dans des laboratoires publics et privés.
Résultats : Il est possible de commander des ensembles de détection d’endotoxines à base de lysat d’amibocyte de limule, communément appelés épreuve biologique par gel coagulé ou « gel clot assay ». Une fois validés par différentes méthodes, ces ensembles pourraient être employés dans les installations d’un centre hospitalier afin de détecter la présence d’endotoxines.
Conclusion : Le recours à l’épreuve biologique par gel coagulé pour détecter les endotoxines dans les préparations stériles à risque élevé est envisageable dans un centre hospitalier québécois, mais nécessite une méthode rigoureuse et exhaustive.
Mots clés : Endotoxines, lysat d’amibocyte de limule, LAL, épreuve biologique par gel coagulé, préparations magistrales et stériles
Abstract
Objective : To evaluate a method for detecting the presence of endotoxins in high-risk sterile preparations, in accordance with standard OPQ 2014.01, in Quebec hospital pharmacy departments.
Background : Currently, there are no clear recommendations regarding detection methods of endotoxins in Quebec hospital pharmacy departments. Samples for analysis are sometimes sent outside the hospital to public and private laboratories.
Results : Endotoxin detection kits based on limulus amebocyte lysate, commonly called gel-clot assays, can be ordered. Once validated with various methods, these kits could be used in a hospital’s facilities to detect the presence of endotoxins.
Conclusion : The use of gel-clot assays to detect endotoxins in high-risk sterile preparations is feasible in Quebec’s hospitals but requires a rigorous, thorough method.
Keywords : Compounded and sterile preparations, endotoxins, gel-clot assay, LAL, limulus amebocyte lysate
Introduction
Les endotoxines, un type particulier d’agents pyrogènes, constituent un élément de la paroi cellulaire externe de toutes les bactéries à Gram négatif. Elles contribuent à l’organisation et à la stabilité de la membrane cellulaire1–6. Elles sont libérées lors de la division cellulaire ou de la mort cellulaire de la bactérie qui mène inévitablement à la rupture de la paroi cellulaire externe1–6. Ce pyrogène est composé de trois éléments communs: un antigène O, un noyau polysaccharidique et un lipide non polaire nommé lipide A2,7. Lorsqu’il est présent dans le sang, le lipide A engendre la production de cytokines pro-inflammatoires et l’activation de la cascade de coagulation8. Une telle réaction peut causer de la fièvre, la défaillance de plusieurs organes, une septicémie, un choc septique et même la mort.9 Une concentration aussi faible que 1 ng/kg/h d’endotoxines peut provoquer chez l’homme une augmentation marquée de sa température10.
Hormis quelques exceptions, les techniques de stérilisation habituelles ne permettent généralement pas d’éliminer totalement les endotoxines présentes a priori dans une préparation. Les endotoxines résistent normalement à la stérilisation par la chaleur humide et passent au travers de la plupart des filtres, y compris le filtre standard de 0,22 micron utilisé pour la filtration stérilisante en pharmacie hospitalière. Il faut également considérer que les méthodes de stérilisation menant à la mort des bactéries à Gram négatif par bris de la membrane externe libèrent des endotoxines. La stérilisation par chaleur sèche constitue un moyen efficace de se débarrasser des endotoxines, mais un tel processus n’est compatible qu’avec les matériaux et les substances résistant à de hautes températures. Par conséquent, elle ne peut être utilisée pour les préparations médicamenteuses qui présentent généralement des contraintes lors de la stérilisation, comme la résistance à la chaleur. Pour toutes ces raisons, il est préférable d’utiliser du matériel et des ingrédients exempts d’endotoxines, et de confirmer l’absence d’endotoxines tel qu’il est recommandé dans la norme 2014.01 de l’Ordre des pharmaciens du Québec (OPQ)11.
Selon la norme 2014.01, « un test de stérilité et de contrôle d’endotoxines bactériennes doit être effectué pour les préparations de produits stériles à risque élevé […] lors: de préparations de produits stériles en lots de plus de 25 unités identiques; d’un délai d’exposition de plus de 12 heures entre 2 et 8 °C avant la stérilisation; d’un délai d’exposition de plus de 6 heures à une température supérieure à 8 °C avant la procédure de stérilisation11 ». Ces tests de stérilité doivent également être appliqués pour pouvoir prolonger la date limite d’utilisation des produits11. Les échantillons des préparations fabriquées en milieu hospitalier faisant l’objet d’un contrôle de stérilité peuvent actuellement être envoyés au Laboratoire de santé publique du Québec (LSPQ) aux fins d’analyse. Au Québec, c’est un des laboratoires publics faisant de telles analyses. Il existe néanmoins de nombreux laboratoires privés offrant ce service. Des recherches ont été entamées afin d’évaluer différentes méthodes de détection des endotoxines pouvant être utilisées au département de pharmacie d’un centre hospitalier.
Les départements de pharmacie des centres hospitaliers du Québec sont soumis aux normes de l’OPQ se référant à la pharmacopée américaine. L’OPQ n’a émis aucune recommandation à l’égard des tests de détection des endotoxines. En revanche, Santé Canada considère que les méthodes présentées dans les pharmacopées américaine, japonaise et européenne, soit l’épreuve biologique par gel coagulé, l’épreuve chromogénique et l’épreuve turbidimétrique, sont interchangeables. En cas de doute, c’est l’épreuve biologique par gel coagulé qui doit être utilisée pour prendre la décision définitive concernant la conformité du produit testé12,13.
À ce jour, de nouvelles méthodes misant sur les affinités chimiques et biologiques des endotoxines ont été mises au point pour les détecter dans une quelconque substance7,14. Ces méthodes ne seront pas abordées dans le présent article.
Méthode
À partir des recherches précédentes, nous avons fait l’acquisition de l’ensemble ToxinSensor, une épreuve biologique par gel coagulé de l’entreprise GenScript15. Son principe d’utilisation est décrit dans le tableau I. Le matériel nécessaire à la réalisation du test est présenté dans le tableau II. Son utilisation, synthétisée dans la figure 1, va comme suit:
-
Tableau I Épreuve biologique par gel coagulé et ses considérations

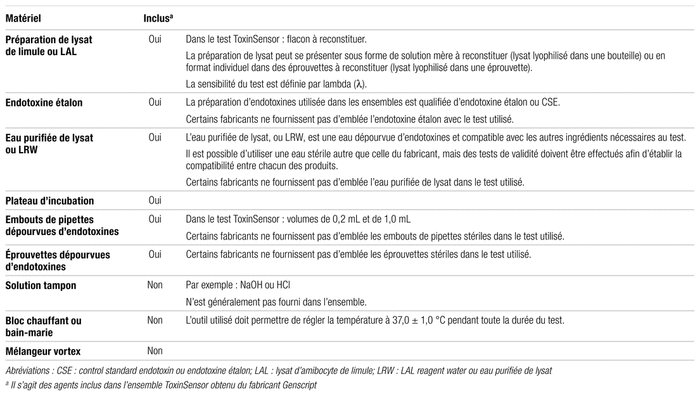
Tableau II Principaux agents requis pour l’épreuve biologique par gel coagulé
| |
| |
|
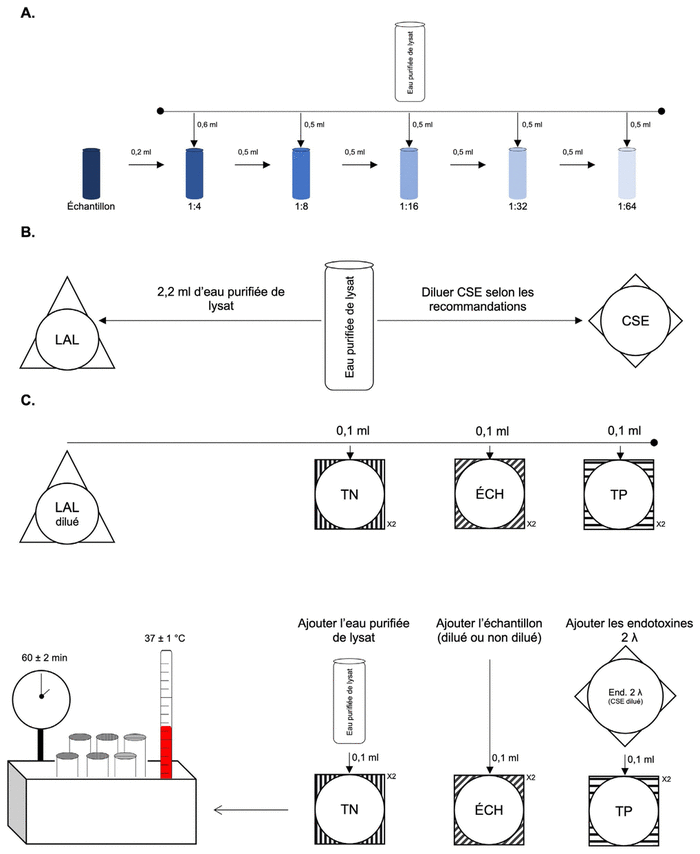
Figure 1 Manipulations nécessaires au déroulement de l’épreuve biologique par gel coagulé
Abréviations: LAL: lysat d’amibocyte de limule, CSE: endotoxine étalon, TN: témoin négatif, TP: témoin positif, ÉCH: échantillon
Légende: Le triangle représente la préparation de lysat, le losange, celle d’endotoxines et les carrés, différentes préparations à tester.
A. Au besoin, l’échantillon à tester doit préalablement être dilué. Les ratios recommandés dans la figure peuvent être utilisés en guise de repère
B. Afin de procéder aux manipulations, les préparations de lysat et d’endotoxine étalon doivent être reconstituées avec de l’eau purifiée de lysat. Une concentration de 2 λ doit être obtenue pour la préparation de l’endotoxine étalon
C. Différentes préparations seront testées (témoin positif, témoin négatif et échantillon). Il est donc recommandé d’identifier chaque éprouvette. Les préparations doivent être testées en double (X2). Lorsque chacune des préparations est mélangée à un volume constant de lysat, les éprouvettes doivent être mises dans un bain-marie (ou dispositif équivalent) à température appropriée pendant 60 minutes |
Conditions préalables
-
La valeur du pH de l’échantillon doit se trouver entre 6 et 8. Il est recommandé de l’ajuster avec une solution tampon, au besoin.
-
S’il faut diluer l’échantillon à tester, il est recommandé de procéder comme l’indique la figure 1. Le facteur de dilution maximal est déterminé par la dilution maximale permise (MVD ou maximum valid dilution, voir tableau I).
-
Préparation du lysat d’amibocyte de limule
-
Reconstituer le lysat en y ajoutant 2,2 mL d’eau purifiée de lysat.
-
Agiter doucement de 3 à 5 fois pour dissoudre le réactif et attendre 20 secondes avant l’utilisation.
-
Ne pas secouer ni inverser le contenant pour éviter la formation de mousse.
-
Le lysat reconstitué se conserve une semaine à une température inférieure ou égale à −20 °C. À des températures supérieures, il doit être utilisé dans les 10 minutes suivant la reconstitution.
-
Préparation du témoin positif
Remarque: Il est recommandé d’utiliser un témoin positif dont la concentration d’endotoxines est d’au moins 2 λ par rapport à celle de la sensibilité du test (p. ex., si la sensibilité du test est de 0,125 unité d’endotoxines (UE)/mL, la concentration du témoin positif doit être d’au moins 0,25 UE/mL)16.
-
Reconstituer l’endotoxine étalon avec 1 à 2 mL d’eau purifiée de lysat conformément aux instructions indiquées sur l’étiquette.
-
La concentration de l’endotoxine étalon est inscrite sur la bouteille.
-
Passer la préparation au vortex pendant au moins 15 minutes pour obtenir une solution mère.
-
Cette solution se conserve jusqu’à 15 jours à une température inférieure ou égale à −20 °C.
-
Préparer une dilution d’endotoxines avec de l’eau purifiée de lysat afin d’obtenir une concentration de 2 λ.
-
Si plusieurs dilutions sont nécessaires pour obtenir une concentration adéquate de l’endotoxine étalon, chaque dilution doit être agitée au vortex pendant 30 secondes.
-
Le facteur de dilution maximal ne doit pas dépasser 10 fois la concentration de l’endotoxine étalon.
-
Préparation du témoin négatif
-
L’eau purifiée de lysat peut être utilisée comme témoin négatif.
-
Méthodologie
-
Transférer délicatement 0,1 mL de la solution de lysat dans différentes éprouvettes stériles préalablement identifiées (témoin négatif, témoin positif et échantillon).
-
Chaque préparation doit être faite en double.
-
Transférer délicatement 0,1 mL de témoin positif, de témoin négatif (eau purifiée de lysat) et des échantillons à tester dans les éprouvettes contenant le lysat, préparées à l’étape précédente.
-
Boucher les éprouvettes et mélanger délicatement.
-
Incuber toutes les éprouvettes à 37 ± 1 °C dans un bain-marie (ou tout autre dispositif équivalent, comme une étuveuse).
-
Retirer les éprouvettes du bain-marie après 60 ± 2 minutes d’incubation. Inverser chaque éprouvette et vérifier si un gel s’est formé ou non. Remarque: Ne pas secouer vigoureusement pendant la vérification, cela pourrait briser le gel coagulé.
-
Une réaction positive est caractérisée par la formation d’un gel ferme qui reste intact lorsque le tube est tourné de 180 °.
-
Une réaction négative est caractérisée par l’absence de caillot solide. Le lysat peut présenter une turbidité ou une viscosité accrue, mais le résultat est tout de même considéré comme négatif.
-
Calculer la quantité d’endotoxines.
-
La quantité d’endotoxines dans un échantillon positif est égale ou supérieure à la sensibilité de détection λ du test utilisé (ici ToxinSensor). Si une dilution de l’échantillon a été effectuée, elle doit être prise en compte dans l’interprétation du résultat (pour une dilution de 1: 200 p. ex., la quantité d’endotoxines dans l’échantillon positif est égale ou supérieure à 200 fois la sensibilité de détection λ du test utilisé).
-
Dans l’échantillon négatif, la quantité d’endotoxines est inférieure à la sensibilité de détection λ du test. Si une dilution de l’échantillon a été effectuée, elle doit être prise en compte dans l’interprétation du résultat (pour une dilution de 1:200 p. ex., la quantité d’endotoxines dans l’échantillon négatif est inférieure à 200 fois la sensibilité de détection λ du test utilisé).
-
Validation des résultats et entreposage des données
-
Il est primordial de valider les résultats du test effectué. Les préparations du témoin négatif doivent tester négativement alors que les préparations du témoin positif doivent tester positivement (formation d’un gel) afin que le test soit valide.
-
Des tests supplémentaires de validation de la méthode utilisée sont parfois recommandés et sont spécifiques à chacun des fabricants.
-
Tous les résultats doivent être documentés conformément aux modes opératoires normalisés en vigueur, aux bonnes pratiques de documentation et/ou aux politiques et aux méthodes du département.
Discussion
Il existe présentement sur le marché différents ensembles permettant de détecter les endotoxines dans diverses préparations. La plupart de ces ensembles reposent sur une réaction de coagulation se produisant dans le sang bleu de la limule (Limulus polyphemus), une sorte de crabe présent principalement sur les côtes américaines4,7,14,17. Les amibocytes sont des cellules sanguines de Limulus polyphemus qui permettent de produire le lysat d’amibocyte de limule, un extrait aqueux de ces cellules sanguines18. Le lysat coagule en présence d’une quantité suffisante d’endotoxines. Pour cette raison, le sang du limule est prélevé et traité.
Un test qualitatif a ainsi été créé afin de constater visuellement la formation d’une coagulation lorsqu’une quantité suffisante d’endotoxines est mélangée au lysat de limule. Il s’agit de l’épreuve de biologique par gel coagulé. Plusieurs fabricants distribuent ce genre de tests: Lonza (Pyrogen), Charles River (EndoSafe), GenScript (ToxinSensor) et Associates of Cape Cod (Pyrosate Kit)19–22. Cette épreuve est d’ailleurs de 3 à 300 fois plus sensible que la méthode privilégiée précédemment, soit le test de recherche des pyrogènes chez le lapin (« Rabbit Pyrogen Test »)18,23. Le « Rabbit Pyrogen Test » consistait à injecter une préparation à des lapins, puis à noter la présence d’une augmentation de température, le lapin présentant une sensibilité similaire à celle de l’humain aux endotoxines18.
Autres méthodes de détection des endotoxines
Une optimisation de l’épreuve biologique par gel coagulé a mené à la création de tests quantitatifs nécessitant l’utilisation d’un spectrophotomètre. Il s’agit de l’épreuve turbidimétrique et de l’épreuve chromogénique. Ces méthodes, tout comme l’épreuve biologique par gel coagulé, reposent sur la réaction enzymatique des cellules d’amibocytes lorsqu’elles sont exposées à des endotoxines7,14. L’épreuve chromogénique nécessite la modification du lysat de limule. Un substrat naturel, le coagulen, est ainsi remplacé par un substrat chromogène ou coloré. Lorsqu’il est activé par la réaction enzymatique, ce nouveau substrat dans la suspension libère une molécule chromogène mesurée par spectrophotométrie (voir figure 2)7,24. L’épreuve turbidimétrique permet plutôt d’observer la turbidité de la solution7,24. Les taux de turbidité et de changement d’absorbance sont proportionnels à la concentration d’endotoxines. À l’aide de ces nouvelles techniques, il est donc possible de quantifier les endotoxines présentes dans une préparation selon la turbidité de la préparation ou son caractère chromogène. Lonza (PYROGENT-5000 Kinetic Turbidimetric LAL Assay, Kinetic-QCL Kinetic Chromogenic LAL Assay), Charles River (Endochrome-K, KTA), Associates of Cape Cod (Pyrotell-T, Pyrochrome) fournissent tous ce genre d’ensemble19,20,22.
| |
| |
|
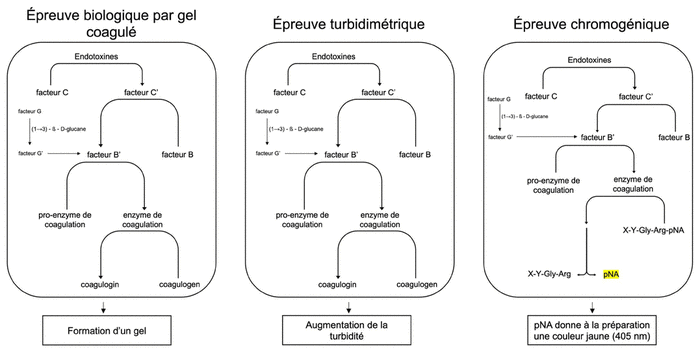
Figure 2 Cascade de coagulation de l’épreuve biologique par gel coagulé (gauche), de l’épreuve turbidimétrique (centre) et de l’épreuve chromogénique (droite)7,24
Légende: La cascade de coagulation présente dans le sang de limule est déclenchée par des endotoxines. L’élément clé de cette cascade est le facteur C. La même cascade peut s’enclencher à partir du facteur G, un facteur interférent |
L’épreuve turbidimétrique et l’épreuve chromogénique sont plus précises et plus sensibles que l’épreuve biologique par gel coagulé, mais nécessitent l’utilisation d’appareils plus sophistiqués, comme un spectrophotomètre, et une validation annuelle de l’équipement. De plus, les ensembles pour ces techniques coûtent généralement plus cher que ceux de l’épreuve biologique par gel coagulé. Toutefois, ils demandent moins de manipulations et permettent d’obtenir un résultat plus rapidement14,17,19,20,22. Comme nous l’avons mentionné précédemment, ces techniques sont acceptées par Santé Canada qui, actuellement, n’exige pas la validation des utilisateurs12,13. Les recommandations actuelles de la pharmacopée américaine sont toutefois de confirmer au besoin les résultats d’une épreuve turbidimétrique ou d’une épreuve chromogénique à l’aide de l’épreuve biologique par gel coagulé qui reste l’épreuve de référence.
Outre les contraintes découlant des techniques précédentes, la surpêche et la collecte de sang présentent une menace pour la population de limules25. Bien que les limules soient renvoyées à la mer après l’extraction d’un volume de leur sang, environ 20 % d’entre elles ne survivent pas26. C’est pourquoi une nouvelle méthode a été mise au point, celle du facteur C recombinant. Ce test repose sur le même principe que les méthodes précédentes, mais remplace le sang de limule par un facteur de coagulation, le facteur C, qui peut être complètement synthétisé en laboratoire. Contrairement aux autres techniques, le test du facteur C recombinant ne présente pas de risque pour la faune. Cette méthode ne fait pas partie des recommandations actuelles, mais plusieurs études en ont établi la supériorité, ou du moins son équivalence, par rapport à l’épreuve biologique par gel coagulé27,28. En 2014, la Direction européenne de la qualité du médicament et des soins de santé a révisé les lignes directrices sur l’utilisation d’ensembles pour la détection d’endotoxines bactériennes qui comprennent dorénavant le facteur C recombinant comme solution de rechange au lysat de limule28.
Conclusion
L’épreuve biologique par gel coagulé constitue un moyen relativement simple, rapide et accessible de détecter les endotoxines dans les préparations magistrales stériles à risque élevé dans les départements de pharmacie des centres hospitaliers du Québec. C’est une solution de rechange intéressante à l’envoi des échantillons à l’extérieur des hôpitaux aux fins d’analyse. Cependant, elle requiert une méthode rigoureuse, une validation et un protocole exhaustif pour être conforme.
L’industrie pharmaceutique est soumise à des normes claires et précises, alors que les normes que doivent respecter les départements de pharmacie des centres hospitaliers québécois manquent quelques fois de clarté. Néanmoins, certains centres hospitaliers québécois ont intégré dans leur milieu une méthode de détection des endotoxines. Ainsi, l’Hôpital général juif est un précurseur dans l’intégration et l’utilisation de l’épreuve biologique par gel coagulé au département de pharmacie. C’est un pas vers l’intégration de méthodes de détection dans les départements de pharmacie des centres hospitaliers du Québec.
Remerciements
Les auteurs reconnaissent l’aide apportée par le secteur de la physico-chimie du Laboratoire de santé publique du Québec et remercient Marcello Manocchio. Cette personne a donné son autorisation écrite.
Financement
Les auteurs n’ont déclaré aucun financement lié au présent article.
Conflits d’intérêts
Tous les auteurs ont soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts lié à cet article.
Références
1. Aida Y, Pabst MJ. Removal of endotoxin from protein solutions by phase separation using Triton X-114. J Immunol Methods 1990;132:191–5.

2. Anspach FB. Endotoxin removal by affinity sorbents. J Biochem Biophys Methods 2001; 49:665–81.

3. Gorbet MB, Sefton MV. Endotoxin: The uninvited guest. Biomaterials 2005;26:6811–7.

4. Magalhães PO, Lopes AM, Mazzola PG, Rangel-Yagui C, Penna TC, Pessoa A Jr. Methods of endotoxin removal from biological preparations: a review. J Pharm Pharm Sci 2007;10:388–404.
5. Ongkudon CM, Chew JH, Liu B, Danquah MK. Chromatographic removal of endotoxins: a bioprocess engineer’s perspective. ISRN Chromatography 2012;2012:649746.

6. Petsch D, Anspach FB. Endotoxin removal from protein solutions. J Biotechnol 2000;76:97–119.

7. Dullah EC, Ongkudon CM. Current trends in endotoxin detection and analysis of endotoxin-protein interactions. Crit Rev Biotechnol 2017; 37:251–61.

8. Ong KG, Leland JM, Zeng K, Barrett G, Zourob M, Grimes CA. A rapid highly-sensitive endotoxin detection system. Biosens Bioelectron 2006;21:2270–4.

9. Kim SE, Su W, Cho M, Lee Y, Choe WS. Harnessing aptamers for electrochemical detection of endotoxin. Anal Biochem 2012;424:12–20.

10. Warren HS, Fitting C, Hoff E, Adib-Conquy M, Beasley-Topliffe L, Tesini B et coll. Resilience to bacterial infection: difference between species could be due to proteins in serum. J Infect Dis 2010;201:223–32.

11. Ordre des pharmaciens du Québec. Norme 2014.01 Préparation de produits stériles non dangereux en pharmacie. 2017. p. 42.
12. European Medicines Agency. ICH guideline Q4B: Annex 14 to note for evaluation and recommendation of pharmacopoeial texts for use in the ICH regions on bacterial endotoxins tests – General chapter (2010). [en ligne] https://www.ema.europa.eu/en/ich-q4b-annex-14-bacterial-endotoxins-tests (site visité le 30 août 2022).
13. Food and Drug Administration. Guidance for industry: Q4B evaluation and recommendation of pharmacopoeial texts for use in the ICH Regions. Annex 14–Bacterial endotoxins test general chapter (2013). [en ligne] https://cacmap.fda.gov/media/79183/download (site visité le 30 août 2022).
14. Schneier M, Razdan S, Miller AM, Briceno ME, Barua S. Current technologies to endotoxin detection and removal for biopharmaceutical purification. Biotechnol Bioeng 2020;117: 2588–609.

15. GenScript. ToxinSensorTM endotoxin detection system user manual: version 12172010. 2019.
16. United States Pharmacopeia. Pharmaceutical compounding–Sterile preparations (Bacterial endotoxins test – chapter 85): USP-NF. 2012.
17. Yamamoto A, Ochiai M, Fujiwara H, Asakawa S, Ichinohe K, Kataoka M et coll. Evaluation of the applicability of the bacterial endotoxin test to antibiotic products. Biologicals 2000;28:155–67.

18. John B, Kamaruzzaman K, Jalal K, Zaleha K. TAL - A source of bacterial endotoxin detector in liquid biological samples. International Food Res J 2012;19:423–5.
19. LONZA. An introduction to bacterial endotoxin testing (2020). [en ligne] https://bioscience.lonza.com/lonza_bs/CA/en/endotoxin-testing (site visité le 30 août 2022).
20. Charles Rivers. LAL test reagents and accessories (2020). [en ligne] https://www.criver.com/products-services/qc-microbial-solutions/endotoxin-testing/lal-reagents-accessories?region=3611 (site visité le 30 août 2022).
21. GenScript. Endotoxin assay kits (2020). [en ligne] https://www.genscript.com/endotoxin_assay_kits.html (site visité le 30 août 2022).
22. Associates of Cape Code. LAL reagents (2020). [en ligne] https://www.acciusa.com/products-and-services/bet-products/lal-reagents/ (site visité le 30 août 2022).
23. Hurley JC. Endotoxemia: methods of detection and clinical correlates. Clin Microbiol Rev 1995;8:268–92.


24. Jackie J, Lau WK, Feng HT, Li SFY. Detection of endotoxins: from inferring the responses of biological hosts to the direct chemical analysis of lipopolysaccharides. Crit Rev Anal Chem 2019;49:126–37.

25. Sakai H, Hisamoto S, Fukutomi I, Sou K, Takeoka S, Tsuchida E. Detection of lipopolysaccharide in hemoglobin-vesicles by Limulus amebocyte lysate test with kinetic–turbidimetric gel clotting analysis and pretreatment of surfactant. J Pharm Sci 2004;93:310–21.

26. Schindler S, Aulock S, Daneshian M, Hartung T. Development, validation and applications of the monocyte activation test for pyrogens based on human whole blood. ALTEX 2009;26:265–77.

27. Bolden J, Smith K. Application of recombinant factor C reagent for the detection of bacterial endotoxins in pharmaceutical products. PDA J Pharm Sci Technol 2017;71:405–12.

28. European Directorate for the Quality of Medicines and Healthcare. EDQM revises 5.1.10. guidelines for using the test for bacterial endotoxins (2014). [en ligne] https://www.gmp-compliance.org/gmp-news/edqm-revises-5-1-10-guidelines-for-using-the-test-for-bacterial-endotoxins (site visité le 30 août 2022).
29. Organisation mondiale de la Santé. Report of an international collaborative study to evaluate three preparations of endotoxin for their suitability to serve as the third international standard for bacterial endotoxin (2012). [en ligne] https://apps.who.int/iris/bitstream/handle/10665/96606/WHO_BS_2012.2193_eng.pdf?sequence=1&isAllowed=y (site visité le 30 août 2022).
Pour toute correspondance: Marc-Olivier Pilon, Centre de pharmacogénomique, Institut de Cardiologie de Montréal, 5000, rue Bélanger, Montréal (Québec) H1T 1C8, CANADA; Téléphone: 514 376-3330; Courriel: marc-olivier.pilon@umontréal.ca
(Return to Top)
PHARMACTUEL, Vol. 55, No. 4, 2022