Julie Bureau, Pharm.D., M.Sc.1,2, Julie Racicot, B.Pharm., M.Sc.3,4,5, Éric Boivin, Pharm.D., M.Sc., Ph.D.3, Chantale Simard, B.Pharm., M.Sc., Ph.D.6,7
Reçu le 20 décembre 2021: Accepté après révision par les pairs le 6 février 2022
Résumé
Objectif : Établir les critères de vulnérabilité permettant de cibler les patients nécessitant une histoire pharmacothérapeutique par le pharmacien après leur admission à l’Institut universitaire de cardiologie et de pneumologie de Québec–Université Laval. Les critères d’évaluation secondaire étaient de déterminer les problèmes pharmacothérapeutiques issus de l’histoire et d’en analyser les répercussions cliniques.
Méthode : En complément au bilan comparatif des médicaments, des histoires pharmacothérapeutiques ont été menées auprès d’un nombre de patients hospitalisés, sur une période d’un mois, afin de détecter des problèmes pharmacothérapeutiques qui ont été classés selon leur nature et leurs répercussions cliniques.
Résultats : Cent quarante-cinq histoires pharmacothérapeutiques ont eu lieu et ont permis de détecter 85 problèmes, dont 55 avaient peu d’effets, 28 avaient un effet important et deux avaient un effet majeur. Les problèmes les plus fréquents étaient les doses trop élevées, les omissions et les inobservances. Le nombre de médicaments en vente libre ou au besoin que prenait le patient et la gestion autonome des médicaments constituaient des facteurs de vulnérabilité lors de la détection de problèmes médicamenteux.
Conclusion : Les critères de vulnérabilité que nous avons trouvés et les répercussions des problèmes pharmacothérapeutiques détectés ne justifient pas des histoires exhaustives pour tous les patients. Toutefois, l’étude a permis d’établir quels patients en bénéficieraient le plus dans un contexte où le bilan comparatif des médicaments est fait pour tous les patients et que l’offre de soins permet de cibler les patients les plus vulnérables de manière à prendre en charge la majorité des problèmes ayant un impact significatif ou majeur.
Mots-clés : Bilan comparatif des médicaments, histoire pharmacothérapeutique, pharmacie clinique, priorisation, problème pharmacothérapeutique
Abstract
Objective : To determine vulnerability criteria for patients requiring a pharmacotherapeutic history by a pharmacist following their admission to the Institut de cardiologie et de pneumologie de Québec-Université Laval. The secondary objectives were to identify the pharmacotherapeutic problems present in the history and to determine their clinical impact.
Method : In addition to medication reconciliation, histories were conducted in a number of hospitalized patients over a one-month period to identify any pharmacotherapeutic problems, which were classified according to their nature and clinical impact.
Results : One hundred and forty-five histories were taken, in which 84 problems were identified. Of these, 55 were having a minor impact, 28 a significant impact, and 2 a major impact. The most common problems were too-high doses, missed doses, and noncompliance. The number of over-the-counter or as-needed medications and the self-management of medications were vulnerability factors that emerged when identifying medication-related problems.
Conclusion : The vulnerability criteria determined in this study and the impact of the pharmacotherapeutic problems identified do not warrant taking a thorough history in all patients. However, the study does help identify patients who would benefit the most in a context where medication reconciliation is established for all patients and where there is an offer of care for the most vulnerable patients, so most problems with a significant or major impact are already being managed.
Keywords : Clinical pharmacy, medication reconciliation, pharmacotherapeutic history, pharmacotherapeutic problem, prioritization
L’histoire pharmacothérapeutique est le processus par lequel une entrevue est menée avec le patient afin d’obtenir, entre autres, des informations précises sur ses médicaments actuels, les essais thérapeutiques antérieurs, les habitudes de vie, les allergies, les intolérances, l’adhésion au traitement, l’efficacité des traitements et la tolérance du patient à ces traitements. Ce processus permet au pharmacien d’évaluer adéquatement le traitement médicamenteux des patients afin, d’une part, de détecter des problèmes pharmacothérapeutiques et, d’autre part, d’établir le meilleur schéma thérapeutique possible pour faire la conciliation médicamenteuse appelée « bilan comparatif des médicaments »1–4.
Le meilleur schéma thérapeutique possible est un « portrait instantané » de l’utilisation actuelle des médicaments courants du patient. On l’obtient « à l’aide d’un processus systématique d’entrevue avec les patients et leur famille et de l’analyse d’au moins une autre source de renseignements fiables dans le but d’obtenir et de valider tous les médicaments que prend le patient (avec ou sans ordonnance) »4. Par la suite, le bilan comparatif des médicaments permet de comparer les médicaments qui sont prescrits à l’hôpital à ceux que prend le patient à domicile et de détecter les divergences non intentionnelles3,4. Depuis 2005, Agrément Canada a inclus le bilan comparatif des médicaments dans les pratiques organisationnelles requises afin de limiter le risque d’erreurs médicamenteuses et, ainsi, améliorer la sécurité des patients5. En effet, la littérature contient de nombreux exemples du rôle important que jouent les pharmaciens dans la prévention des erreurs médicamenteuses grâce à l’histoire6–10.
L’histoire constitue donc un processus qui va au-delà du meilleur schéma thérapeutique possible et du bilan comparatif des médicaments. Elle permet de collecter davantage de données dans le but de détecter les problèmes pharmacothérapeutiques. C’est une activité importante dans la prise en charge globale du patient par le pharmacien. Toutefois, les ressources limitées et la complexité des soins empêchent actuellement les pharmaciens de l’effectuer pour tous les patients. Ainsi, conformément aux recommandations du Vérificateur général du Québec et du ministère de la Santé et des Services sociaux (MSSS) visant l’optimisation des soins pharmaceutiques, l’Institut universitaire de cardiologie et de pneumologie de Québec–Université Laval (IUCPQ–UL) a conçu, en 2016, une offre de soins pour cibler les patients les plus vulnérables que les pharmaciens doivent prendre en charge de façon systématique ou prioritaire11–13.
L’histoire complète n’est donc pas faite pour tous les patients. Les pharmaciens recourent plutôt à des questionnaires dirigés au besoin pour produire le meilleur schéma thérapeutique possible. En contrepartie, le bilan comparatif des médicaments est effectué pour presque tous les patients afin de cibler ceux nécessitant une intervention systématique ou prioritaire et de détecter certains problèmes médicamenteux. Ce processus est possible grâce à la participation de plusieurs intervenants. Les assistants techniques en pharmacie produisent le bilan comparatif des médicaments à partir des informations du Dossier santé Québec (DSQ), puis les pharmaciens valident les informations et questionnent au besoin les patients pour éclaircir certains points. Ensuite, les infirmières interrogent les patients sur leur consommation de médicaments en vente libre, de produits de santé naturels et de médicaments pris dans le cadre d’une étude clinique. Enfin, les médecins questionnent à leur tour les patients sur leur prise réelle d’insuline et de warfarine, le cas échéant.
Selon deux audits internes ayant eu lieu respectivement en 2018 et en 2020 à l’IUCPQ–UL, dont l’objectif était d’évaluer le processus du bilan comparatif des médicaments pour les patients hospitalisés, les pharmaciens cliniciens interrogeaient 44 % des patients en 2018 contre 50 % en 2020 afin de vérifier des divergences auprès des usagers. De plus, ces audits ont mis en évidence que les infirmières questionnaient 72 % patients en 2018 contre 64 % en 2020 sur l’usage de médicaments en vente libre, des produits de santé naturels et de médicaments pris dans le cadre d’une étude clinique. Cela dit, les résultats de l’étude de Boivin et coll. ont montré que les bilans comparatifs des médicaments effectués à partir du DSQ produisaient généralement des portraits médicamenteux fidèles pour les patients de l’IUCPQ–UL et que les divergences résiduelles détectées par un questionnaire effectué par un assistant technique auraient eu un effet clinique non significatif14.
Comme nous l’avons mentionné précédemment, le pharmacien fait une histoire exhaustive auprès de peu de patients de l’IUCPQ–UL en raison du bilan comparatif des médicaments en place. Toutefois, il existe des critères pour l’ajout d’une histoire dans l’offre de soins, mais il est difficile de les trouver à l’aide de l’outil de priorisation électronique intégré au logiciel GesphaRx qu’emploient les pharmaciens de l’IUCPQ–UL. Ils sont donc peu utilisés. On peut ainsi se demander si certains éléments importants qui auraient pu être détectés à l’histoire ne sont pas manquants. Ce questionnement a été soulevé notamment à la suite d’une étude menée par Racicot et coll. à l’IUCPQ–UL où le modèle de soins classiques sans priorisation des patients était comparé à la nouvelle offre de soins14. Parmi les interventions pharmaceutiques ayant un effet clinique important qui n’étaient pas détectées par la nouvelle offre de soins, 27 % étaient issues de l’histoire. De fait, plusieurs histoires faites selon le modèle classique n’auraient pas eu lieu avec le modèle actuel de hiérarchisation des soins pharmaceutiques. L’objectif général de la présente étude est donc de déterminer chez quels patients admis à l’IUCPQ–UL il serait pertinent d’effectuer une histoire complète et aussi d’évaluer sa valeur ajoutée dans le contexte où le bilan comparatif des médicaments est effectué systématiquement.
Plusieurs études ont révélé que les points de transition (admissions, transferts, départs) des soins hospitaliers étaient particulièrement susceptibles de conduire à des erreurs médicamenteuses8,9,14,15–18. Plusieurs de ces erreurs découlent de divergences entre la consommation de médicaments du patient avant son admission et les médicaments prescrits à l’hôpital. Il s’agit généralement de divergences par omission7–9,14,18–20. Actuellement, la tendance dans les hôpitaux est de consulter le profil de la pharmacie ou le DSQ pour rédiger les ordonnances à l’admission, car ces outils sont considérés comme les plus représentatifs du profil médicamenteux du patient14,21,22. Les améliorations apportées au DSQ dans les dernières années ont grandement augmenté sa fiabilité, en plus d’offrir désormais la possibilité de voir les médicaments en attente, ceux de l’annexe II, les traitements terminés, les fréquences et dates de renouvellement ainsi que les médicaments servis par toutes les pharmacies. Toutefois, le profil ainsi que le DSQ ne précisent pas la consommation réelle du patient. L’histoire constitue donc le moyen le plus fiable d’obtenir cette information4,5,8,16,21. De plus, le profil et le DSQ ne montrent pas les changements qu’aurait effectués verbalement le prescripteur ou le patient en raison d’effets indésirables. En outre, certaines informations sur la prise d’un médicament dans le cadre d’une étude clinique, du programme d’accès spécial ou sous forme d’échantillons peuvent être manquantes.
Une étude de Lee et coll. a comparé la précision d’une histoire obtenue à l’aide d’un outil équivalent à celui du DSQ utilisé seul à une histoire obtenue à l’aide du même outil électronique en complément d’une entrevue avec le patient8. Ils ont observé que la combinaison des deux méthodes avait mené à une meilleure détection des divergences, ce qui s’explique notamment par le fait que plusieurs patients ont une consommation différente de celle de l’ordonnance. Or, ce résultat semble indiquer que même quand la liste des médicaments est à jour, la seule manière d’obtenir l’information sur la consommation véritable du patient est de l’interroger. Boivin et coll. ont d’ailleurs constaté la même chose14.
Plusieurs études montrent que le risque de découvrir des divergences augmente avec le nombre de médicaments consommés à domicile, soit à partir de cinq médicaments7,9,14,15,17–19,23–26. L’âge avancé (plus de 65 à 70 ans) représente une autre variable qui accroît le risque de divergences médicamenteuses15,18,23,24,26. Toutefois, il est possible que ce ne soit pas tant l’âge qui augmente le risque que le fait que les personnes âgées ont généralement plus de maladies concomitantes et, conséquemment, plus de médicaments à leur profil13. D’ailleurs, deux autres études ont observé qu’un âge plus avancé constituait en fait un facteur protecteur, probablement en raison des suivis externes plus serrés et de l’aide que ces personnes reçoivent pour la gestion de leurs médicaments16,27. Parmi les critères de vulnérabilité qui ressortent de la littérature comme risque potentiel de divergences accrues, il y a entre autres la barrière de la langue, le faible degré de scolarité, le nombre élevé de maladies concomitantes, les changements récents aux médicaments, la gestion autonome des médicaments, l’utilisation de médicaments « au besoin », les multiples visites médicales extrahospitalières dans la dernière année et les multiples prescripteurs au dossier9,14,17,26,28.
Au-delà des divergences médicamenteuses, il est important de considérer l’effet clinique qui en découle. L’étude de Boivin et coll. a révélé que les divergences décelées uniquement à l’histoire avaient un effet clinique faible14. Dans l’étude de Gleason et coll., 35,6 % des divergences médicamenteuses étaient vraisemblablement peu susceptibles de causer des dommages20. Inversement, 62,8 % des divergences auraient pu occasionner des dommages temporaires ou nécessiter une intervention ou un suivi plus étroit afin d’éviter des dommages. Par ailleurs, seulement 1,3 % des divergences avaient le potentiel de prolonger l’hospitalisation. Quant à Karaoui et coll., ils ont montré que 63 % des divergences n’avaient pas d’effet clinique important, que 36 % avaient un effet clinique important et que 1 % aurait pu avoir un effet sérieux19. Malgré de légères variations, plusieurs études mentionnent des pourcentages semblables7,9,18.
Le critère d’évaluation principal de cette étude était de déterminer les critères de vulnérabilité des patients nécessitant une histoire par le pharmacien après leur admission à l’IUCPQ–UL. Les deux critères d’évaluation secondaires étaient de déterminer les problèmes pharmacothérapeutiques découverts à l’histoire qui ne l’auraient pas été autrement et d’en établir l’effet clinique.
Ce projet est une étude descriptive transversale. La collecte de données s’est faite en deux volets. Le premier, effectué de manière rétrospective, consistait à décrire les patients inclus dans l’étude afin d’établir certains critères de vulnérabilité. Le deuxième, effectué de manière prospective sur ces mêmes patients, consistait à mener l’histoire dans un contexte clinique afin de détecter des problèmes pharmacothérapeutiques.
La collecte de données s’est déroulée du 3 mai au 3 juin 2021, du mardi au vendredi, pour un total de 20 jours de collecte. La population à l’étude correspondait aux patients admis à l’IUCPQ–UL par l’urgence chez qui le bilan comparatif des médicaments avait eu lieu. Nous avons exclu les patients : 1) de l’urgence qui n’étaient pas hospitalisés, 2) pour lesquels le bilan comparatif des médicaments n’avait pas encore été fait, 3) pour lesquels le congé était signé, 4) qui refusaient l’histoire, 5) qui étaient hospitalisés aux soins intensifs et, 4) qui étaient atteints de la COVID-19. Une liste des patients admissibles hospitalisés par l’urgence a été produite à partir du logiciel SIURGE afin de procéder à la sélection aléatoire des patients chez qui une histoire serait effectuée.
Dans le premier volet de la collecte de données, les différentes variables servant à décrire les patients de l’étude étaient divisées en trois catégories liées : 1) aux patients, 2) à certains problèmes médicaux et, 3) aux traitements pharmacologiques. Le logiciel GesphaRx, le DSQ, le dossier médical et le dossier patient électronique (DPE) ont été consultés afin d’obtenir ces informations.
Dans le deuxième volet de la collecte de données, l’histoire a été faite auprès du patient, de la famille ou d’un proche aidant, puis les problèmes liés aux médicaments découverts et leurs répercussions cliniques ont été classés par catégorie selon leur nature : 1) dose trop élevée d’un médicament à indice thérapeutique étroit, conformément à l’offre de soins, 2) dose trop élevée d’un médicament à indice thérapeutique non étroit, 3) dose trop faible d’un médicament, 4) voie d’administration ou préparation inappropriée, 5) précaution ou contre-indication à l’emploi, 6) interaction médicamenteuse, 7) prise d’un médicament sans indication valable, 8) omission d’un médicament, 9) heure d’administration inadéquate, 10) allergie ou intolérance ou 11) inobservance. Ensuite, les problèmes médicamenteux repérés étaient classés selon leur effet clinique présumé par le pharmacien, soit léger, important ou majeur13. Cette classification est reprise de celle de Racicot et coll., utilisée pour décrire les interventions du pharmacien, qui elle a été adaptée de l’échelle de Lukes et Overhages13,15,29. La nature et l’effet clinique des problèmes pharmacothérapeutiques ont été déterminés par la pharmacienne résidente en collaboration avec les superviseurs hospitaliers.
Dans le deuxième volet, la « liste des médicaments à domicile (ou MSTP) », un outil de collecte accessible sur demande dans Cristal-Net, a été employée pour mener l’entrevue avec les patients. Elle contient, entre autres, les données d’identification du patient, son poids, sa taille, ses habitudes de vie, ses allergies et intolérances et la liste à jour de ses médicaments issue du DSQ, dont les médicaments prescrits et ceux de l’annexe II. Il comporte également une section pour inscrire les médicaments en vente libre et les produits de santé naturels pris par le patient et toutes les autres informations complémentaires.
L’analyse des données a été faite à l’aide du logiciel SAS. Les variables qualitatives ont été exprimées en pourcentages et en proportions. Elles ont servi à décrire, entre autres, les problèmes pharmacothérapeutiques, les répercussions cliniques des interventions effectuées et plusieurs variables liées aux patients, aux traitements et aux problèmes médicaux. Le test exact de Fisher a servi à déterminer l’association entre les variables qualitatives et la présence de problèmes pharmacothérapeutiques. Les variables quantitatives, quant à elles, ont été exprimées par des mesures de tendances centrales, telles que la moyenne et la médiane. Elles ont servi à décrire le nombre d’interventions effectuées ainsi que certaines données démographiques des patients, comme l’âge, le poids, la taille et le nombre de médicaments. Le test t de Student a été utilisé pour les variables de nature quantitative afin d’établir la différence entre les groupes avec et sans problèmes pharmacothérapeutiques.
Le projet de recherche a été soumis à la Direction des services professionnels et au Comité d’éthique de la recherche de l’IUCPQ–UL. La confidentialité des données des patients a été assurée par la création d’une banque de données dénominalisées protégée par mot de passe. Les patients n’ont pas été exposés à des risques cliniques puisque l’équipe traitante était avisée des divergences et des problèmes pharmacothérapeutiques, le cas échéant.
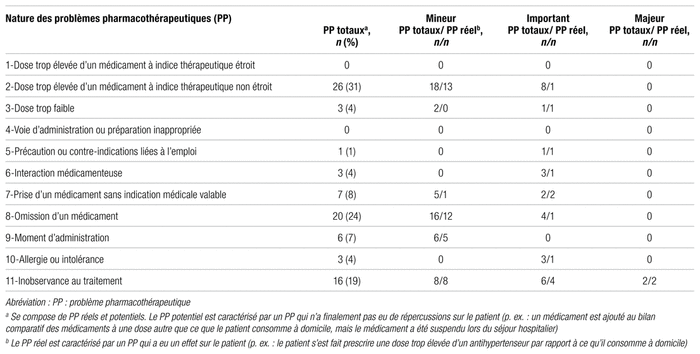
Le tableau I présente les problèmes pharmacothérapeutiques caractérisés selon leur nature. Au total, 85 problèmes ont été détectés auprès de 61 des 145 patients à l’étude (42 %). Les catégories les plus fréquentes étaient les doses trop élevées de médicaments à indice thérapeutique non étroit (31 %), les omissions médicamenteuses (24 %) et les inobservances aux traitements (19 %).
Tableau I Nature des problèmes pharmacothérapeutiques détectés à l’histoire et leurs répercussions cliniques

La figure 1 montre la répartition des problèmes selon l’importance des répercussions cliniques et selon que ces répercussions sont réelles ou potentielles. La majorité des problèmes médicamenteux détectés avaient une influence mineure (55/85), une proportion plus faible de problèmes ayant une influence importante (28/85) et seulement deux problèmes ayant une influence majeure.
|
| ||
|
Figure 1 Répartition des problèmes pharmacothérapeutiques selon leur degré de répercussions cliniques (mineur, important et majeur) et leur caractère réel ou potentiel | ||
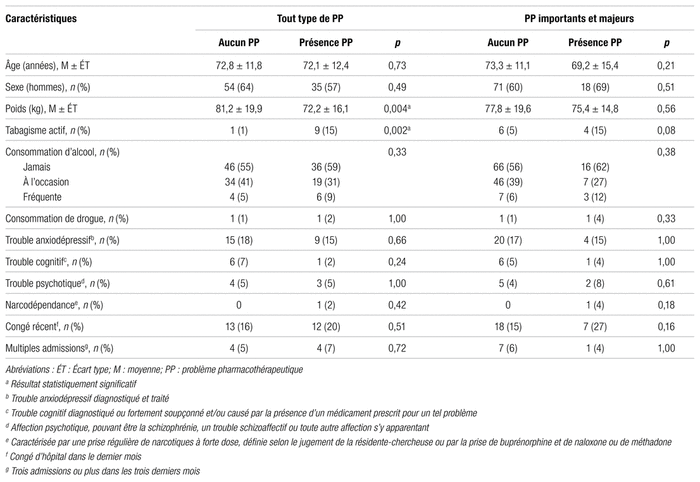
Le tableau II présente les caractéristiques des patients à l’étude. Les deux groupes de patients (c.-à-d., ceux ayant des problèmes pharmacothérapeutiques et ceux n’en ayant pas, étaient comparables, sauf pour le poids des patients ayant des problèmes allant de mineurs à majeurs (72 kg vs 81 kg, p = 0,004) et pour la consommation de tabac (9 patients vs 1, p = 0,002). D’autres caractéristiques des patients à l’étude peuvent être consultées dans l’annexe. Aucune différence significative entre les deux groupes de patients n’y a été trouvée.
Tableau II Caractéristiques des patients inclus dans l’étude
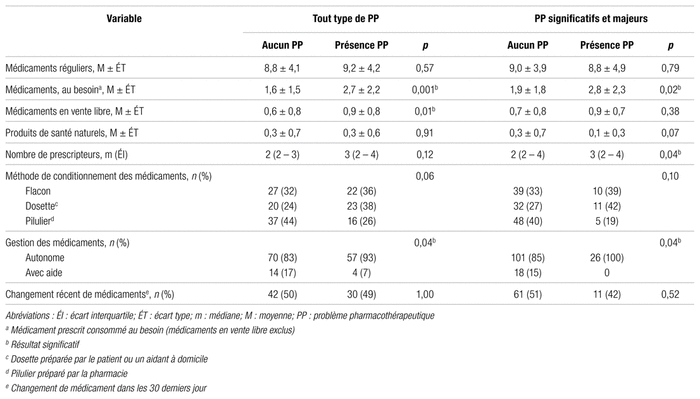
Le tableau III présente certaines caractéristiques des traitements médicamenteux des patients. La différence entre le nombre de médicaments consommés au besoin est significative entre les groupes ayant des problèmes pharmacothérapeutiques et ceux n’en ayant pas (2,7 vs 1,6, p = 0,001). Une différence significative a aussi été trouvée entre ces deux groupes pour les problèmes significatifs et majeurs seulement (2,8 vs 1,9, p = 0,02). La différence dans le nombre de médicaments consommés en vente libre est significative pour tous les types de répercussions, soit de mineurs à majeurs (0,6 vs 0,9, p = 0,01). Par contre, elle n’est plus significative pour les problèmes importants et majeurs seulement. La méthode de conditionnement des médicaments a également entraîné une différence significative pour les problèmes aux répercussions mineures à majeures (p = 0,06). Les patients dont les médicaments étaient servis en flacon et en dosette (préparé par le patient à domicile) présentaient plus de problèmes pharmacothérapeutiques (73,8 % vs 55,9 %) que ceux ayant utilisé des piluliers (préparés par la pharmacie) (26,2 % vs 44,1 %). Par ailleurs, un nombre significativement (p = 0,04) plus élevé de patients faisant eux-mêmes la gestion de leurs médicaments à domicile présentaient des problèmes médicamenteux ayant des répercussions mineures à majeures (93,4 % vs 83,3 %) par rapport à ceux qui recevaient de l’aide (6,6 % vs 16,7 %). La différence significative se maintient lorsque l’on considère les problèmes importants et majeurs seulement (p = 0,04). Enfin, le nombre de prescripteurs au dossier entraîne aussi une différence significative pour les problèmes aux répercussions importantes et majeures (2 vs 3, p = 0,04). Le tableau dans l’annexe décrit brièvement les problèmes pharmacothérapeutiques détectés à l’histoire.
Tableau III Caractéristiques des traitements pharmacologiques des patients
La présente étude décrit les problèmes pharmacothérapeutiques ayant été détectés par une pharmacienne résidente à l’histoire des patients. Cette histoire visait essentiellement à établir les répercussions cliniques des problèmes soulevés. Cette étape était complémentaire au bilan comparatif des médicaments standard. Au terme de l’histoire, on constate que la majorité des problèmes détectés n’avaient qu’un effet mineur et que seulement une faible proportion avait un effet important et majeur. Pour plusieurs de ces problèmes importants, les répercussions n’étaient que potentielles. D’ailleurs, l’étude de Mazhar et coll. parvenait à une conclusion similaire, soit que la moitié des erreurs détectées auraient pu nuire au patient, mais que le nombre d’erreurs ayant un effet majeur était faible (17,7 % seulement)18. Selon Lee et coll., jusqu’à 33 % des erreurs médicamenteuses détectées à l’histoire auraient potentiellement mené à des dommages modérés ou graves pour les patients8.
D’emblée, les problèmes pharmacothérapeutiques les plus fréquents dans la présente étude étaient, dans l’ordre, les doses trop élevées de médicaments à indice thérapeutique non étroit, les omissions médicamenteuses et les inobservances intentionnelles ou non. Ces résultats diffèrent de ceux de la majorité des études similaires, qui concluaient que les omissions médicamenteuses représentaient la divergence la plus fréquente6–8,14,15,19. Dans le cadre de notre étude, la consultation du DSQ pour rédiger les ordonnances à l’admission et effectuer le bilan comparatif des médicaments pourrait expliquer pourquoi nos conclusions diffèrent de celles des autres études. Toutefois, les résultats de l’étude de Van der Luit et coll. vont dans le même sens que les nôtres, à savoir que l’erreur de dose est la plus fréquente et que les omissions médicamenteuses s’inscrivent en seconde place23. Les auteurs expliquent cette incohérence par une différence méthodologique puisqu’ils considéraient les omissions uniquement si la divergence était acceptée par le prescripteur, de sorte que seulement les omissions non intentionnelles étaient comptabilisées.
Comme nous l’avons mentionné précédemment, les doses trop élevées de médicaments à indice thérapeutique non étroit représentaient le problème pharmacothérapeutique le plus fréquent de notre étude, soit 26 des problèmes détectés, dont 18 ont eu un effet mineur et huit, un effet important. Ce type d’erreur s’observait lorsque de nouveaux médicaments étaient prescrits en dose croissante ou encore lorsque les médicaments pouvaient être ajustés selon les symptômes du patient (p. ex. : laxatifs, somnifères et analgésiques). Les médicaments prescrits au besoin constituaient également une source d’erreurs puisque plusieurs patients en faisaient une consommation inappropriée. Néanmoins, il est rassurant de constater que la majorité des problèmes pharmacothérapeutiques liés aux doses trop élevées avaient seulement des répercussions mineures et que ceux ayant un effet important avaient déjà été découverts par l’équipe médicale ou par le pharmacien de l’unité de soins préalablement à l’histoire pharmacothérapeutique. Une attention particulière devrait tout de même être apportée aux nouveaux médicaments, à ceux prescrits en dose croissante et à ceux pouvant être ajustés par le patient.
Ensuite, les omissions médicamenteuses comptaient pour 20 des problèmes détectés, dont 16 avaient un effet mineur et quatre, un effet important. À noter que seulement une des omissions significatives a eu un effet réel, chez une patiente qui prenait la quétiapine (25 mg) de son conjoint contre son insomnie. Autrement, la majorité des omissions concernaient des médicaments consommés en vente libre et des produits de santé naturels, comme les vitamines et minéraux et les laxatifs. La durée moyenne du séjour à l’IUCPQ–UL étant très courte, soit de six ou sept jours, les interruptions de traitement avaient généralement un effet mineur. Par ailleurs, le transit intestinal des patients était bien évalué par le personnel infirmier, qui pouvait au besoin appliquer des ordonnances collectives pour commencer les laxatifs.
Enfin, les cas d’inobservance aux traitements comptaient pour presque un cinquième des problèmes pharmacothérapeutiques recensés dans l’étude, dont six ont eu un effet important et deux, un effet majeur. La première situation concernait un patient qui prenait des anticoagulants pour une fibrillation auriculaire et qui avait réduit sa dose d’apixaban en raison d’ecchymoses. La deuxième concernait un patient qui n’avait pas fait exécuter sa prescription de clopidogrel après la pose de tuteurs percutanés (tableau en annexe). Ces exemples montrent que malgré la pluralité d’informations dans le DSQ sur les dates et les fréquences de renouvellement, l’histoire vient préciser davantage la consommation réelle du patient. C’est d’ailleurs un des constats soulevés dans l’étude de Lee et coll., qui ont montré que malgré l’utilisation d’outils électroniques fiables pour rédiger les ordonnances d’admission, les divergences détectées étaient plus nombreuses lorsque le bilan comparatif était effectué conjointement avec l’histoire, comparativement à l’outil électronique seul8.
Outre les trois problèmes les plus fréquents décrits précédemment, d’autres problèmes pharmacothérapeutiques ont été recensés, notamment par rapport au moment d’administration des médicaments. En effet, les médicaments dont l’administration doit se faire à intervalle particulier (de façon hebdomadaire, par exemple) représentaient souvent une cause de divergence. À titre d’exemple, si un patient était admis à l’hôpital un mardi, la journée d’administration de tous ses médicaments consommés une fois par semaine (bisphosphonates, vitamine D, etc.) était systématiquement inscrite le lundi, soit la journée avant l’admission. Cette méthode est utilisée à l’IUCPQ–UL afin de s’assurer que les patients ne reçoivent pas des doses en double. Les répercussions de ce type de problème étaient néanmoins mineures, d’une part parce que la majorité des médicaments en cause n’entraînaient pas de complications majeures malgré les retards d’administration et, d’autre part, en raison de la courte durée d’hospitalisation. En contrepartie, pour certains médicaments, comme le méthotrexate et les agents biologiques (évolocumab, alirocumab, étanercept, etc.), une modification du moment d’administration pourrait porter préjudice au patient. Ainsi, les médicaments comportant un risque plus élevé sont ciblés dans l’offre de soins, et la pratique locale fait en sorte que les pharmaciens des unités de soins valident systématiquement la journée réelle d’administration auprès du patient.
Parallèlement aux problèmes pharmacothérapeutiques recensés par la pharmacienne résidente, notre projet visait également à déterminer certains critères de vulnérabilité justifiant l’histoire. D’abord, à la lumière des résultats, on peut voir que la consommation de médicaments en vente libre était plus importante chez les patients présentant des problèmes médicamenteux et que le résultat était significatif lorsque les trois degrés de répercussions étaient confondus. Ce constat n’est pas surprenant étant donné que plusieurs problèmes découlaient d’omissions médicamenteuses. Toutefois, cette corrélation n’était plus significative lorsque les divergences mineures étaient exclues. Comme nous l’avons déjà mentionné, il est de la responsabilité du personnel infirmier d’obtenir l’information concernant la consommation des produits en vente libre, ce qui n’est pas toujours fait. Par ailleurs, même quand l’information est obtenue, elle n’est pas nécessairement transmise au pharmacien. Une solution pour remédier à ce problème serait d’ajouter une section « médicaments en vente libre, produits de santé naturels et médicaments pris dans le cadre d’une étude clinique » dans la partie supérieure des feuilles d’ordonnance. L’information serait alors relevée par les assistants techniques en pharmacie et ajoutée au bilan comparatif des médicaments sans ralentir la chaîne de travail. Les assistants pourraient aussi consulter les données consignées par l’infirmière, à condition que l’accès à ces informations leur soit accordé à l’avenir.
Le nombre de médicaments pris « au besoin » était également associé à une différence significative, peu importe le degré des répercussions liées aux problèmes pharmacothérapeutiques. En effet, les patients ayant plus de médicaments « au besoin » avaient une propension à présenter davantage de divergences. Une des explications possibles est que la prise « au besoin » donnait la liberté au patient de moduler sa consommation, pas toujours adéquatement. En effet, certains patients avaient recours à de plus fortes doses que nécessaire, et d’autres, à des doses trop faibles.
Par ailleurs, les patients dont les médicaments étaient servis en flacon et en dosette, ainsi que ceux qui géraient eux-mêmes leurs médicaments à domicile, sans aide, ont présenté davantage de problèmes médicamenteux, contrairement à ceux qui utilisaient un pilulier ou qui avaient de l’aide pour la prise de leurs médicaments à domicile. Ces résultats pourraient s’expliquer par le fait que les patients qui géraient eux-mêmes leurs médicaments pouvaient adapter leur traitement selon leurs symptômes.
Le tabagisme actif était également associé à un risque plus élevé de problèmes pharmacothérapeutiques. Toutefois, comme l’échantillon était très limité (seulement 10 fumeurs actifs), cette différence pouvait être due au hasard. D’ailleurs, aucune intervention spécifiquement liée au tabac n’a été effectuée au cours de l’étude, et les problèmes détectés ne suivaient aucune tendance particulière. Il est important de souligner que la fumée du tabac peut être à l’origine d’interactions importantes par l’induction de l’isoenzyme CYP1A2, notamment avec les antipsychotiques (p. ex. : clozapine et olanzapine), ce qui n’était pas le cas des patients participant à l’étude30,31. Ainsi, le tabac ne constituait pas un facteur de vulnérabilité dans la présente étude, mais pourrait l’être dans un autre contexte de soin. Comme le tabac, le poids des patients était aussi associé à une différence statistiquement significative, un poids plus faible étant associé à un taux supérieur de problèmes pharmacothérapeutiques. Par contre, cette différence n’était pas cliniquement significative. En effet, le poids ne se situait pas dans des valeurs extrêmes de petits poids ou d’obésité, lesquels seraient d’ailleurs ciblés dans l’offre de soins de l’IUCPQ–UL.
À l’instar du poids et du tabagisme actif, le nombre de prescripteurs était également associé, de manière significative, à plus de problèmes pharmacothérapeutiques, sans toutefois que ce résultat soit cliniquement important. D’ailleurs, certains patients à l’étude avaient sept différents prescripteurs, et aucun problème n’a été détecté à l’histoire. Nous avions prévu que ce facteur allait être un critère de vulnérabilité, mais nous n’avons pu le mettre en évidence dans cette étude.
Enfin, nos résultats n’ont pas montré que les troubles cognitifs étaient liés à une plus grande propension aux problèmes pharmacothérapeutiques. Toutefois, il est important de préciser, d’une part, que l’échantillon très limité rend difficile l’obtention de conclusions robustes et, d’autre part, que les patients atteints de troubles cognitifs diagnostiqués ou fortement soupçonnés ne géraient pas leurs médicaments de manière autonome. Pour les patients ayant des troubles cognitifs légers non diagnostiqués, les conclusions pourraient s’avérer différentes, mais cette information n’a pas été collectée aux fins de la présente étude.
En somme, cette étude permet de recenser certains critères objectifs dans le but de faciliter l’identification des patients chez qui il serait pertinent d’effectuer une histoire pharmacothérapeutique. Afin d’aider les pharmaciens à cibler ces patients, les assistants techniques en pharmacie pourraient, au moment de faire le bilan comparatif des médicaments, ajouter des informations additionnelles, à partir des données du DSQ, dont la méthode d’administration des médicaments, les nouveaux médicaments, ceux qui sont prescrits en dose croissante, ceux que le patient peut ajuster lui-même (autres que les médicaments « au besoin »), ainsi que ceux pour lesquels les renouvellements sont souvent devancés ou retardés. Enfin, les informations concernant les médicaments en vente libre et les produits de santé naturels recueillies par le personnel infirmier devraient être ajoutées au bilan comparatif des médicaments. Elles pourraient un jour l’être dans GesphaRx afin d’être intégrées à l’outil de priorisation électronique.
La pharmacienne résidente a constaté quelques limites à notre étude. Premièrement, un risque de biais d’information était présent, car la qualité de l’histoire dépendait de son habileté à obtenir les informations des patients, de la famille ou des soignants. De plus, étant donné le devis prospectif, la pharmacienne résidente connaissait les objectifs de l’étude. Elle pouvait ainsi orienter la collecte de données, de sorte qu’elle effectuait possiblement une histoire plus approfondie. Ensuite, un autre biais concernait la constatation et la classification des problèmes pharmacothérapeutiques, ce qui nécessitait l’interprétation des données et un certain jugement clinique. Enfin, un biais découlait de l’échelle d’évaluation des répercussions cliniques utilisée dans l’étude de Racicot et coll. qui n’a pas été validée13. Toutefois, cette échelle s’inspirait de celle de Overhage et Lukes qui, elle, a été validée29.
En ce qui concerne la validité externe, les résultats de notre étude pourraient ne pas s’étendre aux autres hôpitaux du Québec étant donné le processus du bilan comparatif des médicaments, l’offre de soins pharmaceutiques bien implantée, la patientèle et la mission très spécifiques de l’IUCPQ–UL.
Pour terminer, certaines forces de l’étude ont été constatées. Premièrement, dans l’objectif de limiter le biais d’information lié à la qualité de l’histoire, un outil de collecte de données a été mis au point afin de la standardiser le plus possible. Comme la collecte de données était effectuée par une seule pharmacienne résidente, le risque de variabilité interindividuelle était éliminé, ce qui améliorait la reproductibilité. La méthode d’échantillonnage constituait une autre force de l’étude, car elle était aléatoire et permettait de bien représenter la population cible. Enfin, afin de limiter le biais d’interprétation, l’échelle de gravité a été interprétée par la pharmacienne résidente et deux responsables hospitaliers.
Le processus du bilan comparatif des médicaments actuel est propre à l’IUCPQ–UL. Nous avons montré que cette méthode permettait de brosser un portrait fidèle du profil médicamenteux du patient14. Par ailleurs, les offres de soins permettent de cibler les patients les plus vulnérables chez qui les interventions pharmaceutiques sont les plus pertinentes13. Dans un contexte où les ressources sont limitées, il est important de se questionner sur les retombées cliniques de l’histoire. Les résultats de cette étude montrent que la majorité des problèmes décelés à l’histoire avait un effet mineur et que seulement 12 problèmes avaient un effet important réel. Il est donc rassurant de constater que même si l’histoire n’est pas systématique pour tous les patients admis à l’IUCPQ–UL, faute notamment de ressources, sa valeur ajoutée est limitée quand le modèle d’offre de soins pharmaceutiques est bien établi dans l’ensemble des secteurs cliniques. Cette étude présente tout de même certains indices quant aux patients qui pourraient en bénéficier davantage. À cette fin, certaines informations additionnelles pourraient être apportées au processus actuel du bilan comparatif des médicaments pour orienter les pharmaciens et les critères d’une histoire dans l’offre de soins. Ces informations seront revues en fonction des résultats de cette étude. Certaines données pourraient également être ajoutées à l’outil de priorisation des patients dans le logiciel de la pharmacie.
Cet article comporte une annexe. Elle est disponible sur le site de Pharmactuel au www.pharmactuel.com.
Aucun financement en relation avec le présent article n’a été déclaré par les auteurs.
Tous les auteurs ont rempli et soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts en relation avec le présent article.
1. Ordre des pharmaciens du Québec. Guide des services pharmaceutiques en centre d’hébergement et de soins de longue durée. 1993;46.
2. Association des pharmaciens des établissements de santé du Québec. Recommandations sur la pratique de la pharmacie en établissement de santé - axe 1 : Soins pharmaceutiques. [en ligne] https://www.Apesquebec.Org/sites/default/files/publications/ouvrages_specialises/20180424_publications_pubspec_projet1.Pdf (site visité le 11 janvier 2021).
3. Ordre des pharmaciens du Québec et Collège des médecins du Québec. Bilan comparatif des médicaments : Recueil de politique et procédures. [en ligne] https://www.Opq.Org/wp-content/uploads/2020/03/2647_38_fr-ca_0_recueil_bcm_vf.Pdf (site visité le 11 janvier 2021).
4. Bilan comparatif des médicaments (BCM). Institut pour la sécurité des médicaments aux patients (ISMP) du Canada. [en ligne] https://www.ismp-canada.org/fr/BCM.htm. (site visité le 11 janvier).
5. Agrément Canada. Santé physique : Manuel d’évaluation 2019;413.
6. Abdulghani KH, Aseeri MA, Mahmoud A, Abulezz R. The impact of pharmacist-led medication reconciliation during admission at tertiary care hospital. Int J Clin Pharm 2018;40: 196–201.

7. Buckley MS, Harinstein LM, Clark KB, Smithburger PL, Eckhardt DJ, Alexander E et al. Impact of a clinical pharmacy admission medication reconciliation program on medication errors in “high-risk” patients. Ann Pharmacother 2013;47:1599–610.

8. Lee A, Varma A, Boro M, Korman N. Value of pharmacist medication interviews on optimizing the electronic medication reconciliation process. Hosp Pharm 2014;49:530–8.

9. Rodríguez Vargas B, Delgado Silveira E, Iglesias Peinado I, Bermejo Vicedo T. Prevalence and risk factors for medication reconciliation errors during hospital admission in elderly patients. Int J Clin Pharm 2016;38:1164–71.

10. Wanbon R, Lyder C, Villeneuve E, Shalansky S, Manuel L, Harding M. Medication reconciliation practices in canadian emergency departments: A national survey. Can J Hosp Pharm 2015;68: 202–9.

11. Gouvernement du Québec. Plan stratégique du ministère de la Santé et des Services sociaux – MSSS 2015–2020. [en ligne] http://publications.Msss.Gouv.Qc.Ca/msss/fichiers/2017/17-717-01w.Pdf (site visité le 11 janvier 2021).
12. Vérificateur général du Québec. Rapport du vérificateur général du Québec à l’Assemblée nationale pour l’année 2014–2015 : Vérification de l’optimisation des ressources, printemps 2014, chapitre 6 : Médicaments et services pharmaceutiques. [en ligne] http://www.Vgq.Gouv.Qc.Ca/fr/fr_publications/fr_rapport-annuel/fr_2014-2015-vor-printemps/fr_rapport2014-2015-vor-chap06.Pdf (site visité le 11 janvier 2021).
13. Racicot J, Plante-Proulx A, Taillon I, Pelletier-St-Pierre A, Lacroix C. Évaluation des interventions du pharmacien dans trois secteurs cliniques différents (cardiologie, pneumologie et médecine interne) selon le modèle traditionnel et le modèle décrit dans la nouvelle offre de soins pharmaceutiques de l’IUCPQ-U. Pharmactuel 2018;51:170–9.
14. Boivin E, Racicot J, Drolet B. Évaluation de la qualité des bilans comparatifs des médicaments réalisés pour les usagers hospitalisés à l’IUCPQ-UL depuis l’urgence. Pharmactuel 2018;52:25–33.
15. Belda-Rustarazo S, Cantero-Hinojosa J, Salmeron-García A, González-García L, Cabeza-Barrera J, Galvez J. Medication reconciliation at admission and discharge: An analysis of prevalence and associated risk factors. Int J Clin Pract 2015;69:1268–74.

16. Huber T, Brinkmann F, Lim S, Schröder C, Stekhoven DJ, Marti WR et al. Implementation of an IT-guided checklist to improve the quality of medication history records at hospital admission. Int J Clin Pharm 2017;39:1312–9.

17. Chung C, Gauthier V, Marques-Tavares F, Hindlet P, Cohen A, Fernandez C et al. Medication reconciliation: Predictors of risk of unintentional medication discrepancies in the cardiology department. Arch Cardiovasc Dis 2019;112:104–12.

18. Mazhar F, Akram S, Al-Osaimi YA, Haider N. Medication reconciliation errors in a tertiary care hospital in saudi arabia: Admission discrepancies and risk factors. Pharm Pract (Granada) 2017;15:864.

19. Karaoui LR, Chamoun N, Fakhir J, Abi Ghanem W, Droubi S, Diab Marzouk AR et al. Impact of pharmacy-led medication reconciliation on admission to internal medicine service: Experience in two tertiary care teaching hospitals. BMC Health Serv Res 2019;19:493.

20. Gleason KM, McDaniel MR, Feinglass J, Baker DW, Lindquist L, Liss D et al. Results of the medications at transitions and clinical handoffs (match) study: An analysis of medication reconciliation errors and risk factors at hospital admission. J Gen Intern Med 2010;25:441–7.

21. Brisson M, Cayer G, Dufour A, Poudrette J, Berbiche D. Évaluation de la fiabilité du Dossier santé Québec et du profil pharmacologique de la pharmacie communautaire comparativement à l’histoire pharmacothérapeutique pour la prescription des médicaments à l’urgence. Pharmactuel 2017;50:210–8.
22. Darbon F, Atkinson S, Bourassa E, Bédard P, Thibault M, Bussières J. Enquête québécoise sur la démarche du bilan comparatif des médicaments. Pharmactuel 2019;52:110–20.
23. Van Der Luit CD, De Jong IR, Ebbens MM, Euser S, Verweij SL, Van Den Bemt PM et al. Frequency of occurrence of medication discrepancies and associated risk factors in cases of acute hospital admission. Pharm Pract (Granada) 2018;16:1301.

24. Salanitro AH, Osborn CY, Schnipper JL, Roumie CL, Labonville S, Johnson DC et al. Effect of patient- and medication-related factors on inpatient medication reconciliation errors. J Gen Intern Med 2012;27:924–32.

25. Gleason KM, Groszek JM, Sullivan C, Rooney D, Barnard C, Noskin GA. Reconciliation of discrepancies in medication histories and admission orders of newly hospitalized patients. Am J Health Syst Pharm 2004;61: 1689–95.

26. Falconer N, Nand S, Liow D, Jackson A, Seddon M. Development of an electronic patient prioritization tool for clinical pharmacist interventions. Am J Health Syst Pharm 2014;71: 311–20.

27. Pippins JR, Gandhi TK, Hamann C, Ndumele CD, Labonville SA, Diedrichsen EK et al. Classifying and predicting errors of inpatient medication reconciliation. J Gen Intern Med 2008;23:1414–22.

28. Standards of practice for clinical pharmacy services (2016). [en ligne] https://www.shpa.org.au/resources/standards-of-practice-for-clinical-pharmacy-services (site visité le 11 janvier 2021).
29. Overhage JM, Lukes A. Practical, reliable, comprehensive method for characterizing pharmacists’ clinical activities. Am J Health Syst Pharm 1999;56:2444–50.

30. Micromedex. Monographie de l’olanzapine. IBM Micromedex. [en ligne] https://www.micromedexsolutions.com/home/dispatch/ssl/true(site visité le 11 janvier 2021).
31. Micromedex. Monographie de la clozapine. IBM Micromedex. [en ligne] https://www.micromedexsolutions.com/home/dispatch/ssl/true(site visité le 11 janvier 2021).
PHARMACTUEL, Vol. 55, No. 2, 2022