Myriame Diarra1, étudiante au BSBP, Geneviève Ouellet2, B.Pharm., M.Sc., Arnaud Bonnefoy3, Ph.D., Georges-Étienne Rivard4, M.D., Mihaela Friciu5, M.Sc., Jean-Marc Forest2, B.Pharm., DPH, M.Sc.
1Stagiaire au baccalauréat en sciences biopharmaceutiques, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
2Pharmacien(ne), Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada;
3Spécialiste clinique en biologie médicale, Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada;
4Médecin hémato-oncologue, Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada;
5Agente de recherche, plateforme de biopharmacie, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada
Reçu le 3 janvier 2024; Accepté après révision le 27 juin 2024
Résumé
Objectif: Au Centre hospitalier universitaire Sainte-Justine, plusieurs doses non commerciales d’énoxaparine sont préparées sous forme individualisée en seringue avec une aiguille. Les fioles commerciales d’une concentration de 100 mg/mL sont utilisées. Toutefois, il arrive qu’au moment de l’administration aux patients, un blocage de l’aiguille de la seringue soit observé. La réfrigération des seringues d’énoxaparine avant leur administration semble endiguer le problème. La présente étude vise principalement à examiner cette hypothèse.
Méthode: L’énoxaparine à 100 mg/mL a été reconditionnée en seringues d’un millilitre à partir des fioles de LovenoxMD. Les seringues ont ensuite été séparées en trois catégories, soit réfrigérées, surchauffées et température ambiante, pour différents temps de conservation. L’analyse des seringues a été effectuée à l’aide d’un manomètre pour point de bulle modifié. Les seringues d’énoxaparine réfrigérées ont par la suite été soumises au test de réchauffement. Enfin, l’effet de la réfrigération sur un biosimilaire d’énoxaparine, le RedescaMD, a également été évalué.
Résultats: Pour chacune des catégories, les résultats ont été regroupés sous forme de tableaux pour l’effet de la température de conservation, le temps pour le retour à la température ambiante et les essais avec le biosimilaire.
Conclusion: La réfrigération semble être efficace pour prévenir le blocage des aiguilles des seringues d’énoxaparine, que ce soit avec le médicament original ou le biosimilaire, sans nuire à sa stabilité. De plus, il a été déterminé que les seringues nécessitent de 15 à 20 minutes avant de revenir à la température ambiante après réfrigération, ce qui permet une injection plus confortable pour le patient.
Mots-clés: aiguilles, biosimilaire, énoxaparine, réfrigération, température
Abstract
Objective: At the Centre hospitalier universitaire Sainte-Justine, many non-commercial enoxaparin doses are individually prepared using syringes with needles. Commercially available vials at a concentration of 100 mg/mL are used. However, on occasion, at the time of administration to the patient, the syringe needle is found to be clogged. Refrigerating enoxaparin syringes prior to administration appears to solve this problem. The primary aim of this study was to investigate this hypothesis.
Method: Enoxaparin 100 mg/mL was repackaged in 1-mL syringes from Lovenox® vials. The syringes were then divided into three categories, namely, refrigerated, warming, and room temperature, for different storage times. The syringes were tested using a modified bubble point pressure gauge. The refrigerated enoxaparin syringes were then subjected to a heating test. Lastly, the effect of refrigeration on an enoxaparin biosimilar, Redesca®, was also evaluated.
Results: For each category, the results were grouped in tables according to the effect of storage temperature, the time to return to room temperature, and the trials performed with the biosimilar formulation.
Conclusion: Refrigeration appears to be effective in preventing needle clogging on enoxaparin syringes, whether with the branded or biosimilar drug, without adversely affecting its stability. In addition, it was determined that syringes take 15 to 20 minutes to return to room temperature after refrigeration, which allows for improved comfort when injecting the medication.
Keywords: Biosimilar, enoxaparin, needles, refrigeration, temperature
L’énoxaparine (LovenoxMD) est un anticoagulant prescrit pour traiter ou prévenir différents troubles thromboemboliques, tels que la thrombose veineuse profonde ou l’embolie pulmonaire, ainsi que certaines maladies cardiaques, telles que l’infarctus du myocarde1,2. On la retrouve au Centre hospitalier universitaire (CHU) Sainte-Justine sous forme de fioles multidoses ou de seringues préremplies unidoses, toutes à une concentration de 100 mg/mL. Comme la majorité des doses nécessaires en pédiatrie ne correspondent pas à un format commercial, ces dernières sont préparées en seringue pour une administration sous-cutanée. Pour les doses inférieures à un millilitre, l’aiguille est laissée en place sur la seringue pour limiter les pertes de volume.
Au moment de l’administration de doses servies avec une aiguille, il arrive parfois que les infirmières remarquent un blocage de cette aiguille rendant impossible l’administration de la dose, alors que le patient est déjà piqué, ce qui engendre un inconfort inutile. La décision d’ajouter un volume supplémentaire de 0,07 mL aux doses de moins d’un millilitre et d’apposer un bouchon a été prise afin de contourner ce problème. L’idée de ce surplus était de permettre au personnel infirmier de purger l’aiguille lors de son installation, tout en obtenant la dose voulue. Pour les doses supérieures à un millilitre, le service est effectué en seringue avec un bouchon, sans volume supplémentaire3.
Cette technique avec surplus ne permet pas, comme le souhaite le Département de pharmacie, de toujours fournir une dose exacte et prête à l’emploi. Elle complique aussi les manipulations pour un patient à domicile. Une recherche d’alternative était donc de mise. L’objectif principal était de trouver une solution au blocage des aiguilles sur les seringues d’énoxaparine à l’aide de différentes méthodes en testant les hypothèses préétablies. Puis, une ou plusieurs hypothèses pourraient être avancées pour déterminer la cause probable de ce blocage en présence de l’aiguille.
Selon l’étude d’Hamilton et collaborateurs, la réfrigération évite le blocage des aiguilles d’énoxaparine4. Cette hypothèse d’une solution simple méritait que l’on s’y attarde. La chaleur semblant être la cause de l’obstruction, il fut décidé de surchauffer certaines seringues avec aiguille à 50 °C afin d’observer l’effet contraire, le cas échéant. De plus, la stabilité du biosimilaire utilisé au CHU Sainte-Justine, le RedescaMD, n’étant pas connue lorsqu’il est reconditionné en seringue avec aiguille, puis réfrigéré, il était également nécessaire de l’établir.
Une des difficultés rencontrées consistait à quantifier, même approximativement, ce blocage d’aiguille. Un manomètre, normalement prévu pour la mesure du point de bulle de filtres stériles, a donc été utilisé. Grâce à la pression, exprimée en Pascal (Pa), il était possible de quantifier le blocage des aiguilles des seringues ou non. En effet, lorsqu’une seringue est bloquée, la pression oscille autour de 40 à 45 Pa et se maintient, alors que sans blocage, la pression varie de 20 à 25 Pa et diminue rapidement. Les intervalles permettent une plus grande marge de manœuvre quant à la force appliquée par l’expérimentateur sur le piston. De plus, toutes les mesures ont été effectuées par le même expérimentateur afin de conserver une certaine constance à ce chapitre et ainsi limiter un biais. Cette technique était simple et sans frais, comparativement à d’autres méthodes plus lourdes, telles que la chromatographie liquide à haute performance, plus précise mais plus complexe et dispendieuse.
Par manque de temps, d’équipement, de matériel et de fonds, toutes les hypothèses n’ont pu être testées. Toutefois, comme la réfrigération semblait être la solution à la fois la plus prometteuse et la plus pratique, c’est cette dernière qui a été retenue. Cette option était d’autant plus attirante qu’un test préliminaire de réfrigération des seringues avec aiguille a donné de très bons résultats.
Les seringues d’énoxaparine ont été préparées à partir des fioles de LovenoxMD injectable de la compagnie Sanofi-Aventis (300 mg/3 mL, lot 1F027F) pour les trois premières séries d’expérimentation. Un test préliminaire, mené sur cinq jours avec 10 seringues réfrigérées, 10 seringues à température ambiante et 10 seringues à 50 °C, avec comme témoin 10 seringues d’eau dans chacun des cas, a eu lieu avant d’initier une étude plus complète. Les résultats étant des plus encourageants, l’effet de la température, notamment de la réfrigération, sur le phénomène de blocage de l’aiguille avec l’énoxaparine a été testé. Dans un environnement stérile, un volume de 0,1 mL d'énoxaparine a été prélevé dans 450 seringues d’un millilitre. Une aiguille par seringue était ajoutée, et sa purge était effectuée jusqu’à ce qu’une goutte perle à la pointe de l’aiguille. Les seringues ont été par la suite conservées à trois températures différentes. La première série était conservée au réfrigérateur (soit à une température de 2 à 8 °C), la deuxième dans une étuve (dont la température était fixée à 50 °C) et la dernière a été conservée à la température ambiante (soit de 22 °C). La durée de l’exposition était variable, soit de 1, 2, 4, 7 et 10 jours, le jour zéro ne présentant d’office pas de blocage et étant de toute façon testé par le retour facile du piston pour toutes les seringues. En parallèle, des seringues d’eau munies d’aiguille, préparées à titre de comparateur pour les seringues d’énoxaparine, étaient aussi purgées pour chaque température. Les seringues munies d’une aiguille ont été placées dans des sacs et identifiées selon leur état de conservation afin de simuler la pratique et de limiter l’évaporation. Pour chaque jour d’analyse, 180 seringues ont été testées : 30 seringues d’énoxaparine et 30 seringues d’eau stérile pour chaque condition de conservation afin de déterminer s’il y avait un blocage à l’aide du manomètre à point de bulle (filtres de seringue WIZARDMD Healthmark). Ce système de point de bulle modifié est un dispositif en trois parties. D’un côté, on trouve une seringue remplie d’air et de l’autre, l’aiguille à tester contenant la solution d’énoxaparine, le tout séparé par un manomètre notant la pression en Pascal. Le manomètre sert à quantifier la pression minimale requise pour forcer le liquide à traverser l’aiguille et à s’écouler. Si la valeur dépasse 30 Pa, c’est que l’aiguille est bouchée et donc que le liquide ne s’écoule pas. Une pression inférieure à 20 ou à 25 Pa correspond à la résistance normale dans l’aiguille vu sa faible lumière. Cette pression ne peut être maintenue plus de quelques secondes puisque l’air s’échappe, ce qui n’est pas le cas lors d’une obstruction de l’aiguille. La figure 1A, en annexe, montre le montage de point de bulle modifié utilisé durant l’étude.
La deuxième expérience consistait à étudier le réchauffement des seringues après la réfrigération pour déterminer le temps nécessaire pour un retour à la température ambiante avant l’administration au patient. L’administration d’un liquide froid est déconseillée puisqu’il entraîne de l’inconfort chez le patient. Dans un premier temps, la technique de mesure de la température par un thermomètre infrarouge a été validée avec l’emploi de 10 seringues remplies de 0,1 mL d’eau placées dans des sacs et réfrigérées. Après 48 heures de réfrigération, les 10 seringues ont été retirées du réfrigérateur, déposées sur une surface à température ambiante et séparées les unes des autres afin d’éviter des échanges de chaleur. Toutes les cinq minutes, la température des barillets des seringues a été évaluée à l’aide d’un thermomètre de type MiniTemp pendant 40 minutes. Le MiniTemp est un thermomètre infrarouge qui permet de lire la température des surfaces sans contact, ce qui convenait parfaitement aux besoins de l’étude. La figure 1B, en annexe, montre le thermomètre MiniTemp de la compagnie Rayteck, modèle MT4, utilisé dans l’étude. Il a alors été constaté qu’une stabilisation se dessinait après 15 à 20 minutes. Au moment du retour à la température ambiante, une petite quantité de solution de chacune des seringues était évacuée afin de vérifier si la température du liquide d’énoxaparine correspondait à celle mesurée à l’extérieur de la seringue après 20 minutes pour l’énoxaparine, alors que le test se poursuivait jusqu’à 40 minutes pour l’eau. L’expérience a été reproduite avec cinq seringues munies d’aiguille et contenant 0,1 mL d’énoxaparine (LovenoxMD, lot 1F027F) après 48 heures de réfrigération.
La troisième expérimentation évaluait l’effet de la température, principalement la réfrigération, sur le biosimilaire RedescaMD utilisé au CHU Sainte-Justine en comparaison avec le LovenoxMD, cette donnée sur la stabilité du biosimilaire réfrigéré n’étant pas connue. Pour ce faire, 60 seringues munies d’une aiguille contenant 0,1 mL d’énoxaparine ont été préparées dans un milieu stérile à partir des fioles de RedescaMD injectable de la compagnie Valeo Pharma (100 mg/mL, lot AM00722A), soit 5 par temps et condition de mesure. La fluidité du piston des différentes seringues était vérifiée afin de s’assurer qu’aucune réaction de blocage d’aiguille ne survenait au départ. Elles ont ensuite été placées dans des sacs pour être conservées dans trois milieux différents, soit réfrigéré, surchauffé et à température ambiante pendant quatre périodes de conservation de 0, 4, 7 et 10 jours. En parallèle, des seringues d’eau stérile pour injection de 0,1 mL chacune ont également été préparées à titre de comparateur pour chacune des températures d’expérimentation. Pour chaque jour d’analyse, des seringues de chaque type ont été testées à la recherche d’un blocage à l’aide du manomètre à point de bulle modifié. Les résultats ont ensuite été comparés avec ceux du LovenoxMD.
Enfin, la stabilité du biosimilaire RedescaMD pure à une concentration de 100 mg/mL a été estimée, en trois exemplaires en seringues réfrigérées de 0,1 mL, par l’entremise d’une analyse par l’activité contre le facteur X activé. Pour que la concentration de RedescaMD soit mesurable, et de pouvoir utiliser les courbes de calibration du test d’héparine de faible poids moléculaire en unité internationale (UI)/mL (Trousse Liquid anti-Xa STAGO Asnière, France, Instrument STAGO STA R MAX 3), une pré dilution de 1/1000 du contenu de chaque seringue dans une solution saline à 0,9 % (trois dilutions en série de 1/10), suivie d’une dilution de 1/20 dans un pool de plasma normal (CryoCheck pooled normal plasma référence CCN-15), a été effectuée. La dilution totale était donc de 1/20 000, soit de 5 μg/mL. Le facteur de conversion utilisé est donc de 10 μg/mL, ce qui donne 1 UI/mL. Les résultats sont tabulés en mg/mL, correspondant directement à la concentration du produit utilisé en clinique pour plus de simplicité.
Toutes les mesures ont été faites par le même expérimentateur tout au long des tests afin de conserver une constance à ce niveau et de limiter la survenue d’un biais. Bien que des appareils automatiques pour la mesure du point de bulle existent, ils n’étaient pas disponibles pour l’étude. Dans tous les cas, les seringues utilisées avaient un volume d’un millilitre et étaient fabriquées en polycarbonate (lot 3131853 de la compagnie BD). Les aiguilles étaient de calibre 30G 1/2 (lot 3055902 toujours de la compagnie BD).
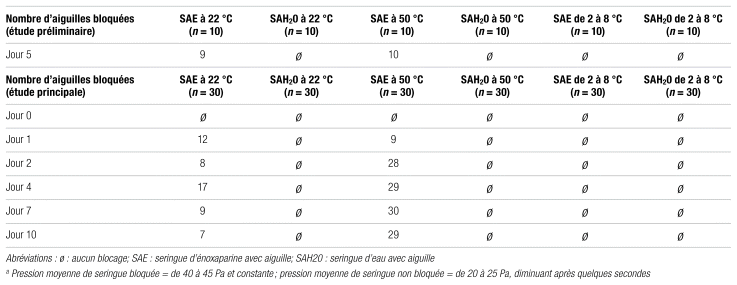
Le sommaire des blocages des aiguilles des seringues d’énoxaparine (LovenoxMD) et d’eau réfrigérée de la première série d’expériences est présenté dans le tableau I. Ce dernier contient deux sections : la première présente l’étude préliminaire avec 10 seringues sur cinq jours seulement aux trois températures de conservation (de 2 à 8 °C, 22 °C et 50 °C). Ensuite, la deuxième montre l’étude principale avec 30 seringues pour chacune des conditions d’entreposage, pour un sommaire du nombre d’aiguilles d’énoxaparine et d’eau retrouvées bloquées après 0, 1, 2, 4, 7 et 10 jours pour les trois conditions de conservation. Au jour 0, aucune aiguille n’a bloqué. Au jour un, 12 aiguilles sur 30 ont bloqué à 22 °C et 9 sur 30 à 50 °C, mais aucune lorsqu’elles étaient réfrigérées. Au jour deux, 8 aiguilles sur 30 ont bloqué à 22 °C et 28 sur 30 à 50 °C. Au jour quatre, 17 aiguilles sur 30 ont bloqué à 22 °C et 29 sur 30 à 50 °C. Au jour sept, 9 aiguilles sur 30 ont bloqué à 22 °C et toutes les aiguilles ont bloqué à 50 °C. Enfin, au jour 10, 7 aiguilles sur 30 ont bloqué à 22 °C et 29 sur 30 à 50 °C. Plusieurs seringues avaient une goutte solide au bout de leur aiguille à 50 °C, qui conservait sa forme et son aspect. Pour chacune des journées, aucune aiguille de seringue réfrigérée n’a été bloquée, ce qui en fait une piste de solution très prometteuse.
Les tableaux II et III montrent les résultats du réchauffement des seringues d’énoxaparine après réfrigération (deuxième série d’expériences). Une première série d’expérimentation a offert des résultats complètement erratiques et ininterprétables à partir des seules seringues d’eau témoins.
Tableau I Portrait sommaire du nombre d’aiguilles bloquées montées sur les seringues de LovenoxMD et d’eau, selon la température et la durée d’entreposage pour l’étude préliminaire et l’étude principalea

Certaines modifications ont été apportées aux tests avec les seringues d’énoxaparine et à de nouvelles seringues d’eau témoin pour la suite. D’abord, la première mesure (à 0 minute) a été prise directement dans le réfrigérateur pour éviter des résultats biaisés. Par la suite, un coin de comptoir sans flux de ventilation dans la pièce a été utilisé. Un réchauffement continu a été observé et un plateau a été atteint avec lectures aux 5 minutes, soit à la température ambiante, après 15 à 20 minutes, même si les lectures se sont étalées jusqu’à 40 minutes par précaution.
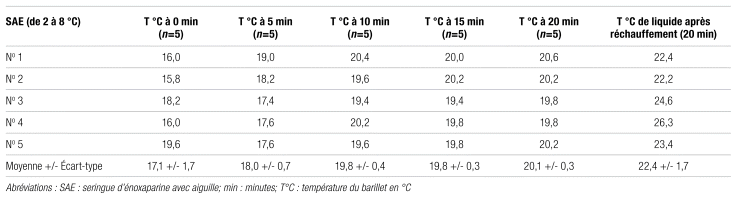
Dans un premier temps, un sommaire est présenté pour les temps de réchauffement pendant 40 minutes, dont un plateau après 20 minutes environ, pour les barillets des seringues d’eau (tableau II) et d’énoxaparine (tableau III), toutes munies d’une aiguille. Après le retour à température ambiante du barillet, la température de la solution a été mesurée et ajoutée au tableau.
Les résultats de la réfrigération sur le biosimilaire RedescaMD sont mentionnés dans le tableau IV. Ce dernier comprend un sommaire du nombre d’aiguilles bloquées sur les seringues d’énoxaparine et d’eau pour les trois conditions de température. Le tout est séparé en quatre sections pour chaque jour d’analyse, soit les jours 0, 4, 7 et 10.
Enfin, le tableau V, en annexe, présente l’activité du biosimilaire RedescaMD contre le facteur X activé, lorsqu’il est conservé pur (100 mg/mL en seringues) au réfrigérateur aux mêmes temps d’analyse standard de l’étude, soit les jours, 0, 4, 7 et 10.
Tableau II Sommaire des températures de réchauffement des barillets de seringues d’eau
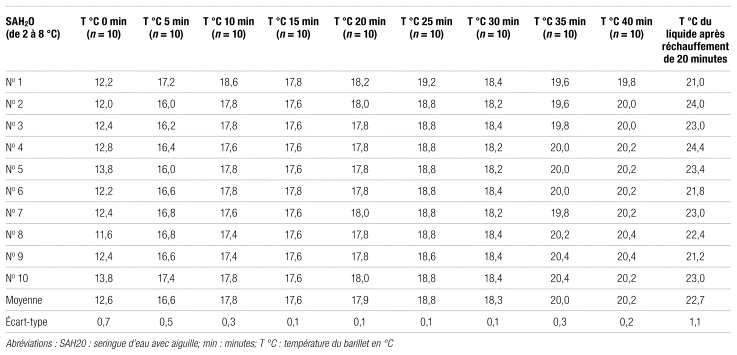
Tableau III Sommaire des températures de réchauffement des barillets de seringues d’énoxaparine (LovenoxMD)
L’étude de Charland et collaborateurs, qui évaluait la stabilité de l’énoxaparine de marque Lovenox MD reconditionnée en seringues à tuberculine avec aiguille, a montré une stabilité de 10 jours au réfrigérateur5. Accessoirement, la réfrigération ne provoquait pas de blocage de l’aiguille (du moins aucun n’y est mentionné). Hamilton et collaborateurs a également conclu à une stabilité de 10 jours à température ambiante pour l’énoxaparine reconditionnée en seringues à tuberculine avec aiguille4. Toutefois, les auteurs notaient un blocage occasionnel de l’aiguille, qu’ils supposaient être relié à une précipitation d’un sel en fonction du temps, alors qu’aucun blocage n’était présent avec la réfrigération. Pour leur part, Mewborn et collaborateurs mentionnent une stabilité d’au moins 48 heures de l’énoxaparine diluée à 1,2 mg/mL dans du chlorure de sodium à 0,9 % provenant d’un sac de chlorure de polyvinyle standard6.
Tableau IV Sommaire des blocages des aiguilles des seringues d’énoxaparine et d’eau pour le biosimilaire d’énoxaparine (RedescaMD)

L’étude préliminaire montre que pour les seringues d’énoxaparine (marque LovenoxMD) conservées à température pièce, neuf aiguilles sur 10 ont bloqué et qu’aucune aiguille d’eau n’a bloqué. Pour les aiguilles réfrigérées, aucune n’a bloqué, tandis que toutes celles chauffées dans l’étuve ont bloqué. Dans le cas de ces dernières, la formation d’un précipité solide au bout de l’aiguille de deux seringues a été observée, mais il est difficile, sans en faire l’analyse approfondie, de déterminer s’il s’agit d’énoxaparine ou d’une autre substance. La figure 1C, en annexe, montre un exemple de goutte solide observée au bout de l’aiguille. Il serait intéressant d’en faire l’analyse poussée pour en déterminer la composition et Enlever SVP l’origine.
Comme on peut le constater dans les tableaux II et III, la température des solutions (eau et énoxaparine) se stabilisait rapidement sans avoir atteint la température ambiante. Cette situation peut être due à plusieurs facteurs. Les seringues se trouvaient directement sous une grille d’aération, ce qui rendait la lecture plus difficile et entraînait une fluctuation des valeurs. De plus, le manque de précision de l’appareil utilisé pour la mesure de la température a pu affecter les résultats. Il faut également noter la forte influence de l’environnement sur le réchauffement de la seringue. En effet, la zone d’air frais semble ralentir considérablement le réchauffement du barillet de la seringue. Ensuite, la température du contenu, soit l’énoxaparine, semble plus élevée d’un ou deux degrés en comparaison de l’extérieur du barillet de la seringue, ce qui indiquerait possiblement que la solution se réchauffe rapidement lorsqu’elle se trouve directement à température ambiante. Ce sont là des observations encore non expliquées.
Quant au troisième volet de l’étude, les résultats du biosimilaire Redesca MD sont semblables à ceux du LovenoxMD. Ainsi, la même stabilité physicochimique connue du LovenoxMD réfrigéré a été retrouvée pour le RedescaMD aux mêmes conditions.
Bien que la réfrigération semble fonctionner, il est possible d’envisager d’autres pistes de solution pour éviter le blocage des aiguilles. Une première consisterait à ajouter de l’azote dans les seringues pour protéger le médicament de l’oxydation et ainsi conserver son efficacité3. Cette hypothèse provient du fait que le fabricant incorpore de l’azote dans les fioles et les aiguilles des seringues commerciales pour éviter l’interaction de l’énoxaparine avec l’oxygène. Il serait intéressant d’appliquer ce principe aux seringues préparées aux doses non standard, c’est-à-dire sur mesure. Ainsi, s’il y a oxydation entre deux éléments dans les conditions sans azote, il serait concevable de travailler sous atmosphère d’azote pour contrer le blocage de l’aiguille de la seringue. Cette solution nécessiterait quelques accommodations techniques, mais n’est pas impossible.
Une autre piste à étudier consisterait à tester la compatibilité entre la solution médicamenteuse et les différentes composantes de l’aiguille7. Dans le cas d’une incompatibilité, il faudrait valider si cette interaction a un effet possible sur le blocage de l’aiguille. Il serait possible de mettre chacun des matériaux (par exemple silicone, polypropylène, époxyacrylique et acier inoxydable) individuellement en contact avec la solution d’énoxaparine, les conserver à température ambiante pendant 10 jours, faire une analyse physique (observation visuelle d’un changement de couleur, de texture, formation d’un résidu, etc.) de chaque matériau, puis utiliser un viscosimètre pour mesurer la viscosité du mélange. Si une variation était observée dans le temps ou s’il y avait une différence par rapport à la solution d’énoxaparine seule, on pourrait supposer qu’il y a eu réaction entre la composante de l’aiguille et le médicament. De plus, si un changement physique était observé, la même conclusion s’appliquerait. Mais le tout demeure complexe et à prouver.
Il y aurait également lieu de prélever de l’énoxaparine dans les seringues à insuline directement à partir des fioles de LovenoxMD, puis de les conserver dans trois conditions de température prédéterminées soit entre 2 à 8 °C (réfrigérateur), à 22 °C (température ambiante) et à 50 °C (étuve). Cette méthode de reconditionnement semble être plus précise, en raison des graduations plus petites de la seringue d’insuline, et pourrait possiblement diminuer les risques d’interactions puisque la surface de contact est possiblement plus petite à la lumière de son aiguille. Cependant, l’utilisation des graduations prévues pour les unités d’insuline peut engendrer des erreurs de mesure de dose.
Il serait finalement possible de se pencher sur l’effet de l’alcool benzylique, un agent de conservation de la préparation. Ce dernier pourrait avoir un rôle à jouer dans le blocage de l’aiguille.
Une explication simple du phénomène de blocage serait liée au fait que l’aiguille est en métal et donc chargée positivement. L’énoxaparine, membre de la famille des «parine», est fortement chargée négativement. Il peut donc y avoir attraction des charges opposées, ce qui pourrait conduire à la formation d’un film qui bloquerait la sortie de liquide de l’aiguille. Cette hypothèse, simple en apparence, mériterait à elle seule toute une série d’évaluations.
Dans le processus de recherche, un mini-sondage informel a aussi été mené dans plusieurs établissements de santé. Bien que plusieurs d’entre eux n’avaient pas le même processus de reconditionnement avec aiguille et d’autres n’avaient pas remarqué ce problème, les différents commentaires sur la situation étaient intéressants, comme la mention que l’énoxaparine est un produit très visqueux et qu’une seringue commerciale avec aiguille est fabriquée sous atmosphère d’azote.
Le CHU Sainte-Justine a opté, par l’entremise de son groupe d’achat, pour l’utilisation du biosimilaire d’énoxaparine RedescaMD en remplacement de l’énoxaparine originale LovenoxMD. Dans les deux cas, une seringue préparée avec aiguille s’obstruait occasionnellement à température ambiante pour une cause inconnue. La réfrigération représente une solution simple qui, selon nos résultats, semble efficace. Les étiquettes des seringues portent donc dorénavant la mention «Réfrigéré», mais il faut se rappeler que c’est pour éviter le blocage de l’aiguille et non pour améliorer la stabilité du médicament. Il faut aussi considérer qu’une fois la seringue d’énoxaparine hors du réfrigérateur, un délai de 15 à 20 minutes est requis pour le retour à la température ambiante, sans réchauffement additionnel. Le biosimilaire RedescaMD a présenté des résultats semblables au LovenoxMD, ce qui indique que peu importe le produit utilisé, la réfrigération fonctionne pour prévenir le blocage de l’aiguille.
Bien qu’une solution ait été trouvée, la cause du blocage de l’aiguille demeure inconnue. Les différentes hypothèses proposées mériteraient qu’on s’y attarde davantage. De plus, il serait pertinent d’étudier les gouttes solides qui ont été observées au bout des aiguilles exposées une température de 50 °C.
Tout le matériel, y compris les médicaments, a été fourni par le Département de pharmacie ou le secteur de fabrication du CHU Sainte-Justine. Le coût des analyses biochimiques et leur réalisation sont à la seule charge du laboratoire Optilab du CHU Sainte-Justine.
Tous les auteurs ont soumis le formulaire de l’ICMJE sur la divulgation de conflit d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts lié au présent article.
Les auteurs remercient Mme Nancy Rose, coordonnatrice des laboratoires regroupés d’Optilab CHU Sainte-Justine pour l’aide dans les dosages de l’énoxaparine. Cette personne a donné son autorisation écrite. De même, Les auteurs remercient l’équipe d’assistants techniques du secteur fabrication du Département de pharmacie du CHU Sainte-Justine pour leur aide dans la préparation des échantillons tout au long de l’étude.
1. DrugBank Online. Enoxaparine (2023). [en ligne] https://go.drugbank.com/drugs/DB01225 (site visité le 29 mai 2023).
2. USP. Enoxaparin Sodium Injection (2020). [en ligne] https://online.uspnf.com/uspnf/document/1_GUID-B6AD8BF0-3FAF-4377-8C58-5BEB9493B798_5_en-US?source=Search%20Results&highlight=énoxaparine (site visité le 29 mai 2023).
3. CHU Sainte-Justine, Département de pharmacie, secteur fabrication. Énoxaparine fiche d’information (2017). [en ligne, données internes seulement] (site visité le 29 mai 2023).
4. Hamilton MA, Stang L, Etches WS, Rennie R, Mant MJ. Stability of low molecular weight heparins stored in plastic syringes. Thromb Res 2003; 112:117–9.
Crossref
5. Charland SL, Davis DD, Tillman DJ. Activity of enoxaparin sodium in tuberculin syringes for 10 days. Am J Health-Syst Pharm 1998;55:1296–8.
Crossref PubMed
6. Mewborn AM, Kessler JM, Joyner KA. Compatibility and activity of enoxaparin sodium in 0.9% sodium chloride injection for 48 hours. Am J Health-Syst Pharm 1996;53:167–9.
Crossref
7. BD, Fiche technique : Aiguilles hypodermiques jetables BD (juin 2022). [en ligne] https://www.bd.com/fr-ca/products/medical-surgical-systems/injection-systems/syringes-and-hypodermic-needles (site visité le 29 mai 2023).
Pour toute correspondance : Jean-Marc Forest, Centre hospitalier universitaire Sainte-Justine, 3175, chemin de la Côte-Sainte-Catherine, Montréal (Québec), H3T 1C5, CANADA; Téléphone : 514 345-4603; Courriel : jean-marc.forest.hsj@ssss.gouv.qc.ca
PHARMACTUEL, Vol. 57, No. 4, 2024