Tasnime-Aicha Cherid1, Jessie Grèves2, DEP, Josée Robillard3, B.Pharm., DPH, Jean-Marc Forest4, B.Pharm., DPH, M.Sc.
1Candidate au doctorat de premier cycle en pharmacie au moment de la rédaction, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
2Cheffe d’équipe des assistants techniques en pharmacie, secteur fabrication, Département de pharmacie, Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada;
3Pharmacienne, Secteur des produits stériles, Hôpital Pierre-Boucher du Centre intégré de santé et de services sociaux de la Montérégie-Est, Longueuil (Québec) Canada;
4Pharmacien, Secteur de la fabrication, Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada
Reçu le 26 janvier 2024; Accepté après révision le 15 mai 2024
Résumé
Objectifs: Dans les départements de pharmacie, les fournitures défectueuses sont inévitables. Cette situation est importante à gérer afin de préserver la satisfaction et de prodiguer des soins de qualité. Il devient intéressant de créer un formulaire permettant d’informer rapidement les fabricants ou les fournisseurs de la défectuosité des fournitures pharmaceutiques, dès la constatation du problème et généralement avant l’utilisation du produit.
Description de la problématique: La première étape consistait à analyser des fournitures présentant le plus fréquemment des défauts, puis faire des recherches en ligne sur des bases de données médicales et dans la base de données de Santé Canada. Un formulaire simplifié a ensuite été créé pour garantir la collecte précise d’informations et la transmission correcte aux compagnies. L’élaboration d’une procédure s’en est suivie.
Résolution de la problématique: Pendant les quatre semaines de ce projet, un formulaire de déclaration de fournitures défectueuses a été créé, ainsi qu’une procédure de gestion des fournitures pharmaceutiques. Néanmoins, un obstacle majeur s’est présenté sous forme de lenteur administrative lors de la communication avec les compagnies.
Conclusion: La création d’un formulaire de déclaration de fournitures pharmaceutiques défectueuses avant leur emploi dans un hôpital est utile pour garantir la qualité des soins ainsi que la sécurité des patients et du personnel et pour informer le fabricant ou le fournisseur. En facilitant la communication entre le Département de pharmacie et les fournisseurs, le formulaire contribue à une gestion plus efficace des fournitures pharmaceutiques et renforce la culture de la sécurité au sein de l’établissement.
Mots-clés: communication, fournitures pharmaceutiques, gestion des équipements et fournitures de l’hôpital, pharmacie, qualité des soins, innocuité du matériel, sécurité des patients
Summary
Objectives: Defective supplies are inevitable in pharmacy departments. This situation is important to manage to maintain satisfaction and provision of quality care. A form allowing staff to quickly inform manufacturers or providers of defective pharmaceutical supplies, as soon as the problem is identified and generally before the product is used, would be useful.
Problem description: The first step was to identify which supplies were most frequently found to be defective and then conduct online research of medical databases and Health Canada’s database. A simplified form was then created to ensure accurate information collection and adequate transmission to companies. A procedure was then developed.
Problem resolution: During the four week project, a form for reporting defective supplies was created, and a procedure for managing pharmacy supplies was written. However, a major obstacle was the administrative delays in communicating with companies.
Conclusion: The creation of a form for reporting defective pharmacy supplies prior to their use in-hospital is useful for ensuring quality of care as well as patient and staff safety and for informing the manufacturer or supplier. By facilitating communication between the department of pharmacy and suppliers, the form contributes to more effective management of pharmacy supplies and reinforces the culture of safety.
Keywords: communication, pharmaceutical supplies, hospital equipment and supplies management, pharmacy, care quality, material safety, patient safety
La qualité des fournitures pharmaceutiques utilisées dans les hôpitaux joue un rôle essentiel dans la prestation de soins de santé de qualité. Les hôpitaux sont des établissements centrés sur la santé et le bien-être des patients. La fiabilité des produits qu’ils emploient est un élément clef pour garantir des soins efficaces et sûrs. Néanmoins, il est important de noter que, malgré les contrôles de qualité de l’industrie, des produits défectueux se retrouvent tout de même parfois dans ces établissements, notamment dans les départements de pharmacie.
Dans ce contexte, la création d’un formulaire de déclaration simplifié de fournitures pharmaceutiques défectueuses est souhaitable pour les hôpitaux. Ce formulaire vise à proposer un mécanisme systématique, rapide et simple pour signaler et gérer les fournitures pharmaceutiques présentant des problèmes, tout en renforçant la communication avec les fournisseurs, leur permettant ainsi de s’améliorer. Le présent article examine les avantages de ce processus sur le plan de la communication avec les fournisseurs et de la sécurité des patients. Il met en évidence l’importance de cette démarche dans le contexte hospitalier, en insistant sur la nécessité de disposer de protocoles clairs pour la gestion des fournitures défectueuses. Enfin, il propose des pistes de solution pour éviter, comme c’est trop souvent le cas actuellement, que des fournitures défectueuses soient tout simplement jetées et remplacées par d’autres, sans qu’aucune trace ne soit gardée de cette manœuvre. La charge de travail étant élevée, il est malheureusement généralement plus simple jeter le matériel défectueux et de continuer avec du matériel conforme, sans procéder au moindre suivi du problème. Le formulaire de déclaration de Santé Canada représente fréquemment une lourdeur non souhaitable, d’autant plus qu’au stade de la découverte de la défectuosité, aucun patient n’est touché.
Dans le processus de création du formulaire de déclaration de fournitures défectueuses, la première étape est de trouver les entreprises dont les produits comportent le plus fréquemment des défauts de fabrication. Cette analyse a été menée par l’examen d’un bac récolté au fil des mois par les assistants techniques séniors en pharmacie (ATSP), contenant surtout des fournitures, quelques médicaments et du matériel pharmaceutique ne correspondant pas aux normes de qualité attendues, présentant des défectuosités ou s’étant brisé prématurément.
Les produits mis de côté étaient principalement :
Des recherches ont ensuite été effectuées dans les bases de données médicales de référence (par exemple : MedLINE et PubMed), en utilisant des termes comme «defect» et «supply» afin de mieux cerner le problème. Cependant, ces recherches n’ont pas abouti à des résultats concluants. Par la suite, une recherche menée dans la base de données de Santé Canada a permis de recueillir des informations sur les formulaires de déclaration d’incidents liés aux dispositifs médicaux afin de mieux comprendre les normes et les pratiques recommandées en matière de signalement des produits défectueux et des incidents liés aux dispositifs médicaux1–3. Les informations obtenues ont servi à la création du prototype du formulaire de déclaration de fournitures défectueuses que le CHU Sainte-Justine pourrait utiliser au Département de pharmacie.
Pour recueillir des informations nécessaires en vue de concevoir le formulaire, des recherches ont également été menées en ligne sur les sites des principales compagnies touchées4–8. Cette démarche visait à comprendre les différentes politiques de retour de produits pharmaceutiques défectueux mises en place par ces compagnies.
Le formulaire, conçu pour faciliter la collecte d’informations précises au sein du Département de pharmacie, prévoit des champs obligatoires pour les données essentielles et des espaces pour des commentaires supplémentaires, au besoin. Ce formulaire a été créé en étroite collaboration avec la cheffe d’équipe des ATSP afin d’en assurer la convivialité et l’efficacité. Les informations requises sont les suivantes :
Le prototype du formulaire a été soumis à la cheffe d’équipe et au pharmacien responsable du secteur de la fabrication afin de recueillir leurs avis et qu’ils en évaluent la convivialité. Une fois les ajustements nécessaires apportés, le formulaire a été envoyé aux différentes compagnies partenaires, par courriel, pour solliciter leurs points de vue et leur suggérer de se servir de ce formulaire à l’avenir comme moyen principal, rapide et efficace, de communication lors de la découverte d’une défectuosité.
En complément du formulaire, une procédure a été élaborée pour l’intégrer dans le système de gestion du Département de pharmacie, en collaboration avec le groupe de travail sur les préparations stériles (GTPS) de l’Association des pharmaciens en établissement de santé (A.P.E.S.). Cette procédure permet aux ATSP et aux techniciens en pharmacie (TP) d’utiliser plus efficacement le formulaire de déclaration de fournitures pharmaceutiques défectueuses dans le cadre de leurs responsabilités, ce qui renforce la gestion globale des dispositifs pharmaceutiques au sein du Département de pharmacie de l’hôpital. Cette procédure est disponible sur le site Web de l’A.P.E.S. dans son microsite sur les produits stériles et non stériles (disponible uniquement aux membres de l’A.P.E.S.).
La participation de différents professionnels du Département de pharmacie (p. ex. : ATSP, TP et pharmaciens) est importante pour la bonne mise en œuvre de cette procédure de déclaration. Certains équipements, installations et outils sont souhaitables, voire nécessaires, notamment des bacs de stockage spécialement destinés aux produits défectueux, des caméras (Web ou régulières, selon les spécifications de l’établissement), un logiciel informatique, ainsi qu’un système de suivi des courriels. La notification de la défectuosité commence lorsque le matériel pharmaceutique ne satisfait pas aux normes de qualité attendues, ne fonctionne pas correctement ou se brise prématurément, en cas de récurrence ou non du même problème pour plusieurs utilisateurs du même produit et en présence ou non d’un défaut présentant un risque pour la sécurité ou la santé.
La première étape consiste à informer rapidement le pharmacien de service, puis de rassembler les informations essentielles sur le produit défectueux. Cette collecte est importante avant d’entreprendre toute démarche de notification afin de faciliter la communication au sein du Département de pharmacie ainsi qu’avec les compagnies et de réduire d’éventuelles lenteurs administratives.
La deuxième étape consiste à fournir des photos du produit défectueux. Au CHU Sainte-Justine, une solution pratique pour simplifier la démarche, pour ceux qui découvrent un produit défectueux, est de prendre une photo mettant en évidence la défectuosité, en y indiquant le numéro de lot et la date de péremption, à l’aide des caméras du Département de pharmacie. Cette méthode permet un transfert automatique de l’image vers le logiciel NUMERx2 (Gespharx / Québec, Canada) assurant ainsi la traçabilité du produit. La personne ayant découvert la défectuosité pourra ajouter, dans la case «commentaire», la date du jour, le terme «défectuosité», ainsi que ses initiales.
Après avoir identifié une défectuosité, il est essentiel de désigner une personne pour faciliter et superviser la communication avec les compagnies et pour en faire le suivi. Au CHU Sainte-Justine, cette personne est la cheffe d’équipe des ATSP du secteur concerné et éventuellement possiblement un TP. Ses principales responsabilités consistent à gérer la communication avec les fournisseurs. Une fois le formulaire rempli, il est envoyé par courriel, accompagné des photos en pièces jointes. Le formulaire est présenté en annexe (figure 1).
En outre, conformément aux recommandations de Santé Canada, il est fortement conseillé de notifier les incidents liés aux instruments médicaux dans les 30 jours suivant leur constatation1–3. À noter toutefois que cette procédure ne concerne que les défectuosités de matériel à la pharmacie et donc avant qu’il soit utilisé avec le patient. C’est une procédure allégée qui n’inclut pas celle de Santé Canada ni celle du formulaire AH-223 du ministère de la Santé et des Services sociaux employée à l’interne4. En aucun cas, ce formulaire allégé ne pourrait être utilisé si un patient était touché.
La communication doit respecter les délais de notification établis par le fournisseur. Après examen des différentes politiques et procédures des compagnies, il a été conclu que les dommages visibles le jour de la livraison doivent être signalés idéalement le jour même, tandis que les dommages découverts au moment de l’utilisation seulement doivent être signalés dans les deux jours suivant leur découverte5–9.
Une copie du courriel doit être conservée pour permettre un suivi hebdomadaire plus efficace. Les compagnies répondent généralement dans un délai de sept à quatorze jours ouvrables. Au besoin, copier le responsable des approvisionnements du centre hospitalier sur le courriel adressé à la compagnie pour qu’il fasse le suivi, le cas échéant (p. ex. : lors du remplacement des médicaments ou des fournitures). Toutefois, dans la majorité des cas, il ne s’agit que de quelques articles défectueux, et sa participation est alors moins pertinente.
Dès réception du formulaire de déclaration de fournitures pharmaceutiques défectueuses, le service à la clientèle de la compagnie traite en principe la demande. En fonction de la situation, la compagnie peut habituellement proposer trois options : un remboursement complet du prix d’achat, un remplacement par un produit en bon état ou aucune action. Il est important de noter que certaines compagnies peuvent demander des détails concernant la valeur du produit défectueux. La compagnie fournira un numéro d’autorisation de retour de marchandise (ARM) uniquement si elle accepte la demande de retour, et le produit doit être retourné, en règle générale, conformément aux instructions fournies par le service à la clientèle de la compagnie, dans les quatorze jours suivant la réception de ce numéro d’ARM.
En ce qui concerne les retours autorisés par les compagnies, ils se divisent en plusieurs catégories, notamment les erreurs d’expédition de la compagnie ou du grossiste fournisseur, les dommages visibles (produits présentant des dommages évidents à la livraison), et les dommages cachés (produits dont les dommages ne sont visibles que lors de l’utilisation)4–8. Il est important de préciser que la décision finale d’autorisation de retour reste à l’entière discrétion de la compagnie.
D’un autre côté, il y a des retours non autorisés selon les normes des compagnies, notamment les retours n’ayant pas reçu de numéro d’ARM, les produits achetés par «commande spéciale» ou non remboursables, les produits périmés (habituellement plus de six mois après la date de péremption indiquée sur l’emballage), les produits hors de leur emballage d’origine ou dont l’étiquette d’origine a été retirée, les produits qui ne sont plus commercialisés par la compagnie, ceux qui ont été endommagés par le client ou en raison d’erreurs du client, les produits abîmés par l’eau ou le feu, les produits inadéquatement manutentionnés, conservés ou entreposés, les produits retournés à la compagnie plus de trente jours après la date d’émission du numéro d’ARM et, enfin, ceux ayant une courte date de péremption acceptée au préalable par le client5–9.
Sur les quatre semaines de durée du projet, la première a été consacrée à la création du formulaire (en annexe), tandis que la deuxième et la troisième l’ont été à la conception initiale et à la révision de la procédure de gestion des défectuosités de fournitures pharmaceutiques.
Ces deux documents ont pour objectif de simplifier la communication et la gestion au sein du Département de pharmacie en cas de produits défectueux, permettant ainsi une coordination plus structurée des activités. Ils ont également pour but de faciliter la communication avec les compagnies, réduisant par le fait même la nécessité d’échanges de courriels incessants. Cette approche est susceptible de conduire à une meilleure notification des défectuosités, à une diminution des risques pour les patients et le personnel, à une amélioration de la qualité des soins avec une utilisation plus efficiente des ressources hospitalières. Elle permet aux compagnies pharmaceutiques et de fournitures connexes de mieux connaître les problèmes de leurs clients et ainsi de mieux y répondre.
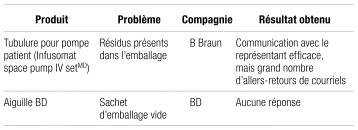
Néanmoins, le principal obstacle rencontré résidait souvent dans la lenteur administrative liée à la communication avec les compagnies. Au cours des quatre semaines du projet, huit compagnies ont été contactées une première fois par courriel et seulement trois ont répondu. Après un second courriel de rappel, une compagnie supplémentaire a finalement répondu. Cette inefficacité dans les échanges administratifs peut entraver la résolution rapide des problèmes liés aux fournitures pharmaceutiques et décourager complètement le processus de déclaration, posant ainsi un défi à la gestion de la défectuosité. Deux exemples se sont produits lors de la réalisation du projet et sont présentés dans le tableau 1.
Les hôpitaux sont l’un des piliers du système de santé, et la qualité des fournitures pharmaceutiques qu’ils utilisent revêt une importance pour la santé et le bien-être de la population. Le formulaire de déclaration des fournitures pharmaceutiques défectueuses joue un rôle intéressant dans cette démarche, car il constitue un outil structuré et simple d’emploi pour identifier, signaler et gérer les fournitures pharmaceutiques présentant des problèmes. En facilitant une communication claire et systématique avec les fournisseurs, il permet de s’occuper rapidement des produits défectueux et aux compagnies de prendre des mesures correctives immédiates pour réduire les risques pour les patients ou le personnel.
Tableau I Défectuosités rencontrées spécifiquement durant la période de stage

Les avantages de cette démarche s’étendent au-delà de la simple communication avec les fournisseurs, en retenant des éléments clefs qui méritent une attention détaillée :
Et il faut rappeler que le formulaire est conçu pour un usage exclusif en pharmacie, et uniquement pour les fournitures défectueuses. Il ne signale donc que des défectuosités sporadiques. Un autre formulaire, comme celui présenté à la figure 2 en annexe, doit être employé pour demander un changement complet de produit lorsque cette dernière ne convient plus. Enfin, le service des approvisionnements a lancé un nouveau formulaire informatisé, pendant que le présent article était en révision, dont le but est exactement le même, soit la déclaration des défectuosités, ce qui montre le bien-fondé et l’utilité de la démarche. Les deux formulaires sont relativement semblables dans l’ensemble. Le département de pharmacie continuera d’utiliser son propre formulaire pour toutes les fournitures pharmaceutiques qu’il achète lui-même, permettant un meilleur encadrement du dossier.
La création d’un formulaire de déclaration de fournitures pharmaceutiques défectueuses représente un atout pour l’amélioration de la pratique hospitalière et la sécurité des patients. Il favorise une communication structurée, la réactivité face aux problèmes et la mise en œuvre de mesures correctives, tout en renforçant la culture de la sécurité au sein de l’établissement de santé. Les avantages englobent la réduction des risques, l’amélioration de la qualité des soins et une gestion plus efficace des dispositifs pharmaceutiques, contribuant ainsi à une meilleure prise en charge des patients et à une pratique médicale de grande qualité. Reste à voir si un tel outil pourra être mis en place dans nos établissements, si son utilisation pourra se maintenir, et si une version informatisée sera généralisée.
Cet article comporte une annexe; elle est disponible sur le site de Pharmactuel ( www.pharmactuel.com ).
Les auteurs n’ont déclaré aucun financement pour le présent article.
Tous les auteurs ont soumis le formulaire de l’ICMJE sur la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts lié au présent article.
Les auteurs remercient les ATSP du CHU Sainte-Justine qui ont partagé leurs avis et ont contribué à la réalisation du projet. Un remerciement est également adressé au GTPS de l’A.P.E.S. pour son soutien dans l’élaboration de la procédure de gestion des défectuosités de fournitures pharmaceutiques et l’ajout de cette procédure dans leur boîte à outils.
1. Santé Canada Guidance on Mandatory Reporting for Hospitals. (Juin 2019) [en ligne]. https://www.canada.ca/content/dam/hc-sc/documents/services/drugs-health-products/medeffect-canada/adverse-reaction-reporting/drugs-devices/guidance/Mandatory-reporting-hospitals-fra.pdf (site visité le 12 octobre 2023).
2. Health Product Regulation Portal. Government of Canada. Formulaire de déclaration des effets indésirables des dispositifs médicaux. (Date de modification : 2021-07-14). [en ligne] https://hpr-rps.hres.ca/side-effects-reporting-form.php?form=medical_devices&lang=fr (site visité le 12 octobre 2023).
3. Règlement sur les produits dangereux, DORS/2015-17 (15 décembre 2022). [en ligne] https://www.laws-lois.justice.gc.ca/fra/reglements/DORS-2015-17/ (site visité le 12 octobre 2023).
4. Gouvernement du Québec. Rapport de déclaration d’incident ou d’accident. AH-233-1_DT9034 (2021-02). [en ligne] http://msssa4.msss.gouv.qc.ca/intra/formres.nsf/c6dfb077f4130b4985256e38006a9ef0/d11170ca3d62f0be85257ca2005faf94/$FILE/AH-223-1_DT9034%20(2021-02)%20aper%C3%A7u.pdf (site visité le 26 janvier 2025).
5. Ansell. Electrical resistance (2024 Ansell). [en ligne]. https://www.ansell.com/ca/fr/hazards/electrical-resistance (site visité le 5 octobre 2023).
6. Baxter Canada. Terms and Conditions (Mars 2019). [en ligne] https://www.baxter.ca/sites/g/files/ebysai1431/files/2019-03/terms_and_conditions_FR.PDF (site visité le 5 octobre 2023).
7. BD. Formulaire plainte de produit (15 juillet 2020). [en ligne] https://www.bd.com/fr-ca/customer-support/product-incident-report (site visité le 5 octobre 2023).
8. BD. Infection Prevention Product Catalog (15 juillet 2020). [en ligne] https://www.bd.com/a/80755 (site visité le 5 octobre 2023).
9. Fresenius Kabi. Politique de retour de produits. (1er janvier 2023) [en ligne] https://www.fresenius-kabi.com/fr-ca/documents/Returned-Goods-Policy-FR-020423.pdf (site visité le 5 octobre 2023).
Pour toute correspondance : Jean-Marc Forest, Centre hospitalier universitaire Sainte-Justine, 3175, chemin de la Côte-Sainte-Catherine, Montréal (Québec) H3T 1C5, CANADA; téléphone : 514 345-4603; courriel : jean-marc.forest.hsj@ssss.gouv.qc.ca
PHARMACTUEL, Vol. 58, No. 1, 2025