
Bianca Beloin Jubinville1, B.Pharm., M.Sc., BCPS, MBA, Audrey-Anne Longpré1, Pharm.D., M.Sc., Nicolas Goettel1, Pharm.D., M.Sc., Jocelyn Dion1, B.Pharm., M.Sc., Mélanie Gilbert1, B.Pharm., M.Sc., Lorraine Legeleux1, Pharm.D., M.Sc., Marie-France Beauchesne1-3, B.Pharm., M.Sc., Pharm.D.
1Pharmacien(ne), Centre intégré universitaire de santé et de services sociaux de l’Estrie–Centre hospitalier universitaire de Sherbrooke, Sherbrooke (Québec) Canada;
2Professeure titulaire de clinique, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
3Chercheuse associée, Centre de recherche du Centre hospitalier universitaire de Sherbrooke, Sherbrooke (Québec) Canada
Reçu le 22 mai 2024; Accepté après révision par les pairs le 25 mars 2025
https://doi.org/10.63209/2025.1546
Résumé
Objectif: Évaluer la conformité de l’usage du voriconazole selon les doses recommandées en mg/kg et selon l’atteinte des concentrations sériques visées.
Méthode: Étude descriptive rétrospective portant sur la conformité des ordonnances de voriconazole aux critères établis par l’équipe de pharmaciens en infectiologie à partir des données probantes. Les informations sur les patients ont été collectées dans les dossiers médicaux des adultes admis au Centre intégré universitaire de santé et de services sociaux de l’Estrie–Centre hospitalier universitaire de Sherbrooke ayant reçu du voriconazole en cours d’hospitalisation entre le 1er janvier 2015 et le 31 décembre 2019.
Résultats: Les 98 sujets de l’étude étaient âgés en moyenne de 63,2 ans et 58 % d’entre eux présentaient une maladie hématologique ou oncologique. Les taux de conformité étaient de 71 % pour la dose de charge et de 89,8 % pour la dose de maintien. Pour les patients ayant un indice de masse corporelle supérieur à 30, le taux de conformité diminuait cependant à 65 % dans les deux cas. Une mesure de la concentration sérique a été effectuée chez 61 sujets (60,7 % des valeurs se situaient dans l’intervalle thérapeutique) et n’était pas indiquée chez 31 sujets. L’ajustement des doses respectait l’algorithme trouvé dans la littérature dans 66 % des cas. Au moins un effet indésirable a été observé chez 12 % des patients, majoritairement de l’hépatotoxicité.
Conclusion: La dose de maintien du voriconazole de même que les concentrations sériques des patients du Centre intégré universitaire de santé et de services sociaux de l’Estrie–Centre hospitalier universitaire de Sherbrooke sont adéquates. Par contre, une amélioration de la dose de charge, de la dose maintien utilisée chez les patients ayant un indice de masse corporelle supérieur à 30 et de la surveillance de l’innocuité serait souhaitable.
Mots clés: antifongique, azoles, concentration sérique, voriconazole
Abstract
Objective: To evaluate the compliance of voriconazole use with the recommended doses in mg/kg and with the achievement of target serum concentrations.
Method: A retrospective descriptive study assessing the compliance of voriconazole prescriptions with criteria established by the infectious diseases pharmacy team based on evidence-based data. Patient information was collected from the medical records of adults admitted to the Centre intégré universitaire de santé et de services sociaux de l’Estrie-Centre hospitalier universitaire de Sherbrooke who received voriconazole during hospitalization between January 1, 2015, and December 31, 2019.
Results: The 98 study subjects had a mean age of 63.2 years, and 58% had a hematologic or oncologic disease. Compliance rates were 71% for the loading dose and 89.8% for the maintenance dose. However, for patients with a body mass index over 30, compliance dropped to 65% in both cases. Serum concentration measurements were performed in 61 subjects (60.7% of values were within the therapeutic range) and were not indicated in 31 subjects. Dose adjustments followed the algorithm found in the literature in 66% of cases. At least one adverse effect was observed in 12% of patients, mostly hepatotoxicity.
Conclusion: The maintenance dose of voriconazole and the serum concentrations of patients at the Centre intégré universitaire de santé et de services sociaux de l’Estrie-Centre hospitalier universitaire de Sherbrooke are adequate. However, improvements in the loading dose, maintenance dose, and safety monitoring for patients with a body mass index over 30 would be desirable.
Keywords: antifungal, azoles, serum concentration, voriconazole
This abstract was translated using Microsoft 365 Copilot and subsequently reviewed by the editorial team.
Les infections fongiques invasives comme l’aspergillose sont associées à une morbimortalité élevée1. Les antifongiques azolés représentent une option de traitement avantageuse en raison de leur facilité d’administration (puisqu’ils sont offerts en plusieurs formes), de leur large spectre d’action et de leur bonne tolérance. Malgré l’arrivée de l’isavuconazole (qui cause moins d’effets indésirables et d’interactions médicamenteuses), le voriconazole constitue toujours un traitement de première intention, notamment pour l’aspergillose invasive2. En raison de la pharmacocinétique non linéaire de type Michaelis-Menten et de la variabilité intra-et inter-individuelle importante du voriconazole, les concentrations sériques doivent être surveillées pour atteindre les cibles thérapeutiques1–4.
L’atteinte des concentrations sériques visées nous permet d’espérer une meilleure réponse au traitement, tout en limitant les effets indésirables. Plusieurs études ont montré une corrélation entre les concentrations sériques au creux du voriconazole, d’une part, et l’efficacité clinique et la toxicité, d’autre part. Une diminution des arrêts de traitement dus aux effets indésirables et une meilleure réponse au traitement ont été associées à la surveillance des concentrations sériques de voriconazole5. L’intervalle thérapeutique souhaité varie légèrement selon les références consultées. Un intervalle de 1 à 5,5 μg/mL a été retenu pour la présente étude1,3,6. Certains facteurs de risque, tels que l’hypo-albuminémie, le jeune âge ou la présence d’un cancer hématologique, ont été associés à des concentrations non conformes6,7. Cependant, peu d’études comptaient une population comparable à la patientèle québécoise, à l’exception de l’étude de Flores et coll., menée à Toronto, qui regroupait toutefois exclusivement des patients souffrant de cancers hématologiques8. Effectivement, dans la plupart des autres études, les sujets étaient d’origine asiatique et présentaient donc des différences importantes sur le plan du métabolisme hépatique du voriconazole. Ils étaient ainsi plus nombreux à être des métaboliseurs lents de l’isoenzyme CYP2C19 du cytochrome P450, la voie principale d’élimination du voriconazole2,6.
Selon une publication de l’Institut national de santé publique du Québec (INSPQ), l’allèle le plus commun de l’isoenzyme CYP2C19 chez les métaboliseurs lents est l’allèle *2, présent chez environ 15 % des personnes blanches, mais chez jusqu’à 35 % des personnes asiatiques9. De plus, jusqu’à 8,9 % de la population asiatique possède l’allèle *3, généralement peu fréquente dans la population (moins de 1 %) et qui entraîne une activité réduite, voire aucune activité. L’aire sous la courbe du voriconazole peut être significativement augmentée chez ces métaboliseurs lents qui sont ainsi exposés à un risque potentiellement plus élevé d’effets indésirables10. La proportion attendue de ces métaboliseurs lents est plutôt faible dans notre région, puisque les Canadiens d’origine asiatique représentent 17,7 % de la population, selon le recensement de 2016, et résident en grande partie (75 % d’entre eux) en Ontario et en Colombie-Britannique11.
Plusieurs différences de pratique sont également mentionnées, en particulier en ce qui a trait à la dose utilisée pour l’administration par voie orale, soit une dose de maintien ajustée selon le poids à 4 mg/kg/dose ou une dose fixe. Toutefois, aucune étude n’évalue ces différences de pratique. Pour le calcul des doses chez les personnes obèses, certains auteurs recommandent de prendre le poids ajusté chez les patients présentant un indice de masse corporelle (IMC) de plus de 30 plutôt que le poids réel afin de réduire au minimum les risques de toxicité3. L’utilisation d’un IMC de plus de 30 comme critère d’ajustement des doses pour les personnes obèses est conforme aux pratiques locales du Centre intégré universitaire de santé et de services sociaux de l’Estrie–Centre hospitalier universitaire de Sherbrooke (CIUSSS de l’Estrie–CHUS), bien que d’autres auteurs suggèrent un IMC de plus de 35 pour l’ajustement des doses chez cette patientèle3.
L’accès limité à la mesure des concentrations sériques au Québec mène à un délai dans l’ajustement des doses de voriconazole. Comme l’analyse des prélèvements est faite dans un centre suprarégional, on observe souvent des délais de plusieurs jours à plusieurs semaines entre l’envoi du spécimen, son analyse et la réception des résultats, puisque toutes ces étapes ne sont pas effectuées quotidiennement.
Aucune étude n’a décrit l’usage du voriconazole en situation réelle au Québec ni la conformité des ordonnances selon des critères factuels. Il importe donc d’explorer l’utilisation réelle (dose prescrite en mg/kg, concentration sérique obtenue, délai d’obtention des résultats, puis d’ajustement) comparativement aux recommandations d’experts afin de mieux la décrire et d’être en mesure d’y apporter des correctifs, le cas échéant.
Tableau I Critères de conformité à l’usage du voriconazole

L’objectif principal de cette étude descriptive rétrospective était d’évaluer, chez les adultes hospitalisés au CIUSSS de l’Estrie–CHUS (Hôpital de Fleurimont et Hôtel-Dieu), la conformité de l’usage du voriconazole selon les doses initiales recommandées, l’atteinte des concentrations sériques visées et le suivi pendant le traitement. La conformité a été évaluée selon les critères de bon usage établis par l’équipe de pharmaciens en infectiologie à partir des données probantes existantes (tableau I). L’objectif secondaire était de décrire l’usage du voriconazole selon les caractéristiques des patients, l’intention thérapeutique, la survenue d’effets indésirables, les ajustements de doses en réponse aux concentrations sériques, les délais pour la mesure des concentrations sériques et l’obtention du résultat.
Cette étude a été approuvée par le Comité d’éthique et de la recherche du CIUSSS de l’Estrie–CHUS. Les données extraites ont été dénominalisées et consignées dans un fichier Excel à accès sécurisé.
Les personnes de 18 ans et plus hospitalisées au CIUSSS de l’Estrie–CHUS (Hôpital de Fleurimont et Hôtel-Dieu) ayant reçu une prescription et au moins deux doses de voriconazole pendant leur hospitalisation entre le 1er janvier 2015 et le 31 décembre 2019 ont été incluses dans l’étude. Si un même sujet répondant aux critères avait été hospitalisé plus d’une fois pendant la période de l’étude, seule la première hospitalisation était retenue.
Le logiciel d’antibiogouvernance APSS a été utilisé afin de trouver les personnes admissibles. Leurs dossiers médicaux ont ensuite été consultés afin d’évaluer leur admissibilité.
Les données ont été collectées à partir du dossier clinique informatisé. Les variables permettant de décrire les caractéristiques démographiques des sujets ont été recensées : âge, sexe, poids, taille, surface corporelle et IMC au premier jour de traitement de voriconazole ou selon la donnée la plus près qui précédait le premier jour du traitement. Ensuite, les maladies concomitantes pouvant avoir un effet sur les concentrations sériques obtenues ont été considérées : cancer hématologique ou atteinte d’un organe solide sous-jacent avec métastases ou non, neutropénie, fibrose kystique, hypo-albuminémie ou insuffisance hépatique, quelle que soit la gravité. Les effets indésirables ont été recueillis à partir de la feuille sommaire d’hospitalisation, des examens cliniques, des analyses de laboratoire et des notes d’évolution lors de l’hospitalisation : hausse des enzymes hépatiques (alanine aminotransférase (ALT), aspartate transaminase (AST) ou phosphatase alcaline à plus de 3 fois la limite supérieure à la normale, bilirubine à plus de 1,5 fois la limite supérieure à la normale), hausse de la créatinine sérique, réaction indésirable cutanée ou ophtalmique et allongement de l’intervalle QT corrigé (QTc). Ensuite, les valeurs de laboratoire suivantes ont été obtenues au premier jour de l’administration de voriconazole ou dès que possible après le début du traitement : créatinine sérique, débit de filtration glomérulaire estimé (DFGe), albumine sérique, AST, ALT, bilirubine totale, phosphatase alcaline et gamma-glutamyl-transférase (GGT). Concernant les concentrations sériques de voriconazole, toutes les valeurs d’un patient au cours de l’hospitalisation ont été colligées. Quant aux valeurs du bilan hépatique et de la fonction rénale, elles ont été notées en cours de traitement pour les patients présentant une concentration supra-thérapeutique (supérieure à 5,5 μg/mL) ou un effet indésirable consigné sur la feuille sommaire. La collecte de données a permis de recueillir l’information sur la prise concomitante d’anti-infectieux afin de décrire la complexité du traitement anti-infectieux chez les sujets à l’étude, de même que la dose de voriconazole utilisée, la voie d’administration et les changements de doses subséquents. Enfin, le contexte de prescription, soit la présence ou non du patient aux soins intensifs au moment de l’instauration du traitement à l’étude ainsi que la durée du séjour aux soins intensifs (s’il y a lieu) et la durée totale de l’hospitalisation ont été consignées.
Des analyses descriptives ont été effectuées. Les caractéristiques des sujets ont été présentées en proportions (avec l’étendue) et en moyennes (avec l’écart type) selon qu’il s’agissait de variables nominales ou continues, respectivement.
La conformité des variables suivantes a été évaluée pour toutes les ordonnances de voriconazole : dose de charge, dose de maintien, obtention d’une concentration sérique entre le 4e et le 7e jour de traitement, ajustement de dose s’il y a lieu et suivi (tableau I). Une proportion a été calculée pour chaque critère de conformité.
Du 1er janvier 2015 au 31 décembre 2019, au total, 98 patients hospitalisés au CIUSSS de l’Estrie–CHUS ont reçu du voriconazole pendant au moins 24 heures (2 doses). Ils ont tous été inclus dans la présente analyse.
Les données descriptives sont détaillées dans le tableau II. L’âge moyen des patients était de 63,2 ans, l’écart allant de 19 à 85 ans. L’IMC médian était de 25, le poids des sujets variant de 38 kg à 170 kg (23 % des patients avaient un IMC supérieur à 30). La majorité des sujets (58 %) présentait une maladie hématologique ou oncologique, dont 24 % étaient neutropéniques au moment de la prise du voriconazole. Quant à la prise concomitante d’autres anti-infectieux, 82 % des patients prenaient au moins un autre agent et sept en prenaient même jusqu’à quatre. Le plus fréquent (10,1 %) était le méropénem. La plupart des sujets avaient une fonction rénale normale (seuls 25 % avaient une clairance de la créatinine inférieure à 50 mL/min) et hépatique adéquate (un seul patient était en insuffisance hépatique, selon la catégorie B de la classification de Child-Pugh). L’intention thérapeutique a été établie chez seulement 40 % des sujets et était clairement inscrite au dossier clinique informatisé ou dans les notes d’évolution à l’instauration du voriconazole. Un agent pathogène a été trouvé chez 45 % des sujets. Un effet indésirable a été noté chez 12 % des patients (surtout de l’hépatotoxicité, mais aussi un cas de toxicité cutanée [photosensibilité avec érythème facial] et un cas de neurotoxicité [hallucinations]). En ce qui concerne les délais, la médiane était de six jours entre le dosage sérique et l’obtention du résultat par télécopieur du laboratoire d’analyse. À cela s’ajoute un délai médian de trois jours pour l’inscription de ce résultat dans le dossier clinique informatisé local.
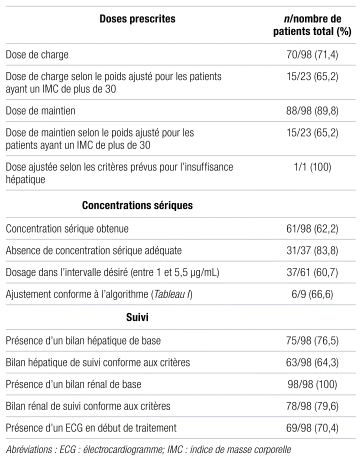
La conformité de l’usage du voriconazole est décrite dans le tableau III. Soixante-dix (71 %) patients ont reçu les deux doses de charge conformément au critère défini. Parmi les usages non conformes, neuf patients ayant reçu des doses de charge supérieures à la dose définie et 17 n’ont pas eu de dose de charge. La conformité de la dose de maintien se situe à 89,8 % pour l’ensemble des sujets. Parmi les patients ayant un IMC supérieur à 30, la conformité des doses de charge et de maintien baisse à 65 % avec l’utilisation du poids ajusté, tant pour les patients ayant reçu des doses trop faibles que trop élevées. Par contre, la non-conformité est plus prévalente pour la dose de charge (12 patients sur 23) que pour la dose de maintien (6 patients sur 23).
Quant à la conformité des concentrations sériques atteintes, les recommandations indiquent de viser un creux sérique de voriconazole (prélèvement entre le 4e et le 7e jour de traitement) entre 1 et 5,5 μg/mL. La concentration sérique de voriconazole a été mesurée au moins une fois chez 62 % des sujets, et ces mesures étaient effectuées au bon moment. Parmi les sujets n’ayant pas eu de mesure de la concentration sérique, il était adéquat de ne pas en faire chez 84 % d’entre eux, puisque le traitement de voriconazole a été cessé avant le 4e jour. Parmi les 61 dosages faits après l’instauration du traitement, 37 (61 %) étaient dans les cibles, 13 (21 %) étaient sous-thérapeutiques et 11 (18 %) étaient supra-thérapeutiques. Des 24 dosages hors cibles, l’arrêt du traitement avait déjà eu lieu chez 17 patients au moment de la réception du résultat. Les sept patients hors cibles restants, en plus de deux aux concentrations thérapeutiques, ont bénéficié d’un ajustement de la dose dont la conformité était de 66 % par rapport à l’algorithme proposé. Quant aux concentrations sériques obtenues, il est intéressant de constater que la médiane des valeurs obtenues dans la présente analyse était de 3,43 μg/mL (étendue : de 0,12 à 14,91), ce qui se situe dans l’intervalle visé. Enfin, la conformité du suivi s’établit à 64 % pour les enzymes hépatiques, à 80 % pour la fonction rénale et les électrolytes et à 70 % pour l’intervalle QTc.
Tableau II Description de la population étudiée
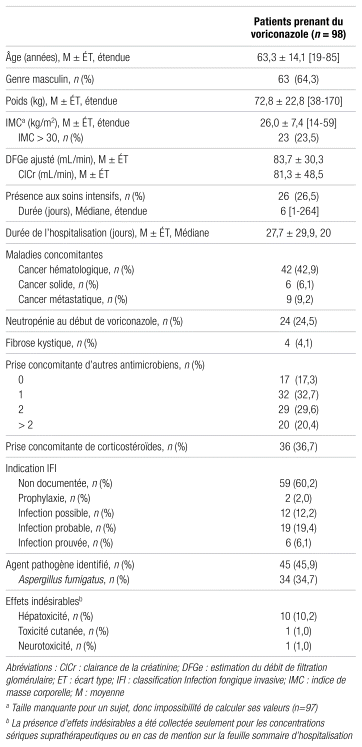
Tableau III Résultats de conformité aux critères
Cette évaluation permet aux cliniciens de cibler des pistes d’amélioration dans l’usage du voriconazole chez les patients admis au CIUSSS de l’Estrie–CHUS (Hôpital de Fleurimont et Hôtel-Dieu) et potentiellement de réduire les risques d’effets indésirables associés, tout en augmentant l’efficacité. Les résultats obtenus semblent indiquer que la conformité de la dose de maintien du voriconazole et l’obtention de concentrations sériques chez les sujets sont adéquates au CIUSSS de l’Estrie–CHUS. En revanche, une amélioration de la dose de charge et de celle utilisée chez les patients ayant un IMC supérieur à 30 de même que des suivis de l’utilisation du voriconazole serait souhaitable.
La proportion de patients ayant reçu une dose de charge conforme s’est avérée inférieure à 80 % (71 %), 11 % ayant eu une dose trop élevée et près de 20 % n’en ayant eu aucune. Par contre, parmi ceux qui n’ont pas eu de dose de charge, il est impossible d’exclure le fait que le traitement ait commencé préalablement en externe et donc que cette dose n’était pas nécessaire. À l’exclusion de ces patients, on observe plutôt une conformité de 88,6 %, comparable au résultat de 91,1 % de Flores et coll.8. Par ailleurs, pour les patients ayant reçu des doses trop élevées, il est probable que la dose de charge standard (400 mg) ait été prescrite quand leur poids se situait sous 55 kg, ce qui les classait d’emblée parmi les cas non conformes. Ces observations sont rassurantes dans le contexte où le taux de conformité était inférieur au résultat attendu.
Pour la dose de maintien, malgré des recommandations posologiques possibles à doses fixes, la pratique locale semble plutôt favoriser l’ajustement de la dose selon le poids, peu importe la voie d’administration. La conformité obtenue (89,8 %) vient confirmer cette pratique. Ces données sont semblables à celles de l’étude descriptive de Yi et coll. qui a mentionné le recours à des doses de voriconazole calculées en mg/kg se rapprochant des recommandations de 8 mg/kg/jour, soit 7,76 et 8,48 pour chacun des deux groupes à l’étude13. Les études descriptives de Dote et coll. et de Cheng et coll. sur des populations asiatiques ont spécifié que les doses moyennes qu’ont reçues les patients étaient beaucoup plus faibles (de 5,5 mg/kg/jour et de 7 mg/kg/jour, respectivement)14,15. Une tendance à utiliser une dose plus faible chez les patients plus âgés (plus de 60 ans) est également observée dans l’étude de Cheng et coll.15.
La faible conformité des doses de charge et de maintien chez les patients ayant un IMC supérieur à 30 s’étant traduite par l’administration de doses trop élevées soulève, quant à elle, des pistes d’amélioration. Aucune donnée comparative n’a été trouvée dans la littérature spécifiquement pour les patients obèses. Par ailleurs, seulement 23 % des sujets de notre étude avaient un IMC supérieur à 30. Il faut cependant être plus attentif à la prescription de voriconazole chez ces patients et mieux consigner les motifs ayant mené au choix d’une dose hors critères. L’utilisation du poids de dosage pour la détermination de la dose de voriconazole, qui demeure une avenue encore méconnue, serait également à privilégier.
Le nombre de prélèvements sériques chez 62 % des sujets de notre étude était comparable aux résultats d’Ostrosky-Zeichner et coll., une étude observationnelle d’un peu plus de 2000 patients prenant des azoles aux États-Unis, dont 491 prenant du voriconazole16. Les auteurs ont suivi les concentrations sériques chez 54 % de leurs patients prenant du voriconazole. Notre résultat de 62 % obtenu est d’autant plus rassurant qu’il était adéquat de ne pas faire de prélèvement chez la majorité de ceux qui n’en ont pas eu (84 %), le voriconazole ayant déjà été cessé au moment de faire ces analyses. L’étude d’Ostrosky-Zeichner et coll. couvre une période semblable à la nôtre (de mars 2017 à avril 2020) et a été menée dans un pays aux pratiques ressemblant aux nôtres étant donné l’utilisation de lignes directrices similaires, soit celles de l’Infectious Diseases Society of America16,17. Ces similitudes permettent plus aisément de comparer nos résultats aux leurs. En ce qui concerne les valeurs sériques, Ostrosky-Zeichner et coll. ont obtenu une médiane de 2,3 μg/mL (minimum 0, maximum 17,8) comparable à notre résultat (3,43 μg/mL) dans une population nord-américaine16. Le poids des patients et la dose utilisée n’apparaissent pas dans la publication d’Ostrosky-Zeichner et coll. On ne peut donc pas comparer ces résultats16. Par contre, dans l’étude de Flores et coll., la concentration sérique moyenne était de 3,2 μg/mL chez des sujets de corpulence semblable, ce qui renforce la validité de nos résultats8.
Malgré la pharmacocinétique imprévisible du voriconazole nécessitant des ajustements de doses fort probables en cours de traitement, peu de références fournissent un guide d’ajustement concret selon les concentrations sériques obtenues. Une seule recommandation a été trouvée dans la littérature à ce sujet2. Même si cet algorithme est méconnu des cliniciens, les ajustements de dose faits à la suite d’une valeur non thérapeutique correspondent aux ajustements proposés dans l’algorithme et dans 66 % des cas. Ce guide d’ajustement reflète donc les changements effectués dans la pratique réelle et s’avère intéressant à considérer pour des cliniciens inexpérimentés.
Concernant la description des caractéristiques des patients ayant reçu du voriconazole, peu de données d’utilisation en contexte clinique réel ont été publiées, à l’exception de l’analyse d’Ostrosky-Zeichner en 2022 et de l’étude récente de Toronto8,16. L’âge moyen des patients était comparable (63,3 dans notre étude contre 55 et 60 ans, dans les deux autres études ci-haut mentionnées respectivement) bien que notre étude excluait les enfants contrairement à l’étude d’Ostrosky-Zeichner (3 % des sujets)16. La proportion de sujets ayant une maladie concomitante hématologique ou oncologique était aussi semblable dans l’étude d’Ostrosky-Zeichner (58 contre 55 %), ce qui augmente la validité externe de cette analyse. Par contre, dans l’étude de Flores et coll., la maladie hématologique constituait un critère d’inclusion. Les sujets étaient donc différents des nôtres8. Par ailleurs, la proportion de patients neutropéniques était plus importante (41,5 %) dans l’étude d’Ostrosky-Zeichner et coll. que dans la nôtre16. Le manque d’information sur le poids et la taille des patients dans l’étude d’Ostrosky-Zeichner est également déplorable, car il existe peu de données sur l’utilisation en contexte de pratique réelle dans une population nord-américaine16. Les patients inclus dans l’étude de Flores et coll. présentent quant à eux un poids moyen comparable à celui de nos patients (73,9 contre 72,8 kg) bien que la proportion de patients ayant un IMC de plus de 30 ne soit pas connue8.
Il est intéressant de constater que l’intention thérapeutique n’a fréquemment pas été consignée dans le dossier clinique des patients prenant du voriconazole (60 %). Malgré tout, un agent pathogène a été plus souvent trouvé (45 %) chez les patients québécois que dans l’étude américaine (10 %). Nous disposons de peu d’informations pour expliquer cette différence16.
Une forte analogie avec l’étude d’Ostrosky-Zeichner est notée quant aux effets indésirables survenus chez les patients recevant du voriconazole16. En effet, 14,2 % des patients d’Ostrosky-Zeichner ont connu des effets indésirables contre 12,2 % des nôtres16. Ces résultats concordent aussi avec les données de la monographie du voriconazole et confirment donc les informations recueillies dans les études initiales12. Plus spécifiquement, l’hépatotoxicité a été signalée chez 10,2 % de nos sujets comparativement à 8,1 % des sujets de l’étude américaine. Ces données nous incitent à réfléchir à des pistes d’amélioration de la pratique étant donné le faible taux de conformité du suivi des enzymes hépatiques (64 %) en situation de pratique courante au CIUSSS de l’Estrie–CHUS. Une contribution des pharmaciens en antibiogouvernance nous semble une avenue intéressante pour assurer un suivi plus systématique pour la sécurité des patients. Les mesures de l’intervalle QTc et de la fonction rénale devraient aussi figurer dans ce suivi méthodique puisque les données relevées dans le cadre de notre étude montrent un manque de conformité aux recommandations. Flores et coll. ont noté, de leur côté, des effets indésirables chez 41,1 % des patients, ce qui est significativement plus élevé8. Il convient par contre de se rappeler que la population étudiée était composée exclusivement de patients atteints d’un cancer hématologique et donc plus fragiles, ce qui explique sans nul doute une partie de la différence observée.
Enfin, concernant le délai de traitement des prélèvements et d’obtention des résultats de dosages sériques, une meilleure connaissance des pratiques en place pourrait en premier lieu contribuer à le réduire par une planification plus optimale des dosages requis. Les moments optimaux du prélèvement et les journées d’envoi des prélèvements au centre externe devraient être inscrits au dossier clinique informatisé pour guider le prescripteur lors de la planification du dosage sérique. Une sensibilisation de l’équipe du laboratoire de biochimie à l’inscription rapide des résultats obtenus du centre externe d’analyse permettrait assurément une optimisation plus rapide du traitement. Selon les données recueillies, il peut s’écouler 9 jours entre le prélèvement d’un échantillon et l’inscription d’un résultat au dossier clinique informatisé, un délai inacceptable pour les patients en situation de sur- ou de sous-dose. Les cliniciens devraient être encouragés à consulter le dossier Santé Québec des patients afin d’éviter de tels retards.
À noter que malgré les interactions multiples avec le voriconazole, cet aspect n’a pas été évalué dans la présente analyse. En effet, presque toutes les interactions entraînent un effet sur l’autre médicament, et non sur le voriconazole, ce qui limite l’intérêt d’inclure ce paramètre dans la présente étude. Néanmoins, à la lumière des résultats de Flores et coll., il aurait été intéressant d’évaluer la prise concomitante d’inhibiteurs de la pompe à protons susceptibles d’augmenter la concentration de voriconazole8,12. Malgré tout, la proportion de patients ayant une concentration sérique dans l’intervalle thérapeutique était semblable chez les patients prenant ou non des inhibiteurs de la pompe à protons8.
La présente étude possède certaines limites. En premier lieu, un changement de pratique depuis la période analysée est possible puisque l’isavuconazole a été commercialisé et a obtenu des critères de remboursement facilitant son utilisation depuis 2020. Bien que cette dernière molécule soit souvent mieux tolérée et comporte moins de variabilité pharmacocinétique, le voriconazole demeure un premier choix dans le traitement de l’aspergillose. Les recommandations sur les doses et le suivi recommandés restent inchangées. Ensuite, on ne peut exclure la possibilité que certains des patients admis à l’hôpital avaient commencé un traitement de voriconazole en externe, ce qui a pu biaiser l’analyse de la conformité à la dose de charge. Comme l’analyse des données n’a été effectuée que pour un seul centre, nos résultats pourraient ne pas être généralisables à d’autres régions ou à d’autres types de centres en raison de données épidémiologiques différentes, de variations entre les hôpitaux ou de lignes directrices distinctes, notamment chez les sujets obèses. La collecte rétrospective des données, à partir des dossiers médicaux, a pu influencer la qualité et la quantité des données recensées. Enfin, la proportion importante de patients (31,6 %) ayant reçu le voriconazole pendant moins de 4 jours limite la généralisation des résultats à une plus grande population.
Malgré ces limites, cette étude observationnelle chez la patientèle de la région de l’Estrie, au Québec, permet d’apporter un éclairage nouveau sur la pratique en contexte réel chez un grand nombre de patients ayant reçu du voriconazole. Bien qu’il s’agisse de données régionales, ce sont néanmoins les premières données québécoises sur ce sujet.
Les résultats obtenus en contexte de pratique réelle dans la région de l’Estrie, au Québec, semblent indiquer que la conformité de la dose de maintien de voriconazole et les concentrations sériques des sujets sont adéquates. Cependant, une amélioration serait souhaitable pour la dose de charge, la dose utilisée chez les patients ayant un IMC supérieur à 30 et pour les suivis effectués. Une participation accrue des services d’antibiogouvernance par la création d’alertes et de suivis standardisés pourrait contribuer à une meilleure prise en charge globale des patients atteints d’une infection fongique invasive.
Ce projet a été financé par les fonds internes des chercheurs et le Département de pharmacie du CIUSSS de l’Estrie–CHUS.
Tous les auteurs ont soumis le formulaire de l’ICMJE sur la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts lié au présent article.
L’équipe de recherche souhaite remercier Jonathan Garcia, candidat à la maîtrise en pharmacothérapie avancée à l’Université de Montréal pour sa contribution à l’analyse des données. Cette personne a donné son autorisation écrite.
1. McCreary EK, Davis MR, Narayanan N, Andes DR, Cattaneo D, Christian R et al. Utility of triazole antifungal therapeutic drug monitoring: Insights from the Society of Infectious Diseases Pharmacists. Pharmacotherapy 2023;43: 1043–50.
Crossref PubMed
2. John J, Loo A, Mazur S, Walsh TJ. Therapeutic drug monitoring of systemic antifungal agents: a pragmatic approch for adult and pediatric patients. Expert Opin Drug Metab Toxicol 2019;15:881–95.
Crossref PubMed
3. Kably B, Launay M, Derobertmasure A, Lefeuvre S, Dannaoui E, Billaud EM. Antifungals drugs TDM: trends and update. Ther Drug Monit 2002;44:166–97.
Crossref
4. Abdul-Aziz MH, Alffenaar J-WC, Bassetti M, Bracht H, Dimopoulos G, Marriott D et al. Antimicrobial therapeutic drug monitoring in critically ill adult patients: a position paper. Intensive Care Med 2020;46:1127–53.
Crossref PubMed
5. Park WB, Kim N-H, Kim K-H, Lee SH, Nam W-S, Yoon SH et al. The effect of therapeutic drug monitoring on safety and efficacy of voriconazole in invasive fungal infections: a randomized controlled trial. Clin Infect Dis 2022;55:1080–7.
Crossref
6. Wei X, Zhao M, Fu P, Xiao X. Risks factors associated with insufficient and potentially toxic voriconazole plasma concentrations: an observationnal study. J Chemo 2019;31:401–7.
7. Hoennigl M, Duettmann W, Raggam RB, Seeber K, Troppan K, Fruhwald S et al. Potential factors for inadequate voriconazole plasma concentrations in intensive care unit patients and patients with hematological malignancies. Antimicrob Agents Chemother 2013;57:3262–7.
Crossref
8. Flores J, Flank J, Polito S, Dhillon P, Pang I, Ho L et al. Evaluation of voriconazole therapeutic drug monitoring in malignant hematology patients. J Oncol Pharm Practice 2024: 10781552241284528.
9. Institut national de santé publique du Québec, Gouvernement du Québec. Syndrome de sensibilité chimique multiple, une approche intégrative pour identifier les mécanismes physiopathologiques (juin 2021). [en ligne] https://www.inspq.qc.ca/sites/default/files/publications/2729-syndorme-sensibilite-chimique-rapport.pdf (site visité le 17 août 2024).
10. Letarte N, Lavoie A, Sheehan N, Hurlimann T, Robb L, Lambert JP, De Denus S. La pharmacothérapie personnalisée et la pharmacogénétique. Pharmactuel 2013;46;258–68.
11. Statistiques Canada, Gouvernement du Canada. Mois du patrimoine asiatique en chiffre (2022-10-04). [en ligne] https://www.statcan.gc.ca/fr/dai/smr08/2021/smr08_250 (site visité le 17 août 2024).
12. Pfizer. Monographie du voriconazole (Vfend). Kirkland, Québec. Septembre 2016.
13. Yi WM, Schoeppler KE, Jeager J, Mueller SW, MacLaren R, Fish DN et al. Voriconazole and posaconazole therapeutic drug monitoring: a retrospective study. Ann Clin Microbiol Antimicrob 2017;16:60.
Crossref PubMed
14. Dote S, Sawai M, Nozaki A, Naruhashi K, Kobayashi Y, Nakanishi H. A retrospective analysis of patient-specific factors on voriconazole clearance. J Pharm Health Care and Sci 2016; 2:10.
Crossref
15. Cheng L, Xiang R, Liu F, Li Y, Chen H, Yao P et al. Therapeutic drug monitoring and safety of voriconazole in elderly patients. Int Immunopharmacol 2020;78:106078.
Crossref
16. Ostrosky-Zeichner L, Nguyen MH, Bubalo J, Alexander BD, Miceli MH, Pappas PG et al. Multicenter registry of patients receiving systemic mold-active triazoles for the management of invasive fun gal infections. Infect Dis Ther 2022;11:1609–29.
PubMed
17. Patterson TF, Thompson III GR, Dennig DW, Fishman JA, Hadley S, Herbrecht R, et al. Practice guidelines for the diagnosis and management of aspergillosis: 2016 update by the Infectious Diseases Society of America. Clin Infect Dis 2016;63:e1–60.
Crossref PubMed
Pour toute correspondance : Bianca Beloin Jubinville, Centre intégré universitaire de santé et de services sociaux de l’Estrie–Centre hospitalier universitaire de Sherbrooke, Hôpital de Fleurimont, 3001, 12e, avenue Nord, Sherbrooke (Québec) J1H 5H3, Canada; Téléphone 819-346-1110, poste 25268; courriel : bianca.beloin-jubinville.ciussse-chus@ssss.gouv.qc.ca
PHARMACTUEL, Vol. 58, No. 3, 2025