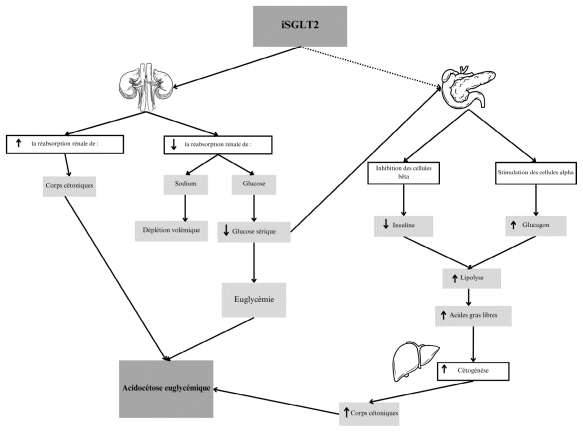
Figure 1 Physiopathologie de l’acidocétose euglycémique causée par les iSGLT2a
Abréviation : iSGLT2 : inhibiteurs du SGLT-2
a La flèche pointillée indique une relation controversée dans la littérature.
Camille Coutu1, Pharm.D., Élisabeth Gaudreau1, Pharm.D., Lynette Israilian1, Pharm.D., Joëlle Latreille1, Pharm.D., Viviane Lavigne2, Pharm.D., M.Sc.
1Candidate au Pharm.D. au moment de la rédaction, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
2Pharmacienne, Institut de cardiologie de Montréal, Montréal (Québec) Canada
Reçu le 4 juin 2024; Accepté après révision par les pairs le 29 novembre 2024
Résumé
Objectif: L’objectif du présent article est de discuter d’un effet indésirable rare, mais grave des inhibiteurs du cotransporteur sodium-glucose de type 2 (iSGLT2), soit l’acidocétose euglycémique. Nous passerons aussi en revue sa physiopathologie, sa détection, sa prise en charge et sa prévention.
Sources des données et sélection des études: Une revue de la littérature scientifique publiée entre 2010 et 2024 dans des bases de données telles que PubMed et Google Scholar a été effectuée en utilisant et en reliant des mots clés comme diabetic ketoacidosis, diagnosis, euglycemic ketoacidosis, iSGLT2, management, non-diabetic ketoacidosis, normoglycemic ketoacidosis, prevention, SGLT2 inhibitors, sodium-glucose cotransporter-2 inhibitors.
Revue du sujet traité: L’acidocétose euglycémique présente un défi diagnostique. De multiples facteurs précipitants associés à l’état de santé, aux habitudes de vie et à la prise concomitante de certains médicaments peuvent prédisposer au développement d’une acidocétose euglycémique. Le traitement hospitalier de l’acidocétose euglycémique repose sur trois axes principaux, soit la réplétion liquidienne, la correction de l’acidocétose et la prévention des hypoglycémies. La surveillance des cétones pourrait permettre une détection précoce de l’acidocétose euglycémique en contexte post-opératoire. La gestion des jours de maladie est un élément crucial à discuter avec les patients pour prévenir les acidocétoses euglycémiques attribuables aux iSGLT2.
Conclusion: Le pharmacien, qu’il pratique en milieu hospitalier ou communautaire, joue un rôle clé dans la prise en charge globale de l’acidocétose euglycémique liée aux iSGLT2.
Mots clés: acidocétose euglycémique, canagliflozine, dapagliflozine, diagnostic, empagliflozine, iSGLT2, prévention
Summary
Objective: To discuss euglycemic ketoacidosis, a rare, but serious adverse effect of sodium-glucose cotransporter-2 (SGLT-2) inhibitors. Pathophysiology and detection, management, and prevention strategies are also reviewed.
Data sources and study selection: A review of the scientific literature published between 2010 and 2024 in databases such as PubMed and Google Scholar was conducted using and linking keywords such as diabetic ketoacidosis, diagnosis, euglycemic ketoacidosis, iSGLT2, management, non-diabetic ketoacidosis, normoglycemic ketoacidosis, prevention, SGLT2 inhibitors, sodium-glucose cotransporter-2 inhibitors.
Subject review: Euglycemic ketoacidosis is a diagnostic challenge. Multiple precipitating factors associated with health status, lifestyle habits, and the concomitant use of certain medications may predispose patients to the development of euglycemic ketoacidosis. Hospital treatment is based on three main principles: fluid resuscitation, correction of ketoacidosis, and prevention of hypoglycemia. Ketone monitoring could enable early detection of euglycemic ketoacidosis in the postoperative setting. Management of medication during sick days is a crucial element to be discussed with patients to prevent euglycemic ketoacidosis secondary to SGLT-2 inhibitor use.
Conclusion: The pharmacist, whether working in the hospital or community setting, plays a key role in the management of SGLT-2 inhibitor-related euglycemic ketoacidosis.
Keywords: euglycemic ketoacidosis, canagliflozin, dapagliflozin, diagnosis, empagliflozin, iSGLT2, prevention
Au Québec, trois inhibiteurs du cotransporteur sodium-glucose de type 2 (iSGLT2) sont disponibles : la canagliflozine, la dapagliflozine et l’empagliflozine. Selon des données de Santé Canada, le nombre de réclamations pour les iSGLT2, autant dans les régimes d’assurances publics que privés, a augmenté d’environ 1,5 fois en 2021 par rapport à 20171. L’engouement pour ces molécules provient entre autres de leurs multiples bienfaits cardiovasculaires et rénaux ainsi que de la réduction du taux d’hospitalisation de la population atteinte d’insuffisance cardiaque. Ces molécules entraînent également des bienfaits sur la maîtrise des glycémies, la perte de poids et la pression artérielle2.
Ces effets bénéfiques ne sont pas complètement élucidés, mais pourraient s’expliquer par une hausse du métabolisme énergétique cardiaque, une diminution de l’état inflammatoire, une participation à l’érythropoïèse ainsi que par l’inhibition du système nerveux sympathique. Ils seraient de plus associés à la diurèse, à la réduction de la pression artérielle, à l’amélioration de la fonction vasculaire et à la vasoconstriction de l’artère afférente rénale3.
Selon les risques et les bienfaits présentés dans une méta-analyse regroupant six études randomisées contrôlées (CANVAS program, dont CANVAS et CANVAS-R, CREDENCE, DECLARE-TIMI 58, EMPA-REG OUTCOME, VERTIS CV), l’emploi d’iSGLT2 chez les patients atteints de diabète de type 2 réduirait la mortalité de cause cardiovasculaire (rapport de risque [RR] : 0,85; intervalle de confiance à 95 % [IC 95 %] : 0,78–0,93), les hospitalisations pour insuffisance cardiaque (RR : 0,68; IC 95 % : 0,61–0,76), la progression de la maladie rénale (RR : 0,62; IC 95 % : 0,56–0,70) ainsi que les événements cardiovasculaires majeurs (RR : 0,90; IC 95 % : 0,85–0,95)4.
Bien que les iSGLT2 ne soient pas officiellement indiqués dans le traitement du diabète de type 1 et qu’ils ne soient donc que rarement prescrits dans ce cas, ils seraient aussi bénéfiques chez ces patients que chez ceux atteints de diabète de type 2 pour réduire la progression vers une insuffisance rénale chronique. Quelques études de phase III (comme inTandem, DEPICT et EASE) comprenant des patients atteints de diabète de type 1 montrent une diminution de l’hémoglobine glyquée (HbA1c), de la pression artérielle et du poids, une augmentation de l’hématocrite ainsi que des bienfaits cardiovasculaires et rénaux5–8.
Ces molécules se sont également avérées efficaces chez les personnes atteintes d’insuffisance cardiaque à fraction d’éjection réduite ou préservée, qu’elles soient diabétiques ou non, en ce qui a trait à la mort de cause cardiovasculaire et aux hospitalisations pour insuffisance cardiaque, comme l’ont révélé les études EMPEROR-Reduced, EMPEROR-Preserved, DAPA-HF et DELIVER9.
Un effet indésirable rare, mais potentiellement grave associé aux iSGLT2 est l’acidocétose euglycémique, soit une acidose métabolique accompagnée d’une augmentation des corps cétoniques sériques et urinaires chez un patient dont la glycémie est normale17,18. Avec l’élargissement des indications et la hausse de la prescription des iSGLT2, de plus en plus de cas d’acidocétose euglycémique sont signalés, ce qui en fait un phénomène préoccupant pour les professionnels de la santé17.
Chez les patients atteints de diabète de type 2, l’incidence des acidocétoses diabétiques liées aux iSGLT2 est estimée à 2,03 événements pour 1000 patients-années19. L’incidence des acidocétoses de type euglycémique liées aux iSGLT2 n’est pas clairement établie dans la littérature, possiblement en raison de la rareté des événements, de leur sous-déclaration et de leur sous-diagnostic17. Dans les grandes études ayant montré les bienfaits de ces molécules, il y avait peu de différence entre les groupes de patients recevant un iSGLT2 et ceux recevant un placebo pour les cas d’acidocétose signalés, et aucune distinction n’était faite entre les acidocétoses hyperglycémiques et euglycémiques4. Une analyse des rapports d’acidocétoses diabétiques associées aux iSGLT2 déclarées dans le système de notification des effets indésirables de la Food and Drug Administration a révélé que 71 % des cas signalés étaient de nature euglycémique21. Le risque d’acidocétose diabétique, en général, serait environ deux fois plus élevé chez des patients atteints de diabète de type 2 prenant un iSGLT2 que chez les sujets témoins22,23. Quant aux patients atteints de diabète de type 1, leur risque d’acidocétose serait environ trois fois plus élevé chez ceux prenant un iSGLT2 en combinaison avec l’insuline comparativement au groupe témoin24. Le risque serait plus important chez ces patients vu leur dépendance à l’insuline exogène et leur risque de déficience relative ou absolue en insuline8,25. Chez les patients atteints d’insuffisance cardiaque traités par un iSGLT2, l’incidence d’acidocétose euglycémique ne semble pas plus fréquente que chez ceux prenant un iSGLT2 et n’étant pas atteints d’insuffisance cardiaque26. Il existe quelques mentions dans la littérature de cas d’acidocétose euglycémique chez des patients non diabétiques souffrant d’insuffisance cardiaque27.
Si l’acidocétose euglycémique n’est pas traitée, elle peut entraîner des complications allant de vomissements persistants à la déshydratation jusqu’au choc hypovolémique, au coma et éventuellement à la mort28. Il n’existe pas de données disponibles sur la morbimortalité associée à l’acidocétose euglycémique provoquée par les iSGLT229. Cependant, le taux de mortalité mentionné pour l’acidocétose diabétique est de 0,65 à 3,3 %30.
Actuellement, certains hôpitaux au Québec ne possèdent pas de protocole préétabli spécifique concernant le traitement des acidocétoses, et certains protocoles existants n’abordent pas les acidocétoses euglycémiques causées par les iSGLT2.
Le but de cet article est donc d’améliorer la connaissance des risques associés à l’utilisation des iSGLT2 par les professionnels de la santé et le niveau d’aisance concernant la prévention et la prise en charge complète des acidocétoses euglycémiques liées à ces médicaments. Nous souhaitons également faciliter une transition plus adéquate entre les différents milieux de soins.
Une revue de la documentation scientifique publiée entre 2010 et 2024 a été effectuée dans PubMed et Google Scholar, à l’aide des mots clés suivants : diabetic ketoacidosis, diagnosis, euglycemic ketoacidosis, iSGLT2, management, non-diabetic ketoacidosis, normoglycemic ketoacidosis, prevention, SGLT2 inhibitors, sodium-glucose cotransporter-2 inhibitors. Elle a permis la consultation d’études cliniques, de revues systématiques, de méta-analyses, de rapports de cas, d’opinions d’experts et de lignes directrices sur les iSGLT2 et sur leur utilisation chez des patients diabétiques ou souffrant d’insuffisance cardiaque ainsi que sur la prévalence et le traitement de l’acidocétose, qu’elle soit euglycémique ou non.
La physiopathologie de l’acidocétose euglycémique liée aux iSGLT2 réside d’abord dans le mécanisme d’action de ces molécules. Les iSGLT2 entraînent une inhibition du cotransporteur de réabsorption du glucose et du sodium de type 2 dans le tubule contourné proximal rénal nommé SGLT-2, responsable de la réabsorption de 90 % du glucose filtré. Ils accroissent l’excrétion urinaire de glucose (glycosurie), diminuent la disponibilité du glucose sérique et entraînent une déplétion volémique. De plus, ils augmenteraient la réabsorption des corps cétoniques par les reins31. Dans le pancréas, les iSGLT2 auraient potentiellement un effet direct sur les cellules alpha et bêta, pouvant causer un déséquilibre des concentrations d’insuline et de glucagon, ce qui favorise la production de corps cétoniques. Cet effet sur le pancréas reste somme toute controversé32,33. L’acidocétose pouvant en découler entraîne une acidose métabolique à trou anionique augmenté. La glycémie tend à être normale (d’où l’emploi du terme « euglycémique » pour qualifier l’acidocétose) en raison des pertes urinaires de glucose et de la réduction du glucose sérique disponible. Bref, tout problème ou tout facteur diminuant la disponibilité ou la production du glucose, réduisant la sécrétion d’insuline ou augmentant la production d’hormones de contre-régulation peut contribuer à l’apparition d’une acidocétose31. La physiopathologie de l’acidocétose euglycémique est schématisée à la figure 1.
Il existe plusieurs facteurs prédisposant à l’acidocétose euglycémique lors de la prise concomitante d’un iSGLT2. Certains états de santé prédisposent ainsi les patients à l’acidocétose euglycémique en raison d’une baisse de l’apport en glucides, d’une période de jeûne ou d’un stress physiologique, augmentant alors les hormones de contre-régulation comme le glucagon, l’adrénaline et le cortisol. Certaines maladies aiguës (p. ex. : infection, diarrhée, pancréatite, ischémie myocardique), certains problèmes de santé affectant l’absorption alimentaire (p. ex. : gastroparésie, troubles de malabsorption, troubles alimentaires ou chirurgie bariatrique récente), un état hypovolémique (p. ex. : préparation pour une coloscopie, exercice intensif tel qu’un marathon, déshydratation) et une chirurgie majeure en sont des exemples34–37.
Des habitudes de vie, comme l’alimentation cétogène régulière, très faible en glucides, peuvent également entraîner une acidocétose euglycémique à la suite d’une baisse des concentrations d’insuline et d’une augmentation des hormones de contre-régulation35,37. En contrepartie, des jeûnes périodiques comme celui du Ramadan comporteraient moins de risques38. Une consommation excessive d’alcool peut aussi prédisposer à l’acidocétose euglycémique, car elle est liée à une diminution des réserves de glucides et de protéines ainsi qu’à la lipolyse35,36. De plus, la diurèse osmotique et les vomissements associés peuvent mener à une déshydratation. Les dommages hépatiques causés par une consommation chronique d’alcool peuvent, en outre, accroître le risque de cétogenèse attribuable à des troubles de la glycogénolyse35.
La prise concomitante de certains médicaments est un autre facteur qui augmente le risque d’acidocétose euglycémique. Lors d’une baisse accrue ou soudaine d’insuline, notamment chez les patients atteints de diabète de type 1, le déséquilibre entre cette dernière et les hormones de contre-régulation favorise la cétogenèse35,37. Certains médicaments à haut potentiel émétisant, comme certaines chimiothérapies, peuvent prédisposer à la déshydratation et ainsi à l’acidocétose euglycémique. D’autres médicaments et drogues peuvent aussi hausser le risque d’acidocétose euglycémique en raison de l’altération des concentrations de glucose sérique, ce qui augmente encore une fois les hormones de contre-régulation. Les substances en cause sont entre autres la cocaïne, les corticostéroïdes, les interférons ainsi que les agents antipsychotiques35,39.
|
| ||
|
Figure 1 Physiopathologie de l’acidocétose euglycémique causée par les iSGLT2a
| ||
L’acidocétose euglycémique peut entraîner des symptômes non spécifiques, comme des nausées et des vomissements, un malaise généralisé, une léthargie, une perte d’appétit, une fatigue ainsi que des douleurs abdominales. Certains patients ne présentent pas de polydipsie ni de polyurie en raison de la nature euglycémique de l’acidocétose. Les patients peuvent également avoir une respiration profonde et rapide, appelée respiration de Kussmaul, lors d’une acidose métabolique grave. Leur haleine a parfois une odeur fruitée due à l’expiration d’acétone. Des signes de perte de liquide corporel peuvent se traduire par une tachycardie, une hypotension, une altération de l’état mental et une diminution de la turgescence de la peau28. Il est à noter que l’absence d’hyperglycémie retarde souvent le diagnostic d’acidocétose euglycémique dans un contexte hospitalier37.
Les deux principaux sous-types de cétones sont le β-hydroxybutyrate et l’acétoacétate, tandis que l’acétone est le troisième et le moins abondant des corps cétoniques41,42. Le corps cétonique prédominant dans l’acidocétose euglycémique est le β-hydroxybutyrate avec un ratio sanguin de 7 à 10 pour 1 pour l’acétoacétate31. Lorsqu’une acidocétose est soupçonnée, il est préférable de mesurer le β-hydroxybutyrate sérique, car le dosage des cétones urinaires ne détecte que l’acétoacétate. Le β-hydroxybutyrate peut être mesuré sur une ponction veineuse ou à l’aide d’un appareil de test capillaire. Selon une étude systématique, le test capillaire a une bonne sensibilité et spécificité. Cependant, sa précision est moins grande que celle du test sanguin lorsque les valeurs dépassent 5 mmol/L43. Par ailleurs, lors de l’utilisation d’un iSGLT2, on observe une augmentation de la réabsorption rénale de cétones, ce qui peut mener à un faux négatif pour les tests urinaires31,44. Si le test capillaire ou sérique n’est pas possible, le test urinaire peut être effectué, bien que sa spécificité et sa sensibilité soient moindres dans le contexte d’une acidocétose euglycémique31. Il existe plusieurs outils pour détecter la présence de cétones si on soupçonne une acidocétose euglycémique, tant en pharmacie d’officine qu’en milieu hospitalier. Les bandelettes urinaires (p. ex. : Roche Chemstrip 7, Roche Chemstrip 9, Ascencia Ketostix) permettent de détecter et de quantifier le taux de cétones à l’aide d’un intervalle de couleurs tandis que les bandelettes sanguines Freestyle Precision B-Ketone strips permettent d’obtenir un résultat chiffré précis, exprimé en mmol/L, à l’aide des glucomètres Freestyle.
Les critères diagnostiques de l’acidocétose euglycémique sont présentés dans le tableau I. Le diagnostic d’acidocétose euglycémique en est un d’exclusion, ce qui signifie que toutes les autres causes d’acidose métabolique doivent être exclues au préalable37.
Une fois le diagnostic d’acidocétose euglycémique confirmé, la première étape de la prise en charge consiste à suspendre l’iSGLT2. Selon l’état du patient, l’acidocétose euglycémique peut être traitée dans une unité de soins courante ou aux soins intensifs. Les critères de gravité sont un pH inférieur à 7,25, une concentration de β-hydroxybutyrate supérieure à 6 mmol/L et une altération de l’état de conscience43. La prise en charge globale d’une acidocétose euglycémique est très semblable à celle d’une acidocétose diabétique. La principale différence est la normalisation des glycémies dès le début. Par conséquent, l’ajout de dextrose est nécessaire pour prévenir les hypoglycémies attribuables à insuline. Selon une étude rétrospective, les différences observées entre les acidocétoses diabétiques et euglycémiques à l’hôpital seraient liées à une administration accrue de fluides par voie intraveineuse malgré des glycémies normalisées, un délai plus long avant la résolution de l’acidose et un temps d’hospitalisation supérieur45. Les trois grands éléments éléments de la prise en charge hospitalière sont illustrés dans la figure 2 : la réplétion liquidienne, la correction de l’acidocétose et la prévention des hypoglycémies.
La réhydratation constitue un élément clé de la prise en charge et devrait être la première étape. Les pertes liquidiennes causées par l’acidocétose euglycémique peuvent atteindre de six à neuf litres. La réplétion liquidienne est donc primordiale pour assurer la résolution des anomalies métaboliques ainsi qu’une bonne irrigation tissulaire36. La solution de réhydratation généralement employée est le chlorure de sodium isotonique (NaCl à 0,9 %). Par contre, il faut se rappeler qu’une perfusion continue de chlorure de sodium peut prolonger l’état d’acidose en provoquant une acidose métabolique hyperchlorémique. La solution de lactate de Ringer représente donc une solution de rechange au chlorure de sodium permettant d’éviter ce risque. En outre, des bienfaits sur la rapidité de correction de l’état d’acidose ainsi que sur les durées d’hospitalisation ont été observés43.
Une perfusion d’insuline associée à une autre de dextrose doit suivre la réplétion liquidienne. L’insuline est essentielle à la prise en charge de l’acidocétose euglycémique, malgré la glycémie normale. En diminuant la glycogénolyse et la gluconéogenèse, l’insuline favorise l’usage du glucose, ce qui provoque la suppression de la formation des corps cétoniques. L’insuline entraîne une entrée de potassium vers le milieu intracellulaire. Il faut donc être vigilant quant aux hypokaliémies et les corriger au besoin ainsi que suspendre l’insuline jusqu’à ce que la kaliémie se soit normalisée36. Chez les patients présentant un débit de filtration glomérulaire estimé inférieur à 15 mL/min, une attention particulière devrait être apportée avant de commencer la perfusion de potassium afin de réduire les risques associés à une accumulation46. Une fois que l’acidocétose est résolue, que l’état du patient est cliniquement stable et que ce dernier est capable de s’alimenter, il faut envisager un passage à l’insuline par voie sous-cutanée, mais poursuivre la perfusion d’insuline pendant les deux heures suivant la première administration sous-cutanée29,43.
Tableau I Critères diagnostiques de l’acidocétose euglycémique

Un suivi étroit des analyses sanguines et des signes vitaux doit être effectué tout au long de la correction de l’acidocétose et jusqu’à l’élimination complète de l’iSGLT2, soit environ 72 heures après son arrêt. Les détails se trouvent dans la figure 2.
Le diagnostic d’acidocétose euglycémique est complexe dans un contexte postopératoire. En effet, les symptômes peuvent s’apparenter à des problèmes relativement fréquents après une intervention chirurgicale, tels qu’un dysfonctionnement rénal, une hypoperfusion des tissus et une infection44. La période postopératoire est associée à un risque plus élevé d’acidocétose euglycémique chez les patients prenant un iSGLT2 en raison de l’augmentation des catécholamines, du cortisol et du glucagon34. Les patients ayant subi une chirurgie cardiaque sont particulièrement à risque d’acidocétose euglycémique si la molécule n’est pas suspendue à temps, car ils se retrouvent plus longtemps en phase catabolique (jeûne prolongé et augmentation de la réponse hormonale au stress). En général, étant donné la demi-vie de 11 à 13 heures des différents iSGLT2, il est recommandé de les cesser au moins 72 heures avant une intervention importante ou nécessitant un jeûne prolongé18,44,48. Une attention particulière devrait être accordée aux patients atteints d’insuffisance rénale chronique, chez qui le temps de demi-vie pourrait être prolongé.
|
| ||
|
Figure 2 Traitement hospitalier de l’acidocétose euglycémique causée par les iSGLT2
| ||
C’est bien de savoir prendre en charge les acidocétoses euglycémiques attribuables aux iSGLT2, mais c’est encore mieux de les prévenir. La clé de la prévention se trouve dans le conseil de remise des médicaments de cette classe, en pharmacie d’officine, par exemple. Bien que le présent article ne porte pas spécifiquement sur les acidocétoses hyperglycémiques, les suggestions suivantes sont tout autant valables pour prévenir l’acidocétose euglycémique.
Le principe le plus important à inculquer aux patients est la gestion des journées de maladie, c’est-à-dire les contextes dans lesquels la prise de l’iSGLT2 devrait être suspendue : infection, diarrhées et vomissements importants, exercice physique intense, faible apport calorique. Un autre élément clé est de présenter au patient les signes et symptômes d’acidocétose euglycémique à surveiller (nausées, vomissements, perte d’appétit, malaise généralisé, fatigue et/ou douleurs abdominales), tout en insistant sur le fait que l’acidocétose euglycémique survient lorsque les glycémies sont normales36. De plus, il semble approprié d’informer les patients de la possibilité de se procurer des tests capillaires pour vérifier la présence de cétones28. Il pourrait être souhaitable, après discussion avec les patients les plus à risque, de leur prescrire une boîte de bandelettes de cétonémie. Il est aussi essentiel d’expliquer au patient l’importance d’un apport calorique relativement stable pendant la prise et de l’aviser de contacter un pharmacien ou un médecin avant un changement considérable d’alimentation, comme l’amorce de l’alimentation cétogène ou un jeûne prolongé33. Enfin, les patients devraient être avisés de consulter un professionnel de la santé dans le cas d’une intervention chirurgicale à venir pour convenir de la conduite à tenir quant à l’iSGLT236. Les conseils de remise et de suivi sont évidemment à individualiser selon les caractéristiques de chaque patient, comme le montre la figure 3.
Il est parfois difficile d’identifier l’acidocétose euglycémique par ses signes et symptômes non spécifiques. Sa détection rapide permet toutefois d’éviter les complications. La mesure des cétones urinaires ou sanguines se fait facilement et est spécifique, mais les tests capillaires et sériques sont préférables. En effet, le pharmacien d’officine, par sa proximité, ses connaissances et son accessibilité, pourrait apporter une aide précieuse dans la détection rapide de l’acidocétose euglycémique et diriger le patient vers l’urgence, le cas échéant25.
|
| ||
|
Figure 3 Stratégies pour réduire au minimum le risque d’acidocétose euglycémique liées aux iSGLT2 selon les caractéristiques des patientsa
| ||
Dans un contexte périopératoire, les patients chez qui la suspension de l’iSGLT2 n’a pu être prévue (p. ex. : intervention urgente) devraient faire l’objet d’une surveillance accrue quant à l’apparition de signes et symptômes d’acidocétose euglycémique. Une surveillance plus étroite du pH veineux et du β-hydroxybutyrate capillaire pourrait être effectuée pendant la période postopératoire où les risques sont plus élevés (environ 72 heures), surtout si des symptômes apparaissent.
Le retard dans le diagnostic de l’acidose peut être très préjudiciable au patient. Comme le délai pour obtenir le résultat du dosage des cétones sériques à l’hôpital est de plusieurs heures, particulièrement quand l’échantillon doit être analysé en externe, les bandelettes de cétonémie pourraient être utilisées à l’urgence lorsqu’une acidocétose est soupçonnée pour assurer une prise en charge adéquate et précoce. D’ailleurs, tous les milieux prodiguant des soins à des patients diabétiques ou prenant des iSGLT2 devraient avoir des bandelettes de cétonémie.
Lors de la prise en charge d’une acidocétose euglycémique en milieu hospitalier, la première étape consiste à suspendre l’iSGLT2. Selon les différentes données recueillies dans la littérature, la réplétion liquidienne, la correction de l’acidocétose et la prévention des hypoglycémies font ensuite partie de la démarche suggérée. Comme le montre la figure 2, les analyses sanguines et les signes vitaux doivent être suivis jusqu’à la correction de l’acidocétose. Une surveillance quotidienne des taux sanguins de β-hydroxybutyrate, des électrolytes, des gaz sanguins et de la volémie serait idéale jusqu’à ce que l’état du patient soit cliniquement stable et que ce dernier soit en mesure de s’alimenter34.
Une controverse souvent soulevée par les cliniciens porte sur la reprise ou l’arrêt définitif d’un iSGLT2 après une acidocétose euglycémique, ainsi que sur le moment de la reprise, le cas échéant. Les consensus publiés à ce jour portent surtout sur les acidocétoses hyperglycémiques. La majorité des lignes directrices ne mentionnent que très peu les iSGLT2, voire pas du tout43. Certaines références soulignent très brièvement de ne pas reprendre l’iSGLT2, car il n’existe pas jusqu’à présent de données fiables quant aux risques et aux avantages de recommencer ces agents après une acidocétose euglycémique.
De plus, des données américaines ont montré que près de 22 % des patients ayant eu une acidocétose diabétique ou un état hyperglycémique hyperosmolaire ont été réadmis à l’hôpital dans les 30 jours de la sortie d’hôpital ou au cours de l’année civile suivante. Parmi ces patients, un peu plus de 40 % avaient souffert d’acidocétose de façon récurrente, dont 50 % avaient été réadmis moins de deux semaines après l’hospitalisation initiale. Donc, les patients ayant fait une acidocétose diabétique présentent un risque de récurrence non négligeable. On ne dispose malheureusement pas de données de cette nature pour les acidocétoses euglycémiques causées par les iSGLT2, vu leur faible prévalence49,50.
Malgré tout, la décision de cesser un iSGLT2 ne doit pas être prise à la légère. Effectivement, les iSGLT2 offrent plusieurs bienfaits et, dans certaines populations, ces bienfaits disparaissent rapidement à l’arrêt. Chez les patients en insuffisance cardiaque, une étude menée chez les cohortes de patients des essais cliniques EMPEROR-Reduced et EMPEROR-Preserved a comparé l’effet de la cessation de l’empagliflozine au placebo sur le critère d’évaluation de mort cardiovasculaire et d’hospitalisations pour décompensation de l’insuffisance cardiaque après environ 30 jours d’arrêt. Les résultats montrent que le risque annualisé de décès d’origine cardiovasculaire ou d’hospitalisation pour insuffisance cardiaque a augmenté chez les patients dont l’empagliflozine a été cessée, ce qui n’était pas le cas dans le groupe témoin. Ces résultats semblent indiquer que les bienfaits cardiovasculaires de l’empagliflozine se dissipent rapidement à l’arrêt51.
Le rapport risques-avantages doit donc être évalué, et une attention particulière doit être portée aux éléments déclencheurs de l’acidocétose euglycémique. Un facteur de risque transitoire et non récurrent pourrait justifier la décision de reprendre l’iSGLT2 beaucoup plus facilement qu’un facteur de risque persistant. Chez les patients où un facteur précipitant clair peut être établi (p. ex. : une infection aiguë), il pourrait être approprié de reprendre le traitement sous surveillance étroite en insistant sur la détection des signes et symptômes et sur la prévention de l’acidocétose euglycémique (p. ex. : suspension de l’iSGLT2 lors des journées de maladie)40. Certains patients présentant des facteurs de risque non transitoires pourraient être plus susceptibles de faire d’autres acidocétoses euglycémiques (p. ex. : les patients très fragiles ayant un grand risque d’infection, les patients ayant des troubles neurocognitifs ou bien des patients souffrant d’un trouble alimentaire). La reprise de l’iSGLT2 chez ces types de patients devrait être évitée pour réduire au minimum le risque de récurrence. Il est à noter qu’il existe d’autres facteurs de risque plus rares pouvant également prédisposer aux acidocétoses euglycémiques, comme certaines immunothérapies ou le diabète insulinodépendant de l’adulte (latent autoimmune diabetes in adults ou LADA)52–54.
Dans sa réflexion, le professionnel devrait tenir compte du fait que si le facteur de risque n’est pas transitoire, il est plus risqué de recommencer l’iSGLT2. L’avis d’un endocrinologue est alors de mise.
Si la cause est de nature idiopathique, certains experts jugent la molécule contre-indiquée afin d’éviter la récurrence44.
Si la décision de recommencer l’iSGLT2 est prise et que le patient est jugé apte à suivre les recommandations sur la gestion des jours de maladie, il est conseillé d’attendre que le patient soit dans un état cliniquement stable, euvolémique et en mesure de s’alimenter avant de reprendre l’iSGLT2. Il est également recommandé d’attendre que la fonction rénale soit stable et que le taux de cétones soit normal34,44. De plus, une méta-analyse a montré une courbe dose-réponse entre la dose d’iSGLT2 reçue et le nombre d’acidocétoses euglycémiques signalées. Une piste de solution à envisager pourrait être la reprise de l’iSGLT2 à plus faible dose afin de diminuer les risques de récurrence20.
Au congé de l’hôpital, les patients devraient idéalement avoir en leur possession les outils nécessaires pour suivre les concentrations de β-hydroxybutyrate capillaires à domicile dans les jours suivant la reprise de l’iSGLT2. Le pharmacien d’officine est le professionnel le mieux placé pour suivre ces patients après leur hospitalisation et pour les diriger rapidement, selon son évaluation de la situation. À noter que des concentrations de β-hydroxybutyrate inférieures à 0,6 mmol/L, sans autres signes ou symptômes, ne sont pas préoccupants25,43.
La prévention constitue un aspect clé de la gestion des acidocétose euglycémique. En effet, il est fortement suggéré d’appliquer les conseils prodigués dans cet article lors de la remise d’un iSGLT2 à un patient afin d’éviter les complications associées à leur prise. Comme pour toute consultation pharmaceutique, les éléments ciblés doivent être adaptés aux caractéristiques du patient afin d’assurer une prévention adéquate, comme le montre la figure 3.
En plus de faire leur place dans l’arsenal thérapeutique du diabète de type 2, les iSGLT2 ont entraîné des bienfaits dans la prévention des complications cardiovasculaires et rénales, ce qui a conduit à l’élargissement de leurs indications thérapeutiques. Bien que les iSGLT2 soient bien tolérés par la plupart des patients, leur profil d’innocuité est associé à des complications rares, dont les acidocétose euglycémique. Cet effet indésirable reste une préoccupation pour les cliniciens. Ainsi, dans cet article, des recommandations sur la prise en charge de l’acidocétose euglycémique sont faites aux pharmaciens, car ils jouent un rôle primordial dans l’enseignement aux patients en leur montrant non seulement comment prévenir les acidocétoses euglycémiques liées aux iSGLT2, mais également comment les détecter et les traiter. Avec l’utilisation de plus en plus fréquente de ces agents, il faudra rester attentifs aux nouvelles données sur l’ampleur de cet effet indésirable et sur les manières d’en améliorer la prise en charge globale.
Les auteures n’ont déclaré aucun financement pour le présent article.
Toutes les auteures ont soumis le formulaire de l’ICMJE sur la divulgation de conflits d’intérêts potentiels. Les auteures n’ont déclaré aucun conflit d’intérêts lié au présent article.
1. Conseil d’examen du prix des médicaments brevetés. Rapport sur la situation du marché : Médicaments antidiabétiques, 2012–2021 (mai 2023). [en ligne] https://www.canada.ca/content/dam/pmprb-cepmb/documents/npduis/analytical-studies/market-intelligence-report/NPDUIS-MI%20Antidiabetic%20Drugs%202012-2021_fr.pdf (site visité le 21 mai 2024).
2. Shah SS, Spratt SE, Edmonston DL, Pagidipati N. Clinical progress note: indications for and management of sodium-glucose cotransporter-2 (SGLT2) inhibitors in hospitalized patients. J Hosp Med 2022;17:360–3.
3. Lopaschuk GD, Verma S. Mechanisms of cardiovascular benefits of sodium glucose co-transporter 2 (SGLT2) inhibitors: a state-of-the-art review. J Am Coll Cardiol Basic Trans Science 2020;5:632–44.
4. McGuire DK, Shih WJ, Cosentino F, Charbonnel B, Cherney DZI, Dagogo-Jack S et al. Association of SGLT2 inhibitors with cardiovascular and kidney outcomes in patients with type 2 diabetes. JAMA Cardiol 2021;6:148–58.
5. Buse JB, Garg SK, Rosenstock J, Bailey TS, Banks P, Bode BW et al. Sotagliflozin in combination with optimized insulin therapy in adults with type 1 diabetes: the North American in Tandem1 study. Diabetes Care 2018;41:1970–80.

6. Dandona P, Mathieu C, Phillip M, Hansen L, Griffen SC, Tschöpe D. Efficacy and safety of dapagliflozin in patients with inadequately controlled type 1 diabetes (DEPICT-1): 24 week results from a multicentre, double-blind, phase 3, randomised controlled trial. Lancet Diabetes Endocrinol 2017;5:864–76.

7. Rosenstock J, Marquard J, Laffel LM, Neubacher D, Kaspers S, Cherney DZ et al. Empagliflozin as adjunctive to insulin therapy in type 1 diabetes: the EASE trials. Diabetes Care 2018;41:2560–69.

8. Liu H, Sridhar VS, Perkins BA, Rosenstock J, Cherney DZ. SGLT2 inhibition in type 1 diabetes with diabetic kidney disease: potential cardiorenal benefits can outweigh preventable risk of diabetic ketoacidosis. Curr Diab Rep 2022;22: 317–32.

9. Vaduganathan M, Docherty KF, Claggett BL, Jhund PS, De Boer RA, Hernandez AF et al. SGLT2 inhibitors in patients with heart failure: a comprehensive meta-analysis of five randomised controlled trials. Lancet Glob Health 2022;400:757–67.
10. AstraZeneca Canada. Monographie de produit: Forxiga (10 décembre 2014). [en ligne] https://www.astrazeneca.ca/content/dam/az-ca/frenchassets/Ourmedicines/forxiga-product-monograph-fr.pdf (site visité le 29 mai 2024).
11. Boehringer Ingelheim (Canada). Monographie de produit: Jardiance (22 juin 2021). [en ligne] https://pdf.hres.ca/dpd_pm/00062118.PDF (site visité le 29 mai 2024).
12. Janssen Inc. Monographie de produit: Invokana (23 janvier 2020). [en ligne] https://pdf.hres.ca/dpd_pm/00054739.PDF (site visité le 29 mai 2024).
13. McGovern AP, Hogg M, Shields BM, Sattar NA, Holman RR, Pearson ER et al. Risk factors for genital infections in people initiating SGLT2 inhibitors and their impact on discontinuation. BMJ Open Diabetes Res Care 2020;8:1–8.

14. Puckrin R, Saltiel MP, Reynier P, Azoulay L, Yu OHY, Filion KB. SGLT2 inhibitors and the risk of infections: a systematic review and meta-analysis of randomized controlled trials. Acta Diabetol 2018;55:503–14.


15. Sarafidis PA, Ortiz A. The risk for urinary tract infections with sodium-glucose cotransporter 2 inhibitors: no longer a cause of concern? Clin Kidney J 2020;13:24–6.


16. Food and Drug Administration. FDA warns about rare occurrences of a serious infection of the genital area with SGLT2 inhibitors for diabetes (7 septembre 2018). [en ligne] https://www.fda.gov/drugs/drug-safety-and-availability/fda-warns-about-rare-occurrences-serious-infection-genital-area-sglt2-inhibitors-diabetes (site visité le 29 mai 2024).
17. Al-Hindi B, Mohammed MA, Mangantig E, Martini ND. Prevalence of sodium-glucose transporter 2 inhibitor-associated diabetic ketoacidosis in real-world data: a systematic review and meta-analysis. J Am Pharm Assoc 2024;64:9–26.e6.

18. Food and Drug Administration. FDA revises labels of SGLT2 inhibitors for diabetes to include warnings about too much acid in the blood and serious urinary tract infections (16 mars 2022). [en ligne] https://www.fda.gov/drugs/drug-safety-and-availability/fda-revises-labels-sglt2-inhibitors-diabetes-include-warnings-about-too-much-acid-blood-and-serious (site visité le 29 mai 2024).
19. Douros A, Lix LM, Fralick M, Dell’Aniello S, Shah BR, Ronksley PE et al. Sodium-glucose cotransporter-2 inhibitors and the risk for diabetic ketoacidosis: a multicenter cohort study. Ann Intern Med 2020;173:417–25.


20. Dutta S, Kumar T, Singh S, Ambwani S, Charan J, Varthya SB. Euglycemic diabetic ketoacidosis associated with SGLT2 inhibitors: a systematic review and quantitative analysis. J Family Med Prim Care 2022;11:927–40.


21. Blau JE, Tella SH, Taylor SI, Rother KI. Ketoacidosis associated with SGLT2 inhibitor treatment: analysis of FAERS data. Diabetes Metab Res Rev 2017;33:1–7.

22. Liu J, Li L, Li S, Wang Y, Qin X, Deng K et al. Sodium-glucose co-transporter-2 inhibitors and the risk of diabetic ketoacidosis in patients with type 2 diabetes: a systematic review and meta-analysis of randomized controlled trials. Diabetes Obes Metab 2020;22:1619–27.


23. Lin DSH, Lee JK, Chen WJ. Clinical adverse events associated with sodium-glucose cotransporter 2 inhibitors: a meta-analysis involving 10 randomized clinical trials and 71 553 individuals. J Clin Endocrinol Metab 2021;106:2133–45.


24. Yamada T, Shojma N, Noma H, Yamauchi T, Kadowaki T. Sodium-glucose co-transporter-2 inhibitors as add-on therapy to insulin for type 1 diabetes mellitus: systematic review and meta-analysis of randomized controlled trials. Diabetes Obes Metab 2018;20:1755–61.


25. Danne T, Garg S, Peters AL, Buse JB, Mathieu C, Pettus JH et al. International consensus on risk management of diabetic ketoacidosis in patients with type 1 diabetes treated with sodium–glucose cotransporter (SGLT) inhibitors. Diabetes Care 2019;42:1147–54.


26. Yeung SL, Wang M, Lou M, Ng TM. Frequency of reported euglycemic ketoacidosis with sodium-glucose cotransporter-2 inhibitors is not increased in patients with heart failure: analysis of US Food and Drug Administration adverse event reporting system (FAERS). Circulation 2023;148(suppl. 1):abstract 17641.

27. Umapathysivam MM, Gunton J, Stranks SN, Jesudason D. Euglycemic ketoacidosis in two patients without diabetes after introduction of sodium-glucose cotransporter 2 inhibitor for heart failure with reduced ejection fraction. Diabetes Care 2024;47:140–3.

28. Plewa, M.C., Bryant, M., & King-Thiele, R. (2023). Euglycemic diabetic ketoacidosis. Dans StatPearls. Récupéré de https://www.ncbi.nlm.nih.gov/books/NBK554570/ (consulté le 29 mai 2024).
29. Chow E, Clement S, Garg R. Euglycemic diabetic ketoacidosis in the era of SGLT2 inhibitors. BMJ Open Diabetes Research and Care 2023; 11:e003666.

30. Goguen J, Gilbert J. Hyperglycemic emergencies in adults. Can J Diabetes 2018;42(suppl. 1): 109–14.

31. Long B, Lentz S, Koyfman A, Gottlieb M. Euglycemic diabetic ketoacidosis: etiologies, evaluation, and management. Am J Emerg Med 2021;44:157–60.


32. Chae H, Augustin R, Gatineau E, Mayoux E, Bensellam M, Antoine N et al. SGLT2 is not expressed in pancreatic α- and β-cells, and its inhibition does not directly affect glucagon and insulin secretion in rodents and humans. Mol Metab 2020;42:101071.

33. Somagutta MR, Agadi K, Hange M, Jain MS, Batti E, Emuze BO et al. Euglycemic diabetic ketoacidosis and sodium-glucose cotransporter-2 inhibitors: a focused review of pathophysiology, risk factors, and triggers. Cureus 2021;13:e13665.

34. Milder DA, Milder TY, Kam PCA. Sodium-glucose co-transporter type-2 inhibitors: pharmacology and peri-operative considerations. Anaesthesia 2018;73:1008–18.


35. Bamgboye AO, Oni IO, Collier A. Predisposing factors for the development of diabetic ketoacidosis with lower than anticipated glucose levels in type 2 diabetes patients on SGLT2-inhibitors: A review. Eur J Clin Pharmacol 2021;77:651–7.

36. Mathew DS, Ng KE, Jacob EC. Management of euglycemic diabetic ketoacidosis. US Pharm 2021;46:HS1–HS6
37. Nasa P, Chaudhary S, Shrivastava PK, Singh A. Euglycemic diabetic ketoacidosis: a missed diagnosis. World J Diabete 2021;12:514–23.

38. Hassanein M, Bashier A, Randeree H, Abouelmagd M, AlBaker W, Afandi B et al. Use of SGLT2 inhibitors during Ramadan: an expert panel statement. Diabetes Res Clin Pract 2020;169:108465.


39. Goldenberg RM, Berard LD, Cheng AYY, Gilbert JD, Verma S, Woo VC et al. SGLT2 inhibitor-associated diabetic ketoacidosis: clinical review and recommendations for prevention and diagnosis. Clin Ther 2016;38:2654–64.


40. Selwyn J, Pichardo-Lowden AR. Managing hospitalized patients taking SGLT2 inhibitors: reducing the risk of euglycemic diabetic ketoacidosis. Diabetology 2023;4,86–92.

41. Cantrell, C.B., & Mohiuddin, S.S. (2023). Ketone metabolism. Dans *Biochemistry* (chap. 41). Récupéré de https://www.ncbi.nlm.nih.gov/books/NBK554523/ (consulté le 29 mai 2024).
42. Laffel L. Ketone bodies: a review of physiology, pathophysiology and application of monitoring to diabetes. Diabetes Metab Res Rev 1999;15: 412–26.
43. Guillermo EU, Davis GM, ElSayed NA, Fadini GP, Galindo RJ et al. Hyperglycemic crises in adults with diabetes: a consensus report. Diabetes Care 2024;47:1257–75.
44. Branco A, Fatima R, Liblik K, Jackson R, Payne D, El-Diasty M. Euglycemic diabetic ketoacidosis associated with sodium-glucose cotransporter-2 inhibitors after cardiac surgery: a review of current literature. J Cardiothorac Vasc Anesth 2022;36:3877–86.

45. Papanastasiou L, Glycofridi S, Gravvanis C, Skarakis N, Papadimitriou I, Kanti G et al. Diabetic ketoacidosis in patients treated with SGLT2 inhibitors: experience at a tertiary hospital. J Clin Endocrinol Metab 2021;20:369–76.
46. Muneer M, Akbar I. Acute metabolic emergencies in diabetes: DKA, HHS and EDKA. Diabetes Res Clin Pract 2021;4:85–114.
47. Queensland Government. Management of diabetic ketoacidosis in adults (age 16 years and over) (2023). [en ligne] https://www.health.qld.gov.au/__data/assets/pdf_file/0019/621640/diabetic-ketoacidosis.pdf (site visité le 29 mai 2024).
48. Gouvernement du Canada. Résumé de l’examen de l’innocuité–Inhibiteurs du cotransporteur de sodium-glucose de type 2 (SGLT2) [canagliflozine, dapagliflozine, empagliflozine]–Évaluation des risques potentiels d’acidocétose diabétique prolongée ou nouvelle malgré l’arrêt du traitement chez les patients adultes atteints de diabète de type 2 (17 octobre 2024). [en ligne] https://pmps.hpfb-dgpsa.ca/documents-d-examen/ressource/SSR1724175682293 (site visité le 29 mai 2024).
49. Hurtado CR, Lemor A, Vallejo F, Lopez K, Garcia R, Mathew J et al. Causes and predictors for 30-day re-admissions in adult patients with diabetic ketoacidosis in the United States: a nationwide analysis, 2010–2014. Endocr Pract 2019;25:242–53.

50. Everett E, Mathioudakis NN. Association of socioeconomic status and DKA readmission in adults with type 1 diabetes: analysis of the US national readmission database. Diabetes Res Care 2019;7:e000621.
51. Packer M, Butler J, Zeller C, Pocock SJ, Brueckmann M, Ferreira JP et al. Blinded withdrawal of long-term randomized treatment with empagliflozin or placebo in patients with heart failure. Circulation 2023;148:1011–22.

52. Kotwall A, Haddox C, Block M, Kadvua Y. Immune checkpoint inhibitors: an emerging cause of insulin-dependant diabetes. BMJ Open Diabetes Res Care 2019;7:1–10
53. Sankar K, Macfarlane M, Cooper O, Falk J. Pembrolizumab-induced diabetic ketoacidosis: a review of critical care case. Cureus 2021;13: e18983.

54. Buzzetti R, Tuomi T, Mauricio D, Pietropaolo M, Zhou Z, Pozzilli P et al. Management of latent autoimmune diabetes in adults: a consensus statement from an international expert panel. Diabetes 2020;69:2037–47.

Pour toute correspondance : Viviane Lavigne, Institut de cardiologie de Montréal, 5000, rue Bélanger, Montréal (Québec) H1T 1C8, CANADA; téléphone: 514-531-9233; courriel : viviane.lavigne@icm-mhi.org.
PHARMACTUEL, Vol. 58, No. 1, 2025