Diem Vo1, B.Pharm., M.Sc., MBA, Josée Robillard2, B.Pharm., M.Sc., Serge Lamoureux2, B.Pharm., Isabelle St-Jean3, M.Sc., Mihaela Friciu4, M.Sc., Jean-Marc Forest5, B.Pharm., DPH, M.Sc., Grégoire Leclair6, B.Pharm., Ph.D.
1Pharmacienne, chef du Département de pharmacie, Centre intégré de santé et de services sociaux de la Montérégie-Est, Longueuil (Québec) Canada;
2Pharmacien(ne), Centre intégré de santé et de services sociaux de la Montérégie-Est, Longueuil (Québec) Canada;
3Agente de recherche et spécialiste en bio-analyse, plateforme de biopharmacie, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
4Conseillère principale en recherche, spécialiste de formulation et coordinatrice, plateforme de biopharmacie, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
5Pharmacien, responsable du secteur fabrication, Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada;
6Professeur titulaire et directeur de la plateforme de biopharmacie, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada
Reçu le 15 juin 2024; Accepté après révision par les pairs le 24 septembre 2024
Résumé
Objectif: La date limite d’utilisation des médicaments injectables pour l’aide médicale à mourir est relativement courte. Une série d’études ont évalué le prolongement de la stabilité physico-chimique du propofol, du rocuronium et du phénobarbital, ainsi que la stabilité physique du sulfate de magnésium.
Méthode: Les préparations ont été conditionnées dans des seringues de polypropylène de 20 mL et entreposées à la température ambiante et au réfrigérateur à 5 °C (propofol seulement). La stabilité physico-chimique du rocuronium, du propofol et du phénobarbital a été évaluée par chromatographie en phase liquide à haute performance sur 10, 14 et 30 jours. Pour le magnésium, le nombre de particules a été évalué sur 10 jours selon le test 1.B du chapitre <788> de la United States Pharmacopeia.
Résultats: La préparation de propofol à 20 mg/mL est demeurée stable pendant toute la durée de l’étude tandis que celles à 10 mg/mL sont restées stables lorsqu’elles étaient entreposées à 5 °C seulement. Les concentrations de rocuronium et de phénobarbital sont demeurées supérieures à 90 % de la concentration initiale dans toutes les conditions d’entreposage pendant la durée de l’étude. Les solutions de magnésium à 100 mg/mL sont restées stables physiquement lorsqu’elles étaient conservées à 25 °C.
Conclusion: Les préparations de propofol à 20 mg/mL peuvent être conservées à la température ambiante et à 5 °C pendant 14 jours, tandis que celles à 10 mg/mL doivent l’être à 5 °C pour demeurer stable durant cette période lorsqu’elles sont reconditionnées en seringue de polypropylène. Les préparations de rocuronium à 10 mg/mL, de phénobarbital à 60 mg/mL et de sulfate de magnésium à 100 mg/mL reconditionnées en seringue de polypropylène, peuvent être gardées à la température ambiante pendant 10 jours, 30 jours et 10 jours, respectivement.
Mots-clés: aide médicale à mourir, bromure de rocuronium, phénobarbital, propofol, stabilité physico-chimique, sulfate de magnésium
Abstract
Objective: Injectable drugs for medical aid in dying have a relatively short beyond-use date. A series of studies have evaluated the extended chemical and physical stability of propofol, rocuronium, and phenobarbital as well as the physical stability of magnesium sulfate.
Method: Preparations were packaged in 20 mL polypropylene syringes and stored at room temperature and refrigerated at 5°C (for propofol only). The physicochemical stability of rocuronium, propofol and phenobarbital was assessed by high-performance liquid chromatography over 10, 14, and 30 days. For magnesium, the number of particles was determined over 10 days using test 1.B in chapter <788> of the United States Pharmacopeia.
Results: The propofol syringes at 20 mg/mL remained stable throughout the study, while those at 10 mg/mL remained stable when stored at 5°C only. The concentrations of rocuronium and phenobarbital remained above 90% of the initial concentration under all the storage conditions throughout the study. The magnesium solutions at 100 mg/mL remained physically stable when stored at 25°C.
Conclusion: Propofol preparations at 20 mg/mL can be stored at room temperature and at 5°C for 14 days, while those at 10 mg/mL must be stored at 5°C to ensure stability over the same period when repackaged in polypropylene syringes. Rocuronium preparations at 10 mg/mL, phenobarbital preparations at 60 mg/mL, and magnesium sulfate preparations at 100 mg/mL repackaged in polypropylene syringes can be stored at room temperature for 10 days, 30 days and 10 days, respectively.
Keywords: Magnesium sulfate, medical aid in dying, phenobarbital, physicochemical stability, propofol, rocuronium bromide
En décembre 2015, le Québec a fait preuve d’ouverture et a participé à un avancement important dans la prestation des soins en rendant accessible l’aide médicale à mourir (AMM)1. Bien que le professionnel qui administre l’AMM joue un rôle central dans la démarche, une collaboration étroite avec le pharmacien est nécessaire et de mise. L’AMM représente un certain nombre de défis dans un département de pharmacie. Dans ce processus de soin, le pharmacien est responsable de la préparation des médicaments requis pour l’AMM, tout en assurant un service pharmaceutique de qualité et sûr. La possibilité de préparer des trousses avec des fioles commerciales constitue une option intéressante dans certaines situations.
Toutefois, la stabilité observée en seringue offre une plus grande flexibilité dans l’organisation des services liés à l’AMM.
Idéalement, ces médicaments doivent être préparés dans des seringues réparties dans deux trousses scellées contenant généralement un anxiolytique, un anesthésique local, un inducteur de coma, un bloqueur neuromusculaire et du chlorure de sodium1,2. Leur stabilité physico-chimique, selon le document intitulé L’aide médicale à mourir : guide d’exercice et lignes directrices pharmacologiques, est très variable, allant de 24 heures à 90 jours1. Par exemple, dans le cas du rocuronium, un bloqueur neuromusculaire, et du propofol, un inducteur de coma, des stabilités empiriques de 48 heures et de 24 heures respectivement ont été attribuées en l’absence de données probantes, ce qui est parfois trop court pour permettre une flexibilité dans la prestation des soins de l’AMM1. Cette stabilité est beaucoup plus longue pour d’autres médicaments, comme par exemple de 30 jours pour le cisatracurium et de quatre semaines à l’abri de la lumière pour le midazolam, tous deux en seringue à la température ambiante1.
Il arrive régulièrement que l’AMM soit demandée la fin de semaine pour accommoder la famille et pour respecter le souhait du patient qui en fait la demande. Or, le temps de préparation des trousses de médicaments est estimé à environ 2 heures par l’équipe de la pharmacie. Par manque de données, la stabilité de certains médicaments dans la trousse est fixée empiriquement à 24 heures dans le guide de préparation, ce qui rend impossible la préparation à l’avance des trousses en semaine.
Une meilleure fluidité du processus de préparation et de gestion des trousses est souhaitable. C’est pourquoi une étude de stabilité du propofol, du bromure de rocuronium, du phénobarbital et du sulfate de magnésium a été menée pour tenter de prolonger la stabilité de ces injectables, autrement fixée empiriquement. L’objectif est d’évaluer la stabilité chimique et physique de trois médicaments injectables reconditionnés en seringue de polypropylène (soit le propofol, le bromure de rocuronium et le phénobarbital) lorsqu’ils sont entreposés à la température ambiante ainsi qu’au réfrigérateur à 5 °C (propofol seulement) pendant une période prédéterminée allant jusqu’à 14, 10 et 30 jours, respectivement. De même, la stabilité physique du magnésium a été évaluée dans des seringues de polypropylène entreposées à la température ambiante sur une période allant jusqu’à 10 jours.
Deux concentrations et quatre fournisseurs de propofol ont été testés, soit Aspen, Baxter, Actavis et Fresenius Kabi pour les solutions à 10 mg/mL et Fresenius Kabi pour celles à 20 mg/ mL. Une concentration de 10 mg/mL et quatre fournisseurs de rocuronium ont été testés, soit Pfizer, Athenex, Sandoz et Juno. Une concentration d’un seul fournisseur a été testée pour le phénobarbital, soit 60 mg/mL de Sandoz (dilution 1:1, v:v de 120 mg/mL dans du NaCl à 0,9 %), et pour le magnésium, 100 mg/mL (dilution 1:4, v:v de 500 mg/mL dans du NaCl à 0,9 %). Toutes ces solutions ont été reconditionnées en seringue de polypropylène (BD, Becton Dickinson, Franklin Lakes, NJ, É.-U.) en respectant les conditions de stérilité de la norme de l’Ordre des pharmaciens du Québec (OPQ) 2014.01 et envoyées à la plateforme de biopharmacie de la Faculté de pharmacie de l’Université de Montréal le jour même pour l’évaluation du temps zéro3. Un contenant de transport isotherme a été utilisé, au besoin.
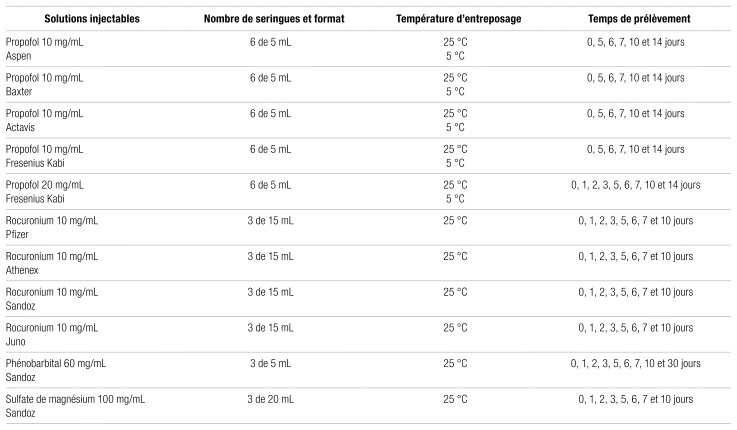
Pour chaque fournisseur et chaque concentration de propofol, trois seringues ont été entreposées à 25 °C et à 60 % d’humidité relative et trois autres seringues à 5 °C. Pour le rocuronium et le phénobarbital, trois seringues ont été entreposées à 25 °C et à 60 % d’humidité relative pour chaque fournisseur. Pour le magnésium, trois seringues ont été entreposées à 25 °C et à 60 % d’humidité relative. Les détails des conditions d’entreposage et des temps de prélèvement pour chaque médicament sont présentés dans le tableau I. Au moment voulu, les différents échantillons étaient prélevés et conservés à −80 °C pour des analyses simultanées subséquentes.
Les solutions injectables ont été observées pour évaluer tout changement physique durant l’étude (couleur, phases, limpidité, etc.), une modification de l’apparence signifiant une possible instabilité de la solution injectable.
Pour les solutions injectables de propofol à 10 mg/mL, 10 μL ont été transférés dans un flacon pour injection contenant 990 μL de méthanol. Pour les solutions à 20 mg/mL, 10 μL ont été transférés dans 1990 μL de méthanol (concentration théorique finale de 100 μg/mL pour tous les échantillons de propofol). Pour les solutions de rocuronium à 10 mg/mL, le jour de l’analyse, les tubes conservés à −80 °C contenant les aliquotes prélevés à chaque temps de prélèvement ont été dégelés à la température ambiante. Chaque tube a été mélangé par vortex, puis 20 μL ont été transférés dans 980 μL d’acétonitrile pour une concentration finale de 200 μg/mL. Pour les solutions de phénobarbital à 60 mg/mL, 100 μL ont été dilués avec 500 μL d’acétonitrile, puis 10 μL de cette solution ont été dilués avec 990 μL d’acétonitrile, pour une concentration finale de 100 μg/mL. Toutes ces solutions ont été analysées par CLHP à ultra-violet (CLHP-UV) selon les paramètres indiqués du tableau II.
Le système de CLHP-UV (Prominence UFLC, Shimadzu, Laval, QC, Canada) consiste en un injecteur réfrigéré SIL-20AC HT, un dégazeur DGU-20A5, une pompe binaire LC-20AD, un chauffe-colonne CTO-20AC et un détecteur à barrettes de diodes SPD-M20A. La liste des consommables, ainsi que leurs concentrations, lots et fournisseurs, se trouve en annexe.
Des solutions standard de propofol et de phénobarbital à 1 mg/mL dans le méthanol ont été achetées. Une solution standard de bromure de rocuronium à 1 mg/mL dans l’acétonitrile a été préparée à partir de poudre. Une courbe de calibration en six points a été préparée pour chaque composé dans le même solvant que leur solution mère, à 0, 80, 90, 100, 110 et 120 μg/mL pour le propofol et le phénobarbital et à 0, 160, 180, 200, 220 et 240 μg/mL pour le bromure de rocuronium. Les échantillons pour les courbes de calibration ont été injectés en triplicata à chaque analyse par CLHP-UV. La variabilité intra-jour a été calculée avec les injections pour chaque élément de la courbe de calibration en triplicata le même jour. La variabilité inter-jour a été calculée pour chaque élément de la courbe de calibration injecté trois fois par jour pendant trois jours consécutifs.
Un lot pilote de chaque solution a été préparé et dilué six fois, comme mentionné dans la section de préparation des échantillons, pour évaluer la récupération de la méthode d’extraction. Les échantillons ont été injectés selon les méthodes de CLHP-UV mentionnées précédemment, pour chaque composé, et les concentrations ont été calculées avec les courbes de calibration respectives.
Pour tester la stabilité des échantillons au cycle gel/dégel, un lot pilote de chaque solution a été préparé et trois aliquotes de 1 mL de chaque préparation ont été prélevés, puis transférés dans un tube Eppendorf et placé à −80 °C. Les tubes ont été dégelés à la température ambiante et recongelés à −80 °C trois fois avant d’être dilués pour injection dans le système de CLHP-UV. Les aires des pics sous la courbe ont été comparées avec celles de solutions fraîches.
Tableau I Sommaire de l’étude de stabilité

Tableau II Paramètres d’analyse CLHP-UV

Des dégradations forcées ont été effectuées sur chaque solution injectable pour vérifier la capacité des méthodes de CLHP-UV de séparer les produits de dégradation du composé parent. Une aliquote de 1 mL de chaque produit a été diluée dans 10 μL d’eau, 10 μL d’acide chlorhydrique 1M, 10 μL d’hydroxyde de sodium 1M ou 10 μL de peroxyde d’hydrogène à 30 %. Les solutions ont été placées à 60 °C pendant 4 heures et une solution témoin dans 10 μL d’eau à 4 °C pendant la même période. Après l’incubation, les solutions ont été neutralisées et diluées pour l’injection dans l’appareil de CLHP-UV. Les chromatogrammes obtenus pour les solutions placées à 60 °C ont été comparés à ceux des solutions témoins gardées à 4 °C.
La stabilité est définie par une concentration qui n’est pas inférieure à 90 % de la concentration initiale de départ, conformément à l’énoncé du comité d’experts en préparations magistrales de la United States Pharmacopeia (USP)4.
Pour le sulfate de magnésium, les exigences relatives au comptage des particules des solutions injectables fournies dans des contenants de moins de 100 mL (test 1.B de la norme <788> de l’USP) ont été appliquées pour l’évaluation de la stabilité physique des solutions5. Le nombre de particules a été évalué initialement et à plusieurs reprises sur 10 jours à l’aide d’un compteur de particules LS-20 (Lighthouse Worldwide Solutions, Fremont, CA, USA). Un volume de 20 mL de chaque échantillon a été analysé en triplicata selon la norme <788> de l’USP5.
La linéarité des courbes standard a été démontrée pour chaque composé avec des coefficients de détermination (r2) tous supérieurs à 0,9997. La variabilité intra-jour était inférieure à 0,2 % pour chaque composé et la variabilité inter-jour, inférieure à 1,0 %. Les récupérations de la méthode d’extraction variaient en moyenne de 97 à 110 %, et les composés étaient stables au cycle gel/dégel avec entre 97 et 103 % de récupération.
Aucune superposition des pics de propofol, de rocuronium et de phénobarbital avec des excipients, impuretés ou produits de dégradation n’a été observée. L’indice de pureté des pics d’actifs est demeuré supérieur à 0,9999 dans toutes les conditions de dégradation forcée. L’incubation à 60 °C en condition acide, basique, oxydative et aqueuse a mené respectivement à des récupérations de 99 %, 98 %, 109 % et 96 % pour le propofol, de 101 %, 98 %, 99 % et 102 % pour le rocuronium et de 93 %, 95 %, 17 % et 65 % pour le phénobarbital. Les figures 1,2 et 3, en annexe, illustrent respectivement pour le propofol, le rocuronium et le phénobarbital, les courbes standard obtenues.
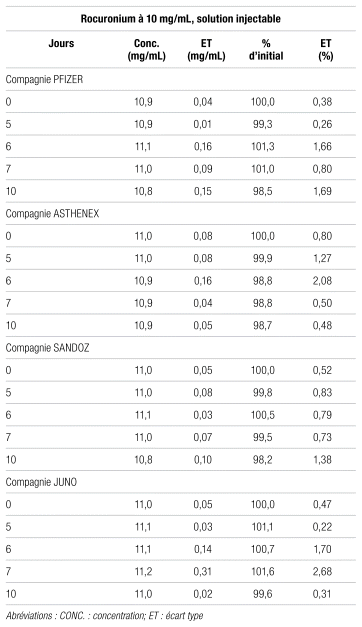
Les solutions injectables de propofol à 10 mg/mL provenant de quatre fournisseurs et à 20 mg/mL d’un seul fournisseur ont été testées. Pour chaque température d’entreposage, la préparation de propofol à 20 mg/mL est demeurée stable pendant toute la durée de l’étude. Cependant, les concentrations de certaines préparations de propofol à 10 mg/mL ont dépassé la limite inférieure de stabilité de 90 % de la teneur initiale lorsqu’elles étaient entreposées à 25 °C, tandis qu’elles demeuraient stables à 5 °C, comme le montre le tableau III. Aucun changement physique n’a été observé pour toutes les solutions de propofol pendant 14 jours.
Comme le montre le tableau IV, les concentrations de rocuronium des quatre fournisseurs sont demeurées supérieures à 90 % de la concentration initiale pendant l’étude, soit 10 jours, et aucun changement physique n’a été observé.
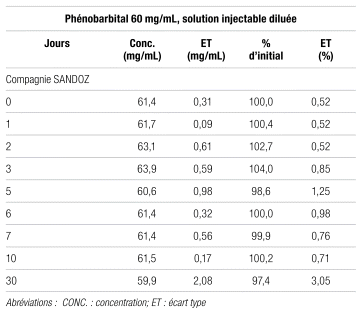
Pour le phénobarbital, les solutions ont été préparées en milieu stérile à partir d’une solution commerciale de phénobarbital à 120 mg/mL diluée dans un rapport de 1 pour 1 avec du NaCl à 0,9 %. Les solutions de phénobarbital à 60 mg/mL sont demeurées stables physiquement et chimiquement pendant toute la durée de l’étude, soit 30 jours (tableau V).
Les critères du test 1.B de la norme <788> de l’USP définissent un nombre moyen de particules d’une taille égale ou supérieure à 10 μm à moins de 6000 par contenant et d’une taille égale ou supérieure à 25 μm à au plus 600 par contenant5. Dans le contexte de l’étude (volume exact de la solution testée égal à 20 mL), le nombre total de particules admis par millilitre est de 300 pour la taille de 10 μm et de 30 pour la taille de 25 μm5. Le nombre de particules détectées dans tous les échantillons testés respectait les critères d’évaluation du test 1.B. Le nombre de particules d’une taille inférieure à 10 microns n’a jamais dépassé trois et celui de particules d’une taille inférieure à 25 microns n’a jamais dépassé un.
Tous les médicaments visés par l’étude sont susceptibles d’être affectés par des phénomènes de dégradation, principalement l’hydrolyse de certaines fonctions moléculaires. Par exemple, dans la littérature, de tels phénomènes sont mentionnés, tant pour le rocuronium que pour le phénobarbital, d’où l’importance de faire une étude de stabilité en bonne et due forme6–8.
Les études effectuées avaient pour but de déterminer la stabilité physico-chimique ou physique des médicaments ciblés reconditionnés en seringue de polypropylène. Les préparations injectables de propofol à 10 mg/mL de quatre fournisseurs (Aspen, Baxter, Actavis et Fresenius Kabi) et à 20 mg/mL d’un seul fournisseur (Fresenius Kabi) ont été entreposées à 25 °C et à 5 °C dans des seringues en polypropylène pendant 14 jours. Aux deux températures, la solution de propofol à 20 mg/mL est demeurée stable pendant 14 jours. Cependant, les préparations à 10 mg/mL ont montré des concentrations variables lorsqu’elles étaient gardées à 25 °C, à des concentrations sous la limite de 90 % aux jours 5 et 6. Cette variabilité n’a pas été observée avec les préparations entreposées à 5 °C analysées simultanément avec la même méthode d’extraction. Ces préparations sont demeurées stables pendant 14 jours. Il est donc recommandé de conserver les solutions de propofol à 10 mg/mL conditionnées en seringue de polypropylène à 5 °C pendant 14 jours.
Les solutions injectables de rocuronium à 10 mg/mL de Pfizer, Athenex, Sandoz et Juno sont restées stables pendant toute la durée de l’étude, soit 10 jours, lorsqu’elles étaient conditionnées en seringue de polypropylène et entreposées à la température ambiante.
Tableau III Stabilité du propofol en seringues de polypropylène
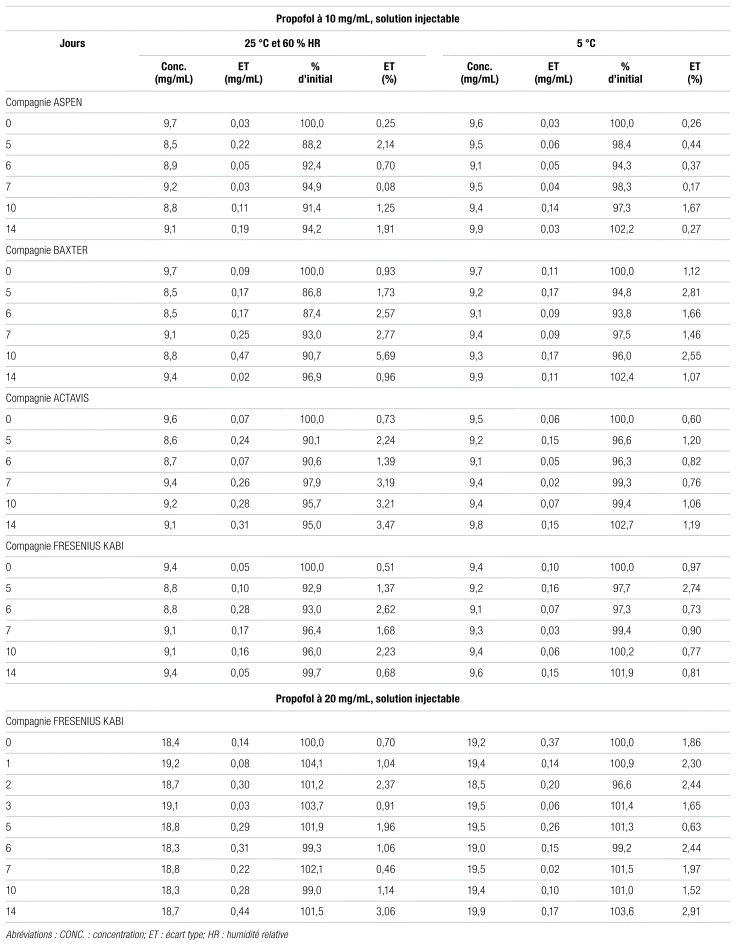
Tableau IV Stabilité du rocuronium en seringues de polypropylène, à 25 °C et 60 % d’humidité relative
La solution de phénobarbital à 60 mg/mL (dilution de 1 pour 1 à partir de la solution à 120 mg/mL de Sandoz en utilisant du NaCl à 0,9 %) est demeurée stable pendant au moins 30 jours dans les seringues de polypropylène conservées à la température ambiante.
En considérant les limites d’acceptation du test 1.B de la norme <788> de l’USP, les solutions injectables de sulfate de magnésium à 100 mg/mL dans du NaCl à 0,9 % conditionnées dans des seringues en polypropylène de l’entreprise Becton Dickinson sont demeurées stables physiquement pendant au moins 10 jours à la température ambiante5.
Il est important de rappeler que, puisque l’objectif de cette étude était d’évaluer la durée de stabilité physico-chimique des médicaments dans les trousses d’AMM, aucun test de stabilité microbiologique n’a été effectué sur les échantillons, compte tenu de la finalité des préparations1. Ces données doivent donc être utilisées uniquement pour les patients dans un contexte d’AMM et pour aucune autre indication, conformément à la norme 2014.01 de l’OPQ3.
Tableau V Stabilité du phénobarbital en seringues de polypropylène, à 25 °C et 60 % d’humidité relative
Sachant que les trousses peuvent être composées de midazolam (stable pendant quatre semaines), de lidocaïne (stable pendant 90 jours) ou de magnésium, de NaCl à 0,9 % en vente commercialement, de propofol, de phénobarbital, de rocuronium ou de cisatracurium (stable pendant 30 jours), les résultats de la présente étude permettent de préparer les trousses de médicaments pour l’AMM jusqu’à 10 jours d’avance lorsque l’on utilise le propofol à 20 mg/ml ou si les seringues de propofol 10 mg/mL sont conservées au réfrigérateur. Ainsi, il sera possible de préparer les trousses d’AMM en semaine pour des soins prodigués la fin de semaine.
Des seringues préparées selon les conditions décrites dans la norme 2014.01 de l’OPQ et destinées à l’administration de l’AMM sont stables selon les critères physico-chimiques dans les conditions suivantes : propofol (1000 mg/50 mL) pendant 14 jours à la température ambiante ou réfrigéré, propofol (500 mg/50 mL) pendant 14 jours à 5 °C, rocuronium (200 mg/20 mL) pendant 10 jours à la température ambiante, phénobarbital (3000 mg/50 mL) pendant 30 jours à la température ambiante, magnésium (1000 mg/10 mL) pendant 10 jours à la température ambiante, sans égard à quelque test microbiologique que ce soit vu leur finalité3. Des discussions en comité interdisciplinaire et au sein du Département de pharmacie pourront permettre de mettre en place des mesures pour faciliter l’AMM au sein de l’organisation. Avec ces nouvelles stabilités et une communication entre le pharmacien et le professionnel qui administre l’AMM dès qu’elle est envisagée, l’équipe de pharmacie sera en mesure de mieux planifier.
Certains auteurs ont reçu un financement pour effectuer cette étude. Les frais de laboratoire de la plateforme de biopharmacie de la Faculté de pharmacie de l’Université de Montréal ont ainsi été payés par le Centre intégré de santé et de services sociaux de la Montérégie-Est.
Tous les auteurs ont soumis le formulaire de l’ICMJE sur la divulgation de conflits d’intérêts potentiels et n’ont déclaré aucun conflit d’intérêts lié à cet article.
Les auteurs aimeraient remercier Francine Vinet et Lucie Houle, respectivement pharmacienne et assistante technique séniore en pharmacie du Centre intégré de santé et de services sociaux de la Montérégie-Est, pour leur participation à cette étude menée conjointement avec le personnel de la plateforme de biopharmacie de la Faculté de pharmacie de l’Université de Montréal. Ces personnes ont donné leur autorisation écrite.
1. Collège des médecins du Québec, Ordre des pharmaciens du Québec, Ordre des infirmières et infirmiers du Québec, Ordre des travailleurs sociaux et des thérapeutes conjugaux et familiaux du Québec, Barreau du Québec et Chambre des notaires du Québec. L’aide médicale à mourir : guide d’exercice et lignes directrices pharmacologiques, mise à jour novembre 2017. [en ligne] https://www.otstcfq.org/wp-content/uploads/2018/09/aide_medicale_a_mourir_-_2017.pdf (site visité le 20 avril 2024).
2. Centre intégré universitaire de santé et de services sociaux du Saguenay–Lac-Saint-Jean. Registre d’utilisation des médicaments d’aide médicale à mourir à l’intention du médecin et du pharmacien. [en ligne] https://santesaglac.gouv.qc.ca/medias/Professionnels/Soins_palliatifs/reg0098-registre_dutilisation_des_medicaments_-amm.pdf (site visité le 4 février 2020).
3. Ordre des pharmaciens du Québec. Norme 2014.01 – Préparation de produits stériles non dangereux en pharmacie (octobre 2017). [en ligne] https://www.opq.org/wp-content/uploads/2020/03/1827_38_fr-ca_0_norme201401_prod_steriles_non_dang_oct2017.pdf (Site visité le 18 septembre 2024).
4. Allen LV, Bassani GS, Elder EJ, Parr AF. Strength and stability testing for compounded preparations (13 janvier 2014). [en ligne]. https://www.usp.org/sites/default/files/usp/document/FAQs/strength-stability-testingcompounded-preparations.pdf.
5. Norme <788> de l’USP. Particulate matter in injections. Dans : United States Pharmacopeia. USP 36. Rockville, MD; United States Pharmacopeia; 2021. p. 350–3.
6. Heeb RM, Kramer RI. Physicochemical stability of rocuronium bromide injection solution 10 mg/mL as bulk solution and in 10 mL ready-to-administer syringes. Eur J Hosp Pharm 2018; 25(suppl 1):A36.
7. Nahata MC, Hipple TF, Strausbaugh SD. Stability of phenobarbital sodium diluted in 0.9 % sodium chloride injection. Am J Hosp Pharm 1986;43:384–5.
PubMed
8. Garrett ER, Bojarski JT, Yakatan GJ. Kinetics of hydrolysis of barbituric acid derivatives. J Pharm Sci 1971;60:1148–54.
Crossref
Pour toute correspondance : Diem Vo, Centre intégré de santé et de services sociaux de la Montérégie-Est, 1333, boulevard Jacques-Cartier Est, Bureau B1.17, Longueuil (Québec) J4M 2A5, CANADA; Téléphone : 450-468-8111, poste 82930; Télécopieur : 450-468-8034; Courriel : diem.vo.cisssme16@ssss.gouv.qc.ca
PHARMACTUEL, Vol. 57, No. 4, 2024