Marianne Girard1, Pharm.D., M.Sc., Amélie Poirier2, B.Pharm., M.Sc., Pierre-Michel Bédard3, M.D., Mia Robert4, M.D., Mahukpe Narcisse Ulrich Singbo5, B. Sc., M.Sc., Denis Soulet6, Ph.D., Marie-Claude Michel2, B.Pharm., M.Sc.
1Pharmacienne, Centre intégré de santé et de services sociaux de Chaudière-Appalaches, Hôpital de Montmagny, Montmagny (Québec) Canada;
2Pharmacienne, CHU de Québec–Université Laval, Québec (Québec) Canada;
3Médecin, Département de médecine, Service d’immuno-allergologie, CHU de Québec–Université Laval, Québec (Québec) Canada;
4Médecin résidente de 4e année en médecine interne au moment de la rédaction, Faculté de médecine, Université Laval, Québec (Québec) Canada;
5Biostatisticien, CHU de Québec–Université Laval, Québec (Québec) Canada;
6Professeur titulaire, Faculté de Pharmacie, Université Laval, chercheur régulier, Centre de recherche du CHU de Québec–Université Laval, Québec (Québec) Canada
Reçu le 27 juin 2024; Accepté après révision par les pairs le 29 janvier 2025
DOI: https://doi.org/10.63209/2025.1565
Résumé
Objectif: Évaluer le rôle d’une ordonnance pharmaceutique individuelle standardisée dans le traitement médicamenteux de l’anaphylaxie chez l’adulte au CHU de Québec–Université Laval.
Méthode: Une ordonnance pharmaceutique individuelle standardisée a été déployée en septembre 2018 à la suite de la découverte de problèmes liés à l’administration d’épinéphrine lors du traitement de l’anaphylaxie. Pour réaliser un suivi de cette intervention et déterminer s’il existe encore des lacunes dans le traitement de l’anaphylaxie, nous avons vérifié, en 2020, l’usage de l’ordonnance et réévalué les traitements et la prise en charge à l’urgence et sur les unités de soins.
Résultats: L’étude comprenait 297 réactions anaphylactiques diagnostiquées à l’urgence et sur les unités de soins entre le 25 septembre 2018 et le 31 décembre 2020. De ce nombre, 270 (91 %) ont reçu au moins une dose d’épinéphrine, dont quatre par voie intraveineuse en première intention. Des doses allant jusqu’à 1 mg en bolus intraveineux ont été administrées. Parmi les cas à l’étude, seulement 156 (53 %) respectaient les critères diagnostiques de la World Allergy Organization 2020. L’ordonnance standardisée a été utilisée dans 21 (8 %) dossiers.
Conclusion: L’épinéphrine pose encore un défi. En effet, elle n’est pas toujours le médicament administré en première intention, et des doses trop élevées sont parfois données par voie intraveineuse. L’ordonnance pharmaceutique de 2018 a été très peu employée. Elle a été mise à jour en 2024, et d’autres actions ont été entreprises pour améliorer la qualité de l’acte.
Mots clés: épinéphrine, anaphylaxie, choc anaphylactique, formulaire d’ordonnances pharmaceutiques, ordonnance pharmaceutique individuelle standardisée, réaction anaphylactique
Objective: Evaluate the role of an individual standardized pharmaceutical prescription in the drug treatment of anaphylaxis in adults at CHU de Québec–Université Laval.
Method: An individual standardized pharmaceutical prescription was deployed in September 2018 following the findings of safety issues with epinephrine administration during anaphylaxis treatment. To monitor this intervention and determine if there are still gaps in anaphylaxis treatment, we checked, in 2020, the use of the standardized prescription and reevaluated treatments and management in the emergency department and care units.
Results: The study included 297 anaphylactic reactions diagnosed in the emergency department and care units between September 25, 2018, and December 31, 2020. Of these, 270 (91%) received at least one dose of epinephrine, including four intravenously as first-line treatment. Bolus doses up to 1 mg intravenous were administered. Among the cases studied, only 156 (53%) met the diagnostic criteria of the World Allergy Organization 2020. The standardized prescription was used in 21 (8%) cases.
Conclusion: Epinephrine still poses issues. It is not always the first-line medication administered, and excessively high doses are sometimes given intravenously. The 2018 pharmaceutical prescription was very rarely used. It was updated in 2024, and further actions have been taken to improve the quality of care.
Keywords: epinephrine, anaphylaxis, anaphylactic shock, pharmaceutical prescription form, individual standardized pharmaceutical prescription, anaphylactic reaction
L’anaphylaxie est une réaction allergique grave d’apparition rapide, le plus souvent généralisée pouvant causer la mort. Les tableaux cliniques sont multiples et de gravité variable1–4. Dans le monde, de 0,3 à 5,1 % de la population subira au cours de sa vie une réaction anaphylactique. L’incidence varie de 50 à 112 anaphylaxies pour 100 000 personnes-années. Cependant, la mortalité est faible, soit de 0,03 à 0,51 décès par million de personnes-années, selon l’agent causal et les maladies concomitantes des patients1,5,6.
Les critères diagnostiques de l’anaphylaxie tels que décrits par la World Allergy Organization (WAO) en 2020 nécessitent l’apparition soudaine de symptômes regroupés selon deux tableaux cliniques possibles. Le premier, pour 90 % des cas, implique une atteinte mucocutanée généralisée en plus de l’atteinte d’un deuxième système1. Le second permet de diagnostiquer l’anaphylaxie en l’absence des symptômes mucocutanés caractéristiques après l’exposition à un allergène connu ou suspecté, mais avec l’apparition d’hypotension artérielle grave isolée d’apparition rapide (pression artérielle systolique de 90 mmHg ou moins), un bronchospasme grave (saturation inférieure à 85 %) ou encore un œdème laryngé aigu1.
Le traitement médicamenteux vise à neutraliser les effets des médiateurs mastocytaires relargués lors d’une réaction allergique, responsables de la vasodilatation, de l’inflammation aiguë et de la contraction de certaines fibres musculaires lisses dans les organes cibles2. L’épinéphrine est le traitement de première intention. Son administration tardive ou sa sous-utilisation est associée à des résultats cliniques moins favorables. En effet, plusieurs études qui ont analysé la mortalité lors d’une réaction anaphylactique indiquent que le facteur principal ayant contribué à une évolution mortelle est soit l’absence d’injection d’épinéphrine, soit son administration trop tardive (plus de 90 minutes)7–10. De plus, la voie intraveineuse n’est pas recommandée en première intention en raison du risque augmenté d’effets indésirables cardiaques, principalement des arythmies ou des infarctus11. Cependant, c’est une option chez les patients ne répondant pas aux injections intramusculaires12. La voie intramusculaire est aussi préférée à la voie sous-cutanée, car elle permet d’atteindre des concentrations plasmatiques et tissulaires plus élevées plus rapidement13. Le glucagon est indiqué chez les patients prenant des bêtabloquants et ne répondant pas à l’épinéphrine par voie intramusculaire.
Les traitements de soutien ne doivent jamais retarder ou remplacer l’épinéphrine par voie parentérale. Ainsi, l’épinéphrine par nébulisation est employée en cas d’obstruction des voies respiratoires supérieures. Quant aux agonistes bêta-adrénergiques (p. ex. : salbutamol), ils figurent parmi l’arsenal thérapeutique en présence d’obstruction des voies respiratoires inférieures (bronchospasme) et peuvent être administrés sous forme de nébules ou d’aérosols-doseurs avec chambre d’espacement. Les antagonistes des récepteurs H1 de l’histamine sont utiles pour le soulagement des symptômes cutanés (démangeaisons, urticaire)14. Enfin, les corticostéroïdes peuvent être administrés en cas d’anaphylaxie réfractaire, notamment chez les patients asthmatiques qui présentent un bronchospasme2. Ils jouent aussi un rôle potentiel dans la prévention des réactions anaphylactiques tardives importantes15.
Malgré une littérature abondante depuis plusieurs décennies, les principaux problèmes liés à la prise en charge de l’anaphylaxie demeurent la difficulté à reconnaître les signes et symptômes, le délai, la voie d’administration non optimale pour l’épinéphrine et la prise en charge après le séjour hospitalier. Dans cette étude, nous voulions vérifier si une ordonnance pharmaceutique individuelle standardisée peut combler ces lacunes. La distinction entre une réaction allergique et une anaphylaxie reste encore un défi pour plusieurs cliniciens16. Sur le plan médical, des études décrivent un manque de connaissances des intervenants de première ligne sur cette situation critique. D’autres études indiquent aussi que les antihistaminiques et les corticostéroïdes sont prescrits plus souvent que l’épinéphrine en première intention8,9. Enfin, en ce qui concerne le suivi des patients après une réaction anaphylactique, Kastner et coll. mentionnent de faibles taux de prescription d’auto-injecteurs d’épinéphrine et une orientation insuffisante en spécialité17.
En 2018, au CHU de Québec–Université Laval, ci-après nommé CHU de Québec–UL, quatre erreurs majeures ont été repérées dans le traitement de l’anaphylaxie dont trois ont mené à une hospitalisation aux soins intensifs. Les erreurs étaient liées à l’usage de l’épinéphrine par voie intraveineuse (inapproprié en première intention), une administration en bolus trop rapide (en une minute), une confusion entre les doses recommandées par voie intramusculaire et intraveineuse (ayant entraîné une dose trop élevée) et une erreur de calcul des doses en millilitres (à partir de la notation 1:1000 sur les fioles d’épinéphrine). Afin de rendre les soins plus sûrs, le Département de pharmacie a ajouté une étiquette apposée sur le sac lors du service des fioles d’épinéphrine pour rappeler certaines informations clés et a rendu disponible, depuis le 25 septembre 2018, une ordonnance pharmaceutique individuelle standardisée présentée en annexe (figure 1). Le recours à un formulaire de prise en charge comprenant une aide au diagnostic et un algorithme pharmaceutique à l’urgence pour l’anaphylaxie a déjà été mentionné par Manivannan et coll. comme une solution avantageuse. Dans leur étude, le taux d’administration d’épinéphrine par voie intramusculaire après la mise en œuvre de cet outil est ainsi passé de 33 à 51 %18.
L’objectif principal de cette étude est de décrire le traitement médicamenteux de l’anaphylaxie chez l’adulte au CHU de Québec–UL. Les objectifs secondaires sont d’évaluer la conformité des diagnostics d’anaphylaxie selon les critères de la WAO 2020, de mesurer le taux d’utilisation de l’ordonnance pharmaceutique individualisée standardisée de 2018 et d’évaluer la conformité des ordonnances avec cette dernière selon quatre indicateurs : le choix des médicaments, les doses, les voies d’administration et l’administration de l’épinéphrine par voie intramusculaire en première intention.
Nous présentons ici une réévaluation du traitement et de la prise en charge de l’anaphylaxie deux ans après le déploiement de cette ordonnance pharmaceutique individuelle standardisée qui est centrale à notre intervention.
Il s’agit d’une étude descriptive de population longitudinale avec collecte de données rétrospective, menée dans un centre tertiaire universitaire regroupant cinq hôpitaux. Étant donné que l’étude était considérée comme une évaluation de la qualité de l’acte, une approbation du comité d’éthique n’était pas requise. Le projet a été autorisé par la Direction des services professionnels. Le protocole a été rédigé par une équipe de pharmaciens, une résidente en médecine interne et un immuno-allergologue.
Les patients ont été trouvés par le Service des archives médicales à l’aide des diagnostics «réaction anaphylactique» et «choc anaphylactique». La population étudiée incluait tous les patients de 18 ans ou plus ayant reçu ces diagnostics à l’urgence ou sur une unité de soins (courants ou intensifs) entre le 25 septembre 2018 et le 31 décembre 2020. Les réactions prises en charge uniquement aux blocs opératoires et en cliniques externes ont été exclues en raison d’un contexte de soins non comparable et des difficultés liées à la traçabilité de l’information.
Les doses d’épinéphrine reçues en préhospitalier ont été considérées pour évaluer l’ordre d’administration des traitements. La prise en charge à l’urgence a été comparée à celle des unités de soins. Nous avons aussi répertorié les causes potentielles d’anaphylaxie et, lorsqu’elles étaient possiblement de nature médicamenteuse, nous avons vérifié si la pharmacie de l’établissement en avait été avisée. Enfin, dans une perspective de prise en charge globale, nous avons déterminé le nombre de patients orientés en immuno-allergologie et vérifié la fréquence de prescription d’épinéphrine auto-injectable au congé.
Les analyses statistiques ont été menées avec l’aide d’un biostatisticien et du logiciel SAS (version 9.4). Selon les calculs, l’inclusion de 200 cas permettait d’obtenir un intervalle de confiance à 95 % avec une précision de plus ou moins 7 % pour une proportion estimée à 50 %19,20. Des analyses de sous-groupes, prévues au protocole, sur les cas confirmés d’anaphylaxie ont été effectuées. Elles ont aussi été stratifiées selon le lieu de traitement (urgence ou unités de soins). Les résultats de ces deux secteurs ont été comparés à l’aide du test du Khi deux pour les variables qualitatives. Quant aux variables quantitatives, elles ont été décrites par des mesures de tendance centrale et de dispersion. Ces dernières sont présentées sous forme de fréquences.
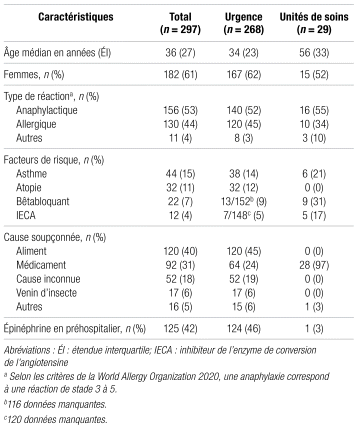
Parmi les 511 cas de réactions anaphylactiques répertoriés, 214 ont été exclus. Il s’agissait d’enfants, de cas d’anaphylaxie pris en charge au bloc opératoire ou en clinique externe ou de doublons. Finalement, 297 cas ont donc été retenus. Les caractéristiques de la population à l’étude sont décrites dans le tableau I.
Tableau I Caractéristiques de la population (n = 297)

Les patients ayant consulté à l’urgence représentaient 90 % des cas recensés. Près de la moitié (48 %) ont été pris en charge par le centre d’orientation en allergologie du CHU de Québec-UL. Les patients des unités de soins étaient plus âgés qu’à l’urgence (médiane de 56 ans contre 35 ans) et prenaient plus fréquemment des bêtabloquants (31 % contre 8 %) et des inhibiteurs de l’enzyme de conversion de l’angiotensine (17 % contre 5 %). L’origine médicamenteuse était plus souvent soupçonnée chez les patients hospitalisés que chez ceux consultant à l’urgence (97 % contre 24 %). La pharmacie de l’établissement a été avisée de l’allergène possible pour 39 des 92 patients pour qui une origine médicamenteuse était évoquée, soit pour 16 de l’urgence et 23 des unités de soins. Les traitements administrés à l’hôpital sont présentés dans le tableau II.
Des 297 réactions incluses, 256 ont reçu au moins un traitement pharmacologique durant leur prise en charge au CHU de Québec–UL et 79 patients ont reçu de l’épinéphrine en préhospitalier sans administration subséquente au cours de la prise en charge intrahospitalière. En tout, 270 patients (91 %) ont eu au moins une dose d’épinéphrine, toutes voies d’administration confondues, y compris les doses avant l’arrivée à l’hôpital et celles à l’hôpital, soit 251 à l’urgence et 19 sur les unités. L’épinéphrine a été donnée par voie intraveineuse à quatre patients n’en ayant pas reçu au préalable par voie intramusculaire. Les patients à qui l’épinéphrine a été administrée par nébulisation en avaient tous reçu au préalable par voie parentérale. La dose d’épinéphrine par voie intramusculaire la plus utilisée était de 0,3 mg, suivie de 0,5 mg. Pour l’épinéphrine par voie intraveineuse, la perfusion a été davantage employée que le bolus. Les doses étaient variables, avec des débits initiaux de 0,01 à 0,5 μg/kg/min et des bolus de 0,1 à 1 mg. Il n’y a pas eu d’administration par voie sous-cutanée.
Tableau II Traitements de l’anaphylaxie au CHU de Québec-Université Laval
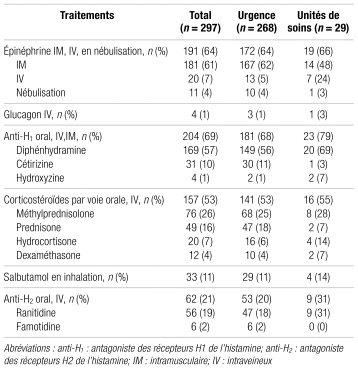
L’ordonnance pharmaceutique individuelle standardisée a été employée dans 21 cas (8 %), dont 20 à l’urgence. Les 41 cas pour lesquels aucun traitement intrahospitalier n’a été administré ont été exclus des analyses de conformité à l’ordonnance pharmaceutique individuelle standardisée (n = 256). Les résultats de conformité détaillés selon chaque indicateur préétabli sont présentés dans le tableau III. Le taux de conformité global à l’ordonnance pharmaceutique individuelle standardisée est de 22 %. Les résultats étaient similaires que le diagnostic soit conforme ou non.
Le taux de prescription d’épinéphrine auto-injectable au congé était de 4 % sur les unités de soins comparativement à 72 % à l’urgence (p < 0,001), tandis que le taux d’orientation en immuno-allergologie était de 36 % sur les unités de soins contre 53 % à l’urgence.
L’anaphylaxie est une affection médicale possiblement mortelle qui nécessite une reconnaissance rapide et un traitement ciblé. Une administration retardée ou une dose inappropriée d’épinéphrine est associée à une morbimortalité accrue. L’intention principale de nos travaux était d’évaluer les traitements médicamenteux et la prise en charge de l’anaphylaxie depuis la mise en place d’une ordonnance pharmaceutique individuelle standardisée.
Dans notre étude, les diagnostics non confirmés étaient en majorité des allergies de stade 1 et 2 non reconnues, selon l’échelle sur 5 de la WAO1. Il s’agissait souvent d’une atteinte cutanée généralisée associée à des symptômes sans signes objectifs d’un deuxième système qui induisait les cliniciens en erreur. D’ailleurs, l’étude de Kastner et coll. l’avait déjà souligné17. En effet, dans sa revue systématique sur la prise en charge de l’anaphylaxie, ce dernier mentionne aussi la difficulté de plusieurs cliniciens de première ligne (jusqu’à 30 à 45 %) à reconnaître les signes d’hypersensibilité généralisée immédiate21. Dans notre étude, les résultats du sous-groupe de cas confirmés ne se distinguent pas des résultats de la population totale, ce qui est cohérent avec le diagnostic initial en fonction duquel les cliniciens ont agi.
Quoiqu’il en soit, les causes présumées les plus fréquentes d’anaphylaxie que nous avons répertoriées concordent avec la littérature, c’est-à-dire une origine alimentaire ou médicamenteuse2,5. De plus, l’incidence des allergènes les plus courants correspond à l’âge médian de chaque groupe et à leur lieu de prise en charge. En effet, les patients hospitalisés étaient plus âgés et davantage exposés à de nouveaux médicaments, tandis que les patients à l’urgence étaient plus jeunes et avaient des antécédents d’atopie.
Tableau III Conformité des prescriptions selon l’ordonnance pharmaceutique individuelle standardisée de 2018 pour le traitement de l’anaphylaxie chez l’adulte au CHU de Québec - Université Laval
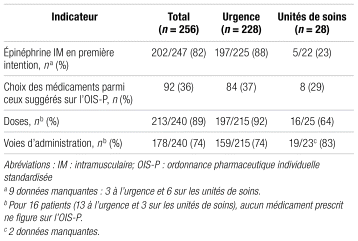
Les résultats ont probablement été influencés par l’absence de limite de cas par hôpital, menant à une proportion beaucoup plus importante d’anaphylaxies dans le centre d’orientation en immuno-allergologie du CHU de Québec–UL, où les cliniciens étaient possiblement plus à l’aise avec la prise en charge. Malgré tout, les ordonnances étaient d’une manière générale peu conformes à l’ordonnance pharmaceutique individuelle standardisée. Bien qu’il ne s’agisse pas de l’élément le moins conforme à l’ordonnance standardisée, le taux de prescription d’épinéphrine en première intention est le plus préoccupant, car il s’agit de la pierre angulaire du traitement de l’anaphylaxie. L’épinéphrine administrée avant l’arrivée des patients à l’urgence ou sur les unités a été comptabilisée pour éviter de sous-estimer le taux réel, étant donné que la prise en charge commence souvent en préhospitalier. Le taux de prescription général est donc beaucoup plus élevé que le taux de prescription intrahospitalier. Le taux de prescription d’épinéphrine dans cette étude est supérieur à celui d’autres études22,23. Cependant, environ le tiers des patients des unités de soins n’en avaient pas reçu. La dose prescrite était principalement de 0,3 mg. Plusieurs hypothèses sont proposées pour expliquer cette situation, la principale étant l’habitude et la connaissance des prescripteurs. Aussi, le poids est rarement pris en considération chez les adultes. D’ailleurs, l’ancienne ordonnance pharmaceutique individualisée standardisée suggérait deux doses possibles, sans égard au poids. Encore à ce jour, la dose de 0,3 mg est fréquemment utilisée. Par ailleurs, l’élimination du recours à la voie intraveineuse en première intention représentait une des cibles principales d’action à la suite des erreurs mentionnées en 2018. Malheureusement, son utilisation en première intention persiste, et les doses sont parfois encore trop élevées. D’ailleurs, dans notre cohorte, un cas de cardiomyopathie de stress attribuable à une dose de 0,5 mg donnée par voie intraveineuse en première intention a été noté. Enfin, nous documentons encore les lacunes évoquées dans l’étude de Kastner et coll., notamment dans la prise en charge, la connaissance des critères diagnostiques et les soins de suivi17.
L’utilisation de médicaments hors ordonnance individuelle, comme des corticostéroïdes différents de l’hydrocortisone, constituait le point le moins conforme (87 % de non-conformité). Toutefois, cette divergence a été jugée cliniquement peu préoccupante puisque les autres corticostéroïdes représentent des options tout aussi valides en anaphylaxie15. Au moment de la création de l’ordonnance pharmaceutique individuelle standardisée en 2018, l’hydrocortisone avait été retenue, en raison de la possibilité de l’administrer par voie intraveineuse et de son moindre coût. Du salbutamol et de l’épinéphrine en nébulisation ont également été recensés dans quelques dossiers, ce qui a contribué à diminuer le taux de conformité, ces produits ne figurant pas sur l’ordonnance standardisée de 2018. La famotidine par voie intraveineuse a été considérée comme conforme puisqu’il s’agissait de l’antagoniste des récepteurs H2 de l’histamine utilisé comme produit de remplacement durant la pénurie de ranitidine au CHU de Québec-UL. La voie d’administration était le second critère de moins bonne conformité à l’ordonnance pharmaceutique individuelle standardisée. Cette situation s’explique par l’administration des antihistaminiques et des corticostéroïdes par voie orale et de l’épinéphrine par nébulisation, ce qui n’était pas suggéré sur le formulaire.
Lorsqu’il y a un risque de réexposition à l’allergène dans la collectivité, une ordonnance d’auto-injecteur d’épinéphrine avec l’enseignement nécessaire devrait être remise au patient avant son congé1. Dans notre étude, le taux de prescription d’épinéphrine auto-injectable est supérieur à l’urgence, probablement dû au doute plus important sur l’allergène et, par conséquent, au plus haut risque de récidive. Les lignes directrices recommandent aussi une orientation en immuno-allergologie, notamment pour confirmer les allergènes soupçonnés, pour prévenir les récidives et prodiguer un enseignement adéquat aux patients1. Les patients du sous-groupe dont le diagnostic d’anaphylaxie a été confirmé ont été significativement plus souvent dirigés en immuno-allergologie, probablement en raison de la gravité clinique de leur état (p = 0,001). Nous déplorons quand même une grande proportion de patients non dirigés en spécialité pour une évaluation et une prise en charge.
Bien que notre étude comporte les limites connues des études rétrospectives (p. ex. : absence de groupe témoin, données manquantes ou incomplètes au dossier, interprétation de la situation clinique, etc.), les résultats aident à cibler les éléments de la prise en charge de l’anaphylaxie à améliorer en centre hospitalier. Dans l’étude de Manivannan, il y avait des groupes de comparaison avant et après la mise en œuvre du formulaire18. Cette dernière étude, en 2014, souligne un déficit de traitement par l’épinéphrine chez les patients vus à l’urgence pour des anaphylaxies causés par des aliments (19 %) ou des venins d’insecte (13 %). De même, très peu de patients ont reçu une ordonnance d’épinéphrine auto-injectable et ont été orientés en allergologie à leur congé de l’hôpital. Pour optimiser le diagnostic d’anaphylaxie et son traitement à l’urgence de leur établissement, les auteurs de cette étude ont mis au point un formulaire de prise en charge qui inclut entre autres une aide au diagnostic et un algorithme pharmaceutique. Cet outil a été utilisé avec 57,2 % des patients (88/154). Le formulaire a amélioré de façon significative le taux d’administration d’épinéphrine après la mise en œuvre des mesures (de 33 % à 51 %), mais pas la prescription d’un auto-injecteur d’épinéphrine au retour à la maison (54 % contre 62 %) ni l’orientation en allergologie (44 % contre 42 %)18.
Les résultats de notre étude ont été présentés aux pharmaciens, urgentologues et immuno-allergologues du CHU de Québec-UL. L’ensemble de ces intervenants ont été sollicités afin de retravailler une nouvelle version de l’ordonnance pharmaceutique individuelle standardisée conforme aux lignes directrices de 2020 et qui répondrait mieux aux besoins des cliniciens afin d’en favoriser l’utilisation. La version de 2024 issue de nos travaux se trouve dans la figure 2 en annexe. Nous avons principalement réorganisé l’ordre des traitements suggérés afin de prioriser l’épinéphrine par voie intramusculaire comme traitement initial et de garder la voie intraveineuse en dernière intention, même après le glucagon chez les patients prenant un bêtabloquant et présentant une réaction anaphylactique réfractaire. Nous avons précisé la dose d’épinéphrine par voie intramusculaire à privilégier selon le poids des usagers. Pour ce qui est des traitements de soutien, nous en avons aussi précisé les indications et avons insisté pour qu’ils ne retardent en aucun cas l’administration d’épinéphrine. Les bronchodilatateurs et l’épinéphrine en nébulisation ont été ajoutés. La diphénhydramine a été conservée malgré ses effets sédatifs et hypotenseurs, car aucun antagoniste des récepteurs H1 de l’histamine de seconde génération par voie parentérale n’est présentement offert au Canada. La ranitidine a été retirée étant donné le manque de données soutenant l’usage des antagonistes des récepteurs H2 de l’histamine pour cette indication. Enfin, un algorithme d’aide au diagnostic pour les médecins a été créé et mis au verso de l’ordonnance standardisée. Avant son déploiement, l’outil a été révisé par les immuno-allergologues du milieu.
L’évaluation de la qualité des actes professionnels exige non seulement un portrait détaillé des situations problématiques, mais aussi un suivi des correctifs nécessaires. À la suite de nos constatations, différentes actions ont été mises en œuvre. D’abord, nous avons diffusé les résultats de l’étude à nos groupes d’experts les plus consultés et exposés à cette situation, c’est-à-dire les immuno-allergologues, les urgentologues et les pharmaciens du CHU de Québec–UL afin d’obtenir un consensus sur les lignes directrices à mettre en place. Ensuite, l’ordonnance pharmaceutique individuelle standardisée de 2024 comprenant un algorithme d’aide au diagnostic au verso a été déployée en mars 2024. La présente étude ne permettait pas d’évaluer les raisons pour lesquelles les prescripteurs n’utilisaient pas l’outil, mais plusieurs hypothèses ont été émises, comme sa méconnaissance ou le sentiment de ne pas en avoir besoin dans cette situation. Néanmoins, pour certaines situations critiques, protocoliser les interventions assure une meilleure prise en charge des patients. L’étude de Manivannan l’a montré dans le contexte de l’anaphylaxie18,24. Une ordonnance pharmaceutique individuelle standardisée est un moyen parmi plusieurs autres de favoriser l’atteinte de cet objectif, à condition qu’elle soit utilisée. Ensuite, l’étiquetage des fioles d’épinéphrine dans les coffrets d’urgence est une mesure ayant été maintenue. L’étude a aussi mené à la révision de la prise en charge dans des secteurs cliniques additionnels, comme en oncologie. Un nouveau bulletin d’information a été transmis aux cliniciens de tous les départements, et un plan amélioré de communication avec les intervenants de première ligne est programmé dans le but de faire connaître l’outil et d’en accroître l’emploi. De plus, le dossier de l’anaphylaxie a été choisi par l’établissement dans le cadre de la campagne canadienne «Choisir avec soin», soulignant l’importance de notre démarche. Enfin, nous pensons que la formation des étudiants en sciences de la santé pourrait être revue afin de les rendre plus à l’aise avec la prise en charge de ce problème aigu. Nous croyons aussi qu’il faudrait poursuivre l’enseignement aux cliniciens afin de répéter les messages clés et d’informer ces derniers des avancées sur ce sujet.
Cet article comporte une annexe. Elle est disponible sur le site de Pharmactuel ( www.pharmactuel.com).
Les auteurs n’ont déclaré aucun financement lié au présent article.
Tous les auteurs ont soumis le formulaire de l’ICMJE sur la divulgation de conflits d’intérêts potentiels et aucun n’a déclaré de conflit d’intérêts lié à cet article.
Nous remercions Mme Nicole Déry, pharmacienne au CHU de Québec–Université Laval, pour son soutien dans la mise en œuvre du plan d’action découlant de la présente étude et visant des pratiques exemplaires dans la prise en charge médicamenteuse de l’anaphylaxie. Cette personne a donné son autorisation écrite.
1. Cardona VJ, Ansotegui I, Ebiwasa M, El-Gamal Y, Fernandez Rivas M, Fineman S et al. World Allergy organization anaphylaxis guidance 2020. World Allergy Organ J 2020;13:100472.
Crossref PubMed
2. Dreskin SC, Stitt JM. Anaphylaxis. Dans : Burks AW, Holgate ST, O’Hehir RE, Broide DH, Bacharier LB, Khurana Hershey GK et al., rédacteurs. Middleton’s allergy principles and practice. 9e éd. Amsterdam : Elsevier; 2020. p. 1228–46.
3. Turner PJ, Worm M, Ansotegui IJ, El-Gamal Y, Rivas MF, Fineman S et al. Time to revisit the definition and clinical criteria for anaphylaxis? World Allergy Organ J 2019;12:100066.
Crossref PubMed
4. Fischer D, Vander Leek TK, Ellis AK, Kim H. Anaphylaxis. Allergy Asthma Clin Immunol 2018;14(suppl. 2):54.
Crossref PubMed
5. Turner PJ, Jerschow E, Umasunthar T, Lin R, Campbell DE, Boyle RJ. Fatal anaphylaxis: mortality rate and risk factors. J Allergy Clin Immunol Pract 2017;5:1169–78.
Crossref PubMed
6. Tanno LK, Bierrenbach AL, Simons FER, Cardona V, Thong BYH, Molinari N et al. Critical view of anaphylaxis epidemiology: open questions and new perspectives. Allergy Asthma Clin Immunol 2018;14:1–11.
Crossref
7. Lockey RF, Benedict LM, Turkeltaub PC, Bukantz SC. Fatalities from immunotherapy and skin testing. J Allergy Clin Immunol 1987;79:660–77.
Crossref PubMed
8. Bock SA, Munoz-Furlong A, Sampson HA. Fatalities due to anaphylactic reaction to foods. J Allergy Clin Immunol 2001;107:191–3.
Crossref PubMed
9. Pumphrey RS. Lessons from management of anaphylaxis from a study of fatal reactions. Clin Exp Allergy 2000;30:1144–50.
Crossref PubMed
10. Wüthrich B. Lethal or life-threatening allergic reactions to food. J Investig Allergol Clin Immunol 2000;10:59–65.
PubMed
11. Campbell RL, Bellolio MF, Knutson BD, Bellamkonda VR, Fedko MG, Nestler DM et al. Epinephrine in anaphylaxis: higher risk of cardiovascular complications and overdose after administration of intravenous bolus epinephrine compared with intramuscular epinephrine. J Allergy Clin Immunol Pract 2015;3:76–80.
Crossref PubMed
12. Lieberman P, Simons FE. Anaphylaxis and cardiovascular disease: therapeutic dilemmas. Clin Exp Allergy 2015;45:1288–95.
Crossref PubMed
13. Simons FE, Gu X, Simons KJ. Epinephrine absorption in adults: intramuscular versus subcutaneous injection. J Allergy Clin Immunol 2001; 108:871–3.
Crossref PubMed
14. Sheikh A, Broek VT, Brown SGA, Simons FER. H1-anti-histamines for the treatment of anaphylaxis: Cochrane systematic review. Allergy 2007;62:830–7
Crossref PubMed
15. Choo KJL, Simons E, Sheikh A. Glucocorticoids for the treatment of anaphylaxis: Cochrane systematic review. Allergy 2010;65:1205–11.
Crossref PubMed
16. Clark S, Camargo CA Jr. Emergency management of food allergy: systems perspective. Curr Opin Allergy Clin Immunol 2005;5:293–8.
Crossref PubMed
17. Kastner M, Harada L, Waserman S. Gaps in anaphylaxis management at the level of physicians, patients, and the community: a systematic review of the literature. Allergy 2010;65:435–44.
Crossref
18. Manivannan V, Hess EP, Bellamkonda VR, Nestler DM, Bellolio MF, Hagan JB et al. A multifaceted intervention for patients with anaphylaxis increases epinephrine use in adult emergency department. J Allergy Clin Immunol Pract 2014;2:294–9
Crossref PubMed
19. Fleiss J L, Levin B, Paik MC. Statistical methods for rates and proportions. 3e éd. New York : John Wiley & Sons; 800 p.
20. Newcombe, RG. Two-sided confidence intervals for the single proportion: comparison of seven methods. Stat Med, 1998;17:857–72.
Crossref PubMed
21. Krugman SD, Chiaramonte DR, Matsui E. Diagnosis and management of food-induced anaphylaxis: a national survey of pediatricians. Pediatrics 2006;118:e554–60.
Crossref PubMed
22. Ruiz Oropeza A, Lassen A, Halken S, Bindslev-Jensen C, Mortz CG. Anaphylaxis in an emergency care setting: a one-year prospective study in children and adults. Scand J Trauma Resusc Emerg Med 2017;25:111.
Crossref
23. Ehrhard S, Gautschi D, Eyb V, Schauber SK, Ricklin ME, Klukowska-Rötzler J et al. Use of epinephrine in anaphylaxis: a retrospective cohort study at a Swiss university emergency department. Swiss Med Wkly 2023;153:40065.
Crossref PubMed
24. Sevransky JE, Agarwal A, Jabaley CS, Rochwerg B. Standardized care is better than individualized care for the majority of critically ill patients. Crit Care Med 2021;49;151–5.
Crossref
Pour toute correspondance : Marianne Girard, 350, boulevard Taché Ouest, Montmagny (Québec) G5V 3R8, CANADA; Téléphone : 418-248-0630; courriel : marianne.girard.cisssca@ssss.gouv.qc.ca
PHARMACTUEL, Vol. 58, No. 2, 2025