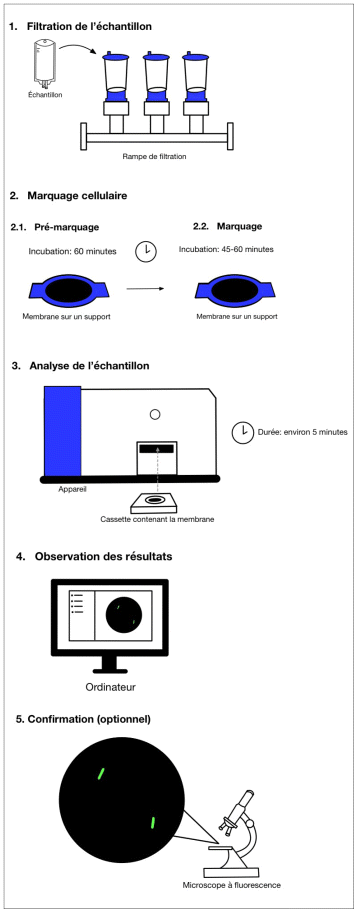
Figure 1 Manipulations nécessaires au déroulement de l’analyse par le ScanRDIMD (schéma fruit d’un montage par l’auteure principale de l’article)
Tatiana Cheng1, Pharm.D., Thomas Sullivan2, B.Sc., Pharm.D., Jean-Marc Forest3, B.Pharm., DPH, M.Sc.
1Candidate au Pharm.D. au moment de la rédaction, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
2Pharmacien, Centre intégré universitaire de santé et de services sociaux du Centre-Ouest-de-l’Île-de-Montréal, Hôpital général juif, Montréal (Québec) Canada;
3Pharmacien, secteur fabrication, Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada
Reçu le 10 août 2024; Accepté après révision le 17 février 2025
DOI: https://doi.org/10.63209/2025.1566
Résumé
Objectif: Cet article vise à explorer les méthodes de rechange au test de stérilité standard effectué par les départements de pharmacie des centres hospitaliers québécois à des fins de contrôle microbiologique pour les préparations stériles. Dans ces centres, c’est présentement la norme USP <71> qui est privilégiée pour les tests de stérilité. Les contrôles microbiologiques actuels, quant à eux, suivent la méthode classique décrite dans les pharmacopées internationales. Les échantillons sont filtrés à travers une membrane qui est ensuite incubée pendant 14 jours, ce qui représente un délai non négligeable. L’échantillon est validé par évaluation visuelle de la turbidité dans un premier temps.
Description de la problématique: Bien que l’utilisation de méthodes rapides de microbiologie semble implantée depuis plusieurs années dans le secteur privé, principalement dans l’industrie, peu de données sont disponibles sur le sujet. Parmi les différentes technologies existantes, on retrouve un système de cytométrie en phase solide permettant la détection de la contamination microbienne en quelques heures à peine.
Résolution de la problématique: Une revue de la littérature a été réalisée dans le but de trouver des méthodes de rechange au test de stérilité standard utilisé dans différents milieux, notamment en établissement hospitalier. Idéalement, ces méthodes permettraient d’obtenir des résultats plus rapidement.
Conclusion: La mise en place d’un test de stérilité rapide de façon systématique dans les établissements hospitaliers est difficilement envisageable à court terme en raison de divers obstacles. L’avenir de cette méthode s’annonce cependant prometteur.
Mots clés: cytométrie en phase solide, méthode microbiologique de rechange, méthode rapide de microbiologie, préparations magistrales, préparations stériles, test de stérilité rapide
Objective: This article aims to explore alternative methods to the standard sterility test performed by pharmacy departments in Quebec hospital centres for microbiological control of sterile preparations. In these centres, the USP <71> standard is currently preferred for sterility tests. Current microbiological controls follow the classical method described in international pharmacopoeias. Samples are filtered through a membrane, which is then incubated for 14 days, representing a significant delay. The sample is initially validated by visual evaluation of turbidity.
Description of the problem: Although the use of rapid microbiology methods seems to have been implemented for several years in the private sector, mainly in industry, little data is available on the subject. Among the existing technologies, there is a solid-phase cytometry system allowing microbial contamination detection in just a few hours.
Resolution of the problem: A literature review was conducted to find alternative methods to the standard sterility test used in various settings, particularly in hospital settings. Ideally, these methods would provide faster results.
Conclusion: The systematic implementation of rapid sterility testing in hospital settings is difficult to consider in the short term due to various obstacles. However, the future of this method looks promising.
Keywords: solid-phase cytometry, alternative microbiological method, rapid microbiology method, compounded preparations, sterile preparations, rapid sterility test
La préparation des produits stériles en milieu hospitalier est de plus en plus centralisée dans les départements de pharmacie pour diverses raisons, notamment la complexité des techniques, la logistique des produits à servir et la nécessité d’améliorer la sécurité des patients. Les antibiotiques, les opioïdes et les solutions de nutrition parentérales figurent parmi les produits dont la préparation est la plus centralisée1. Contrairement aux médicaments fabriqués par l’industrie pharmaceutique, les préparations stériles créées en pharmacie sont soumises à des dates limites d’utilisation (DLU) plus restreintes. Cette restriction est attribuable à leur stabilité souvent plus courtes et souvent normatives plutôt qu’expérimentale, et aux différents contrôles moins rigoureux qui les encadrent. On définit la stabilité d’une préparation comme «la longueur de temps durant laquelle une préparation stérile bien préparée conserve, dans des limites spécifiées et tout au long de la période d’entreposage et d’utilisation, les mêmes propriétés et caractéristiques qu’elle possédait au moment de sa préparation»2. Cet énoncé englobe tout l’aspect microbiologique à vérifier lot par lot. Dans un contexte aseptique, la préparation doit être exempte de micro-organismes, d’où la notion de stérilité. Pour s’en assurer, on effectue un test de stérilité, c’est-à-dire un essai visant à confirmer l’absence de cellules microbiennes viables dans un produit. Puisqu’il n’est pas possible de tester l’ensemble des préparations, seule une partie d’un lot le sera. On estime que le risque de contamination microbiologique des préparations stériles en pharmacie pourrait aller jusqu’à 0,5 %3. Puisqu’il n’est pas possible de garantir l’absence de contamination pour chaque préparation, cette détermination de la stérilité des produits demeure un défi.
Les départements de pharmacie des milieux hospitaliers du Québec sont assujettis aux normes de l’Ordre des pharmaciens du Québec (OPQ). Conformément à la norme 2014.01, un test de stérilité doit être effectué pour les produits stériles à risque élevé, soit ceux préparés notamment à partir d’ingrédients non stériles et où la formulation doit être filtrée pour sa stérilisation. C’est aussi le cas s’il y a plus de 25 unités préparées et dont la date limite d’utilisation souhaitée dépasse celle que recommande la norme2. La norme québécoise ne précise pas le type d’essai microbiologique à réaliser, mais réfère plutôt au chapitre <797> de la Pharmacopée américaine (United States Pharmacopeia ou USP). Ce dernier mentionne que les tests de stérilité doivent respecter les paramètres établis par la méthode décrite dans la norme USP <71>, sinon il faut opter pour une autre méthode non inférieure à celle de la pharmacopée4,5.
La méthode standard a été initialement décrite dans la pharmacopée britannique en 1932. Outre quelques modifications de certains paramètres, le procédé est resté le même depuis6,7. Pour ce faire, l’échantillon est d’abord filtré à travers une membrane dont les pores retiennent les micro-organismes, puis cette membrane est inoculée dans deux milieux nutritifs : le thioglycollate pour les bactéries anaérobies et l’hydrolysat de caséine-soja pour les mycètes et les bactéries aérobies. Les milieux de culture sont ensuite incubés à une certaine température pendant 14 jours. La présence d’une contamination microbienne est déterminée par examen visuel, plus précisément par changement de turbidité. Un échantillon trouble indique une croissance microbienne et donc une contamination. Cette méthode est de plus en plus remise en question en raison du long délai requis de 14 jours pour l’obtention des résultats et de l’évaluation visuelle pour sa lecture6–9. Ce délai représente à lui seul une embûche majeure, car il retarde considérablement l’utilisation des produits stériles.
Ainsi, depuis une vingtaine d’années, le développement et la mise en œuvre de méthodes rapides de microbiologie ont connu un certain essor. Déjà répandues dans l’industrie agroalimentaire et cosmétique, ces technologies ont l’avantage d’offrir un résultat en quelques heures à quelques jours, grâce notamment à l’automatisation6–10. Ces technologies se caractérisent par trois types d’essais : qualitatif, quantitatif et d’identification. Les essais qualitatifs évaluent la présence ou l’absence de micro-organismes alors que les essais quantitatifs permettent de dénombrer le nombre de contaminants, voire d’identifier des micro-organismes. On les classifie également selon trois méthodes de détection : méthode fondée sur la croissance, mesure directe et analyse de composantes cellulaires. Les techniques basées sur la croissance détectent la présence de produits métaboliques, comme le monoxyde de carbone (CO2). La mesure directe permet de visualiser directement les micro-organismes, généralement par coloration. L’analyse de composantes cellulaires repose, pour sa part, sur la détection d’un élément spécifique de la cellule, comme les acides nucléiques ou les acides gras.
Bien que l’utilisation de méthodes rapides de microbiologie semble implantée dans le secteur privé tel l’industrie dans son ensemble, et ce, depuis plusieurs années, peu de données sont disponibles dans la littérature. Parmi les différentes technologies existantes se retrouve un système de cytométrie en phase solide permettant la détection de la contamination microbienne en quelques heures à peine.
Une revue de la littérature a initialement été effectuée dans le but de repérer les méthodes de rechange utilisées dans différents milieux, notamment en établissements hospitaliers, dans les pharmacies préparatrices et dans l’industrie pharmaceutique. L’analyse bibliographique a permis d’en trouver quelques-unes pouvant potentiellement être adoptées en milieu hospitalier et qui ont ensuite été évaluées. Le système ScanRDIMD a été retenu pour vérifier la faisabilité de sa mise en œuvre en milieu hospitalier11. Un des avantages principalement recherchés était la diminution du délai d’obtention des résultats. Cet avantage fait partie des raisons justifiant le choix de ce système, qui seront abordées plus en détail dans la discussion.
Le système ScanRDIMD détecte directement la présence ou l’absence de micro-organismes. L’utilisation de la cytométrie en phase solide permet de déceler la présence d’aussi peu qu’une seule cellule microbienne en quelques heures à peine. Toutefois, le produit à tester doit être filtrable pour être compatible avec la méthode de préparation de l’échantillon. Le système comprend un ordinateur, un appareil d’analyse (cytomètre) et un microscope à fluorescence12.
Le processus global d’analyse peut être divisé en quatre étapes principales : la filtration, le marquage, l’analyse et l’observation des résultats. Dans certains cas, une étape de confirmation est requise. La figure 1 schématise les étapes de manipulation nécessaires à l’analyse de l’échantillon. Il est à noter qu’il n’existe pas de protocole universel, car certains paramètres varient selon la solution stérile à tester. De plus, l’opérateur doit avoir été préalablement formé par la compagnie afin de bien utiliser l’appareil.
La première étape consiste à filtrer l’échantillon sur une membrane noire en polyester (non fibreuse) mesurant 25 mm de diamètre. Les pores de 0,4 μm permettent de retenir les bactéries, moisissures et levures. Cette étape se fait en milieu aseptique, soit sous flux laminaire ISO 5. La rampe de filtration peut porter jusqu’à six échantillons simultanément.
L’étape de marquage se divise en deux sous-étapes : le prémarquage et le marquage. La membrane est d’abord imbibée d’une solution de prémarquage et incubée pendant 60 minutes. Cette étape permet d’activer le métabolisme des cellules dormantes et de provoquer la germination des spores. Ensuite, la membrane est imprégnée d’une solution de marquage appelée ChemChrome V6, puis incubée une seconde fois pendant de 45 à 60 minutes. Le fluorophore pénètre d’abord dans les cellules par transport actif, puis est métabolisé par les enzymes intracellulaires, les estérases. Une fois clivée, l’entité fluorescente est libérée dans le cytoplasme et retenue par la membrane cellulaire intacte. Le colorant fluorescent s’accumule alors dans la cellule et pourra ainsi être détecté13.
| � |
| � |
|
Figure 1 Manipulations nécessaires au déroulement de l’analyse par le ScanRDIMD (schéma fruit d’un montage par l’auteure principale de l’article) | ||
Le filtre est ensuite placé, pour lecture, dans le cytomètre ScanRDIMD. L’analyse, d’une durée d’environ cinq minutes, se fait par excitation à partir d’un laser à l’argon à 488 nm et par balayage automatique. Si le rayon émis entre en contact avec le fluorophore, les détecteurs seront en mesure de capter le signal fluorescent à 515 nm.
Une fois l’analyse terminée, le logiciel comptabilise tous les événements fluorescents détectés. Les résultats sont affichés à l’ordinateur par ce logiciel qui identifie les positifs sous forme de points sur une carte représentant la membrane. L’opérateur visualise en temps réel les micro-organismes marqués sur un microscope à fluorescence afin de confirmer les résultats. Le microscope automatisé permet à l’opérateur de localiser chaque événement fluorescent sans avoir à chercher manuellement.
Lors de la revue de littérature initiale, trois méthodes de rechange ont été prises en considération afin de vérifier l’absence de croissance microbienne dans un échantillon stérile. Celle qui semblait avoir le plus d’applications dans les départements de pharmacie en milieu hospitalier est le BacT/AlertMD de bioMérieux14–16. Cette méthode automatisée détecte la production de CO2 par colorimétrie. Elle repose sur la croissance microbienne. Les résultats sont obtenus après sept à dix jours selon le micro-organisme et les conditions de croissance. La validation de la méthode serait plus complexe et, si on tient compte du délai comparable à celui de la méthode standard de 14 jours, l’option n’a pas été explorée davantage.
L’utilisation d’une trousse de test de détection par amplification des acides nucléiques a également été considérée17. La technique de PCR (réaction en chaîne de polymérase) détecte les fragments spécifiques d’ADN. Toutefois, la méthode semblait moins pertinente pour les préparations magistrales stériles. Cette technique est très spécifique (reconnaissance de fragments d’ADN propres à l’organisme ou aux organismes recherchés) et ne détecte pas tous les micro-organismes présents. En outre, elle ne permet pas de différencier le matériel génétique provenant d’organismes vivants de celui provenant d’organismes morts.
Pour ce qui est de la méthode du ScanRDIMD, méthode retenue pour cet article, la revue de littérature n’a pas permis de relever son utilisation systématique dans le milieu hospitalier. Elle est toutefois largement employée dans l’industrie pharmaceutique18–21. Les applications possibles sont notamment le contrôle environnemental de l’eau, les solutions salines injectables et les produits ophtalmiques. De plus, le système est utilisé à grande échelle aux États-Unis depuis plus d’une dizaine d’années pour les tests de stérilité de centaines de pharmacies préparatrices22. Le peu de littérature pourrait s’expliquer par le fait qu’il est principalement employé dans le secteur privé où les données ne sont pas nécessairement publiées ou sont même volontairement gardées confidentielles.
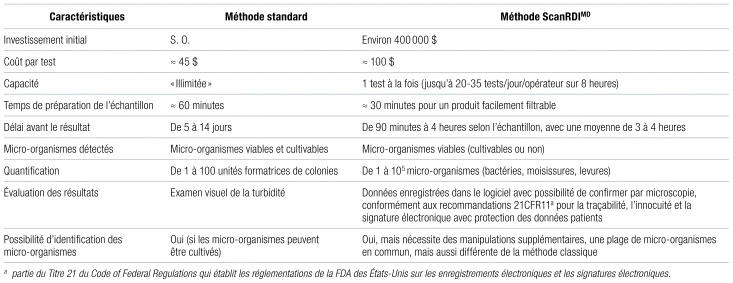
Le tableau I compare différents paramètres de la méthode standard, soit les géloses incubées durant 14 jours, à celle du ScanRDIMD. La sensibilité du système et la rapidité du processus sont les principaux avantages associés à la technologie. Puisque la méthode standard est dépendante de la croissance, la détection repose sur le caractère viable et cultivable du micro-organisme, qu’on appelle unité formatrice de colonie (UFC). Or, certains micro-organismes peuvent échapper à la détection en raison d’un état de stress, d’affaiblissement ou à une incapacité à croître selon les paramètres de la pharmacopée18,20. L’analyse directe par ScanRDIMD détecte tous les micro-organismes viables (cultivables ou non), y compris les spores. De plus, l’utilisation du ChemChrome V6 comme marqueur cellulaire a révélé une supériorité pour détecter la viabilité cellulaire13. Par ailleurs, l’obtention d’un résultat en quelques heures permettrait un meilleur suivi des stocks, en plus d’améliorer la gestion et la sécurité du circuit du médicament. L’aménagement d’un espace d’entreposage pour les médicaments en quarantaine pourrait être réduit, voire éliminé. De façon plus importante, le court délai entraîne une meilleure réactivité en cas de contamination en permettant la mise en place des mesures correctives plus rapidement, et en améliorant la planification et la mise en place de mesures préventives. Il peut aussi être pertinent d’identifier le germe en question afin de mieux cibler les interventions. Toutefois, contrairement à la méthode standard où l’identification est simplifiée, la méthode ScanRDIMD nécessite des manipulations supplémentaires23. L’observation au microscope peut aussi indiquer la morphologie du germe.
L’instauration d’un tel système nécessite une importante mobilisation des ressources financières et humaines. Il faut d’abord compter l’investissement initial pour l’équipement et la formation. Il s’agit d’un appareil de test de stérilité rapide dispendieux24. Le coût d’analyse est aussi plus élevé, mais peut se justifier par le résultat obtenu en quelques heures. Il faut également considérer la présence permanente d’au moins un(e) technicien(ne) de laboratoire pour faire fonctionner l’appareil. Quant à la rentabilité, la préparation de produits stériles dans un seul centre hospitalier n’est probablement pas assez importante pour maximiser la capacité de l’appareil. Cependant, un laboratoire central desservant plusieurs milieux pourrait amortir les coûts. Pour ce qui est de la formation du personnel sur le fonctionnement de l’appareil, l’entreprise s’en charge. Bien que les manipulations soient relativement peu complexes, elles exigent tout de même un travail rigoureux afin d’obtenir des résultats valides. Il existe un risque non négligeable d’erreurs de manipulation et de présence d’événements fluorescents pouvant mener à des résultats faussement positifs6,7,20 si le produit testé présente des particules auto fluorescentes. Une confirmation par observation au microscope est nécessaire, et l’opérateur doit être en mesure de distinguer les événements fluorescents par rapports aux micro-organismes marqués. Une préparation contenant des ingrédients fluorescents ne serait donc pas compatible avec cette technologie s’il y a trop d’interférences. L’appareil se vend uniquement avec un microscope qui inclut une caméra à haute définition afin de capturer des images et d’assurer une meilleure traçabilité et de meilleures analyses des échantillons. La présence de manipulations est un point critique, surtout si on considère que les paramètres peuvent varier d’un protocole à l’autre selon le produit à tester. Certaines étapes peuvent nuire davantage à la validité d’un résultat que d’autres, comme avec des produits à haute teneur en lipides pour lesquels des rinçages sont ajoutés au protocole, renforçant ainsi la nécessité d’une formation de l’opérateur.
Tableau I Comparaison de la méthode standard par géloses incubées et du ScanRDIMD
Avant de mettre en place une méthode de détection microbiologique rapide, peu importe l’appareil, il faut effectuer le laborieux processus de validation. Présentement, seul le test de stérilité standard sur 14 jours est officiellement reconnu par la Food and Drug Administration (FDA). Toutefois, les pharmacopées encouragent l’utilisation de méthodes de rechange, tant qu’elles sont validées selon les critères de l’USP <1223>25. La validation de la méthode doit être faite par l’acquéreur de la technologie. Pour ce qui est du ScanRDIMD, le fabricant offre plusieurs outils pour faciliter le processus, notamment un fichier de référence sur les médicaments (Drug Master File) de la FDA et des protocoles de validation types. Comme déjà mentionné précédemment, les méthodes d’analyse peuvent varier selon la famille de molécules et de préparations à tester. Pour chaque classe médicamenteuse, la méthode doit donc être validée.
Selon les différentes pharmacopées, les principaux paramètres à valider pour une méthode qualitative sont : la spécificité, la limite de détection, la reproductibilité et la robustesse11,25. Dans le contexte où une telle technologie serait mise en place dans un centre hospitalier, les critères à valider pourraient changer en fonction de plusieurs facteurs.
La spécificité d’une autre méthode de stérilité qualitative fait référence à son habilité à détecter une gamme de micro-organismes spécifiques qui posent généralement un risque pour le patient ou le produit ou qui sont souvent présents dans l’environnement au moment de la préparation. Les organismes sélectionnés pour les tests sont le plus souvent les six décrits dans la norme USP <71> : Staphylococcus aureus, Bacillus subtilis, Pseudomonas aeruginosa, Clostridium sporogenes, Candida albicans, Aspergillus brasiliensis. Certains vont aussi évaluer deux micro-organismes plus caractéristiques de leur milieu de travail. La méthode de rechange doit être en mesure de détecter chaque espèce à un niveau égal ou supérieur à la méthode standard.
La limite de détection est le plus petit nombre de micro-organismes pouvant être détecté dans un échantillon, sans nécessairement être quantifiée. Elle est généralement obtenue en faisant une série de dilution d’un micro-organisme et en évaluant la capacité de chaque méthode à détecter la présence d’une contamination.
La reproductibilité se rapporte à la capacité d’une méthode à générer des résultats similaires lorsqu’elle est effectuée plusieurs fois dans les mêmes conditions. Elle pourrait être démontrée en utilisant, par exemple, plusieurs aliquotes du même échantillon ou de différents médicaments.
La robustesse d’une méthode qualitative de rechange est sa capacité à ne pas être affectée par des variations environnementales et de fonctionnement. Elle nous donne une indication de la fiabilité de la méthode dans des conditions normales. Dans l’USP <1223>, une distinction est faite entre les termes robustness et ruggedness, tous deux traduits par «robustesse». Dans le premier cas, on évalue la capacité à résister aux variations des paramètres de la méthode (p. ex. : temps d’incubation, volume de réactif). Dans le second cas, on évalue plutôt la capacité à résister aux conditions environnementales ou externes (p. ex. : l’opérateur, l’appareil, le lot d’un réactif). Dans la pharmacopée européenne, seule l’étude de la robustesse est nécessaire et regroupe ces différentes variations. Elle est généralement évaluée par le fabricant, à moins que l’utilisateur modifie un paramètre critique au protocole ou à l’appareillage.
Les méthodes rapides de microbiologie semblent avoir un avantage considérable. Il est estimé que le marché des tests de stérilité rapides en industrie pharmaceutique continuera de croître26. Avec le développement incessant de nouveaux traitements, on remarque parallèlement une demande grandissante pour ces technologies de rechange. Le marché canadien pour ces appareils serait en plein essor et appelé à croître prochainement. À titre comparatif, les compagnies d’analyse américaines peuvent chacune posséder à elles seules plusieurs appareils. Une des raisons qui pourrait expliquer l’expansion du marché est notamment l’émergence des thérapies cellulaires et géniques. D’ailleurs, le chapitre <1071> de l’USP reconnaît le potentiel des méthodes microbiologiques de rechange, particulièrement pour les produits à courte durée de vie27. Plusieurs facteurs laissent croire que les tests de stérilité rapides seront de plus en plus utilisés dans l’avenir.
Malgré le peu de littérature scientifique sur le ScanRDIMD, le système est tout de même utilisé depuis plusieurs années dans le secteur privé. Les centres hospitaliers pourraient également bénéficier des avantages qu’il offre, dont la rapidité des résultats et sa sensibilité accrue. Évidemment, les ressources financières et d’exploitation requises restent des défis difficiles à contourner. Bien que les méthodes de détection microbiologique de rechange soient plus rapides que le test de stérilité standard, cette rapidité n’est pas observable en ce qui concerne leur mise en place.
À la lumière des éléments de cette revue, plusieurs questions demeurent encore en suspens. Pour quelles raisons les tests de stérilité de rechange sont-ils aussi peu utilisés dans les centres hospitaliers? Est-ce que la mise en œuvre de cette technologie pourrait être facilitée si plusieurs centres hospitaliers se regroupaient? À plus grande échelle, est-ce qu’un tel appareil pourrait répondre au besoin d’optimisation des services de biologie médicale des laboratoires OPTILAB? Serait-il plus avantageux de faire appel à une entité externe pour effectuer les tests de stérilité de divers centres hospitaliers, entité qui serait dépositaire de l’appareil? Ces questions sont des plus intéressantes et méritent qu’on s’y attarde. La Pharmacopée américaine laisse croire que, dans les prochaines années, plusieurs méthodes de rechange seront officiellement reconnues, dont la cytométrie en phase solide28. Le potentiel de ces technologies n’est donc pas à négliger, notamment par la diminution draconienne du temps requis pour obtenir les résultats.
Les auteurs n’ont déclaré aucun financement lié au présent article.
Tous les auteurs ont soumis le formulaire de l’ICMJE sur la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts lié au présent article.
Les auteurs tiennent à remercier Monsieur Yves Vallières, directeur du développement des affaires, secteur industrie, chez bioMérieux, pour avoir généreusement transmis des informations et documents essentiels à la compréhension de l’appareil et pour avoir approuvé le schéma des manipulations. Cette personne a donné son autorisation écrite.
1. Painchart L, Palamini M, Odou P, Bussières JF. Profile of centralization practices for preparation of non-hazardous drugs in Quebec hospitals. Pharm Technol Hosp Pharm 2019;4:89–94.
Crossref
2. Ordre des pharmaciens du Québec. Norme 2014.01 – Préparation de produits stériles non dangereux en pharmacie (octobre 2017). [En ligne] https://www.opq.org/wp-content/uploads/2020/03/1827_38_fr-ca_0_norme201401_prod_steriles_non_dang_oct2017.pdf (Site visité le 25 avril 2024).
3. Austin PD, Hand KS, Elia M. Systematic review and meta-analysis of the risk of microbial contamination of parenteral doses prepared under aseptic techniques in clinical and pharmaceutical environments: an update. J Hosp Infect 2015;91:306–18.
Crossref PubMed
4. United States Pharmacopeial Convention (USP). Chapter <797> Pharmaceutical Compounding-Sterile preparations. Dans: USP-NF. Rockville, MD 2021. 35 pages.
5. United States Pharmacopeial Convention (USP). Chapter <71> Sterility tests. Dans: USP-NF. Rockville, MD 2021. 12 pages.
6. Gressett G, Vanhaecke E, Moldenhauer J. Why and how to implement a rapid sterility test. PDA J Pharm Sci Technol 2008;62:429–44.
7. Deutschmann S, Paul M, Claasen-Willemse M, Van Den Berg J, Izjerman-Boon P, Grunert Da Fonseca V et al. Rapid sterility test systems in the pharmaceutical industry: Applying a structured approach to their evaluation, validation and global implementation. PDA J Pharm Sci Technol 2023;77:211–35.
Crossref PubMed
8. Taylor A. Quality control: Rapid sterility testing for compounding pharmacies. Int J Pharm Compd 2020;24:299–303.
PubMed
9. Henriques J, Cardosa C, Vitorino C. Rapid microbiological methods. They are rapid! Are they fast? [en ligne] https://meddocsonline.org/ebooks/ebook-microbiology/rapid-microbiological-methods-they-are-rapid-are-they-fast.pdf (site visité le 25 avril 2024).
10. Pharmacopée européenne. Chapitre 5.1.6 Méthodes alternatives pour le contrôle de la qualité microbiologique. Dans: Ph. Eu. (11e) 2023. 20 pages.
11. bioMérieux. When you need to know now – ScanRDI®. (12 octobre 2023) [en ligne] https://www.youtube.com/watch?v=2aQxvPQ-TlU (site visité le 25 avril 2024).
12. bioMérieux. Validation and successful implementation of ScanRDI®. [En ligne] https://www.biomerieux-industry.com/sites/default/files/2022-03/SCAN%20RDI%20White%20Paper%20-%20Final%20Art.pdf (site visité le 25 avril 2024).
13. Parthuisot N, Catala P, Lemarchand K, Baudart J, Lebaron P. Evaluation of ChemChrome V6 for bacterial viability assessment in waters. J Appl Microbiol 2000;89:370–80.
Crossref PubMed
14. De Jonghe PJ, Dekeyser I, Verhelle K. Implementation of BacT/alert (Biomerieux) culture bottles in a hospital pharmacy production unit for the sterility testing of chemotherapeutic batches. Eur J Hosp Pharm 2017;24(suppl. 1):216.
15. Hiom S, Denyer S, Talbot C, Maillard J-Y, Spark P, Smith J. A preliminary investigation into the ability of three rapid microbiological methods to detect microorganisms in hospital intravenous pharmaceuticals. PDA J Pharm Sci Technol 2013;67:376–86.
Crossref PubMed
16. Le Roy C, Bermudez E, Carre N, Chanat C, Castelain C, Poutet H et al. Validation of the BacT/Alert® method for microbiological control of pediatric parenteral nutrition (PPN) mixtures. GERPAC (8 octobre 2015) [en ligne] https://www.gerpac.eu/validation-of-the-bact-alert-r-method-for-microbiological-control-of-pediatric-parenteral-nutrition-ppn-mixtures (site visité le 25 avril 2024).
17. Sartorius. Microsart® ATMP Sterile Release: Instructions for Use. Prod No. SMB95-1007. Minerva Biolabs GmbH | Berlin | Germany. Material No 100005493, Version 2021–05.
18. Smith R, Von Tress M, Tubb C, Vanhaecke E. Evaluation of the ScanRDI® as a rapid alternative to the pharmacopeial sterility test method: comparison of the limits of detection. PDA J Pharm Sci Technol 2010;64:356–63.
19. Constanzo SP, Borazjani RN, McCormick PJ. Validation of the Scan RDI for routine microbiological analysis of process water. PDA J Pharm Sci Technol 2002;56:206–19.
20. Silva GBL, da Silva CM, de Sá LZCM, Rocha ML, Gil EdeS, Alves VF et al. Solid phase cytometry applied to sterility tests for injecting 0.9% sodium chloride. Afr J Pharm Pharmacol 2015;9:1051–61.
Crossref
21. Eagle Analytical Services, Inc. ScanRDI® system performance data as a sterility test method for pharmacy compounded preparations: A ten-year survey (2019). [En ligne] https://eagleanalytical.com/wp-content/uploads/2019/04/ScanRDI-System-Performance-A-10-Year-Survey.pdf (site visité le 25 avril 2024).
22. bioMérieux. Non-growth based alternative sterility testing-Appropriate response to an out-of-specification sterility test when using the ScanRDI®. [En ligne] https://www.biomerieux.com/corp/en/education/resource-hub/white-papers/pharmaceutical-qc-white-papers/non-growth-based-alternative-sterility-testing-white-paper.html (site visité le 25 avril 2024).
23. Gosselin J, Palazuelo V, Girard V, Monnin V, Saccomani MC, Wittemberg V et al. Easy post-scan growth method provides combination of rapid industry relevant microorganisms quantification and identification with ScanRDI® and VITEK® MS. (octobre 2015) [en ligne] https://www.researchgate.net/profile/Felix-Montero-Julian/publication/306291896_Easy_post-scan_growth_method_provides_combination_of_rapid_industry_relevant_microorganisms_quantification_and_identification_with_ScanRDIR_and_VITEKR_MS/links/57b7204808aedfe0ec937e4a/Easy-post-scan-growth-method-provides-combination-of-rapid-industry-relevant-microorganisms-quantification-and-identification-with-ScanRDIR-and-VITEKR-MS.pdf (visité le 25 avril 2024).
24. Hauschild J, Breugelmans P, Cheung D, Conway D, Saxer S, Quain C et al. Rapid microbial method feasibility study for J&J biologics production process monitoring. Présenté à la 9e édition de la Annual global conference on pharmaceutical microbiology. Bethesda, MD (20–22 octobre 2014).
25. United States Pharmacopeial Convention (USP). Chapter <1223> Validation of alternative microbiological methods. Dans: USP-NF. Rockville, MD 2023. 28 pages.
26. Research and Markets. Pharmaceutical sterility testing market size, share & trends analysis report by type (outsourcing, in-house), by product type, by test type, by sample, by end-use, by region, and segment forecasts, 2024–2030 (février 2024). [En ligne] https://www.researchandmarkets.com/reports/4621734 (site visité le 25 avril 2024).
27. United States Pharmacopeial Convention (USP). Chapter <1071> Rapid microbial tests for release of sterile product: A risk-based approach. Dans: USP-NF. Rockville, MD 2021. 12 pages.
28. Tu H. USP evolving position on use of rapid microbial methods (27 juin 2023). [En ligne] https://www.casss.org/docs/default-source/cgtp/2023-speaker-presentations/tu-huiping-usp-2023.pdf?sfvrsn=d43f184c_6 (site visité le 25 avril 2024).
Pour toute correspondance : Jean-Marc Forest, Centre hospitalier universitaire Sainte-Justine, 3175, chemin de la Côte-Sainte-Catherine, Montréal (Québec) H3T 1C5, CANADA; Téléphone : 514 345-4603; Courriel : jean-marc.forest.hsj@ssss.gouv.qc.ca
PHARMACTUEL, Vol. 58, No. 2, 2025