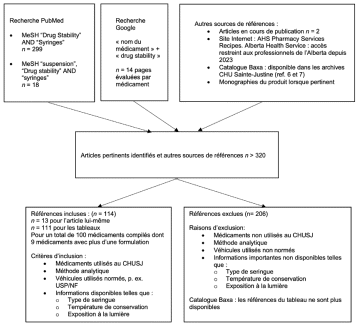
Figure 1 Organigramme pour la recherche d’articles
Wassim Mekideche1, Dominique Lemieux2, B.Pharm., M.Sc., Jean-Marc Forest2, B.Pharm., DPH, M.Sc.
1Candidat au Pharm.D. au moment de la rédaction, Faculté de pharmacie, Université de Montréal, Montréal (Québec) Canada;
2Pharmacien(ne), Centre hospitalier universitaire Sainte-Justine, Montréal (Québec) Canada
Reçu le 14 septembre 2024; accepté après révision le 27 octobre 2025
https://doi.org/10.63209/2026.1569
Résumé
Objectif: L’objectif de cet article est de présenter une revue non exhaustive de la littérature portant sur la stabilité de certains médicaments conservés dans des seringues orales ou intraveineuses utilisés au Centre hospitalier universitaire Sainte-Justine. L’entreposage de médicaments sous forme liquide, qu’ils soient d’origine commerciale ou magistrale, dans des seringues en plastique suscite des interrogations quant à la durée de stabilité et une possible altération de l’efficacité et de l’innocuité du traitement.
Méthodologie: Une mise à jour a été faite et a conduit à la création de tableaux visant à orienter les utilisateurs quant à la période d’entreposage recommandée pour les médicaments reconditionnés en seringues. La revue de la littérature a été réalisée en employant les termes MeSH « Drug Stability » et « Syringe » pour la recherche des articles.
Résultats: Au total, les données d’une centaine de médicaments ont été compilées dans 110 conditions différentes, le tout à partir de plus de 123 références ciblées tant dans PubMed et Google que dans les données du Centre hospitalier Sainte-Justine. Les résultats de cette revue sont synthétisés et présentés sous forme de tableaux, pour un usage pratique par les divers intervenants.
Conclusion: Cette recherche non exhaustive dans la littérature a été effectuée pour produire des tableaux de stabilité de médicaments en seringue. Cet article se présente comme une mise en commun de certaines données sur la stabilité qui ne sont pas toujours facilement accessibles ou qui sont dispersées dans la littérature pharmaceutique.
Mots-clés: magistrale, médicament, seringues, stabilité
ABSTRACT
Objective: The objective of this article is to present a non-exhaustive review of the literature on the stability of certain medications stored in oral or intravenous syringes and used at the Centre hospitalier universitaire Sainte-Justine. The storage of liquid medications, whether commercially available or compounded, in plastic syringes raises questions regarding stability duration and potential alterations in treatment efficacy and safety.
Methodology: An update was performed, leading to the creation of tables designed to guide users on the recommended storage period for medications repackaged in syringes. The literature review was conducted using the MeSH terms “Drug Stability” and “Syringe” to locate relevant articles.
Results: In total, data of approximately one hundred medications were compiled under 110 different conditions, based on more than 123 targeted references from PubMed, Google, and internal data from the Centre hospitalier universitaire Sainte-Justine. The results of this review are summarized and presented in table format for practical use by various collaborators.
Conclusion: This non-exhaustive literature search was carried out to produce stability tables for medications stored in syringes. This article serves as a consolidation of certain stability data that are not always easily accessible or are scattered throughout the pharmaceutical literature.
Keywords: compounding, medication, syringes, stability
This abstract was translated using Microsoft 365 Copilot and subsequently reviewed by the editorial team.
Au Centre hospitalier universitaire (CHU) Sainte-Justine, deux principales lignes de production de reconditionnement en seringue existent, soit un Centre de préparation des médicaments oraux et un Centre de préparation des médicaments intraveineux. Pour un établissement de santé distribuant des unidoses sur une période de 24 heures, il est préférable de viser une stabilité de 48 heures au minimum en seringue, étant donné l’incertitude quant au moment précis du conditionnement en seringue par rapport à celui de l’administration du médicament au patient. Ce délai détermine si les médicaments peuvent maintenir leur stabilité pour assurer leur qualité depuis leur préparation jusqu’à leur distribution et utilisation, soit au moins 24 heures après leur sortie de la pharmacie.
L’utilisation de formulations extemporanées et de reconditionnement peut sembler être une option simple, mais elle comporte des enjeux potentiellement complexes pour le personnel soignant. Avant que l’on puisse servir de telles préparations, plusieurs facteurs doivent être pris en compte, dont la stabilité des médicaments, qui est essentielle pour garantir l’efficacité du traitement sur toute la durée prescrite. Sans stabilité en seringue, ce reconditionnement deviendrait hasardeux et dangereux pour les patients. Il est également crucial de s’assurer de l‘innocuité des médicaments administrés. En particulier, dans un contexte pédiatrique, les préparations commerciales ne conviennent pas toujours. Des études ont démontré que, notamment chez les patients très jeunes, la difficulté à avaler ou la nécessité de petites doses rendent les préparations commerciales, sous toutes leurs formes, souvent inutilisables1.
Un vieil adage dit que les enfants ne sont pas simplement des versions miniatures des adultes. Cela souligne les importantes différences physiologiques, pharmacocinétiques et pharmacodynamiques entre adultes et enfants. Par exemple, des paramètres comme la clairance et le volume de distribution varient en fonction de l’âge. De plus, la manière dont les médicaments sont absorbés, distribués, métabolisés et éliminés est souvent différente chez l’enfant2.
Les différences entre enfants et adultes impliquent que les formulations commerciales ne conviennent pas toujours. Cela souligne l’importance de disposer de préparations adaptées et sûres pour les enfants. Dans ce contexte, l’obtention d’informations sur la stabilité des médicaments en seringue devient cruciale. L’un des buts de cette revue est de réunir un certain nombre de ces données, utiles au CHU Sainte-Justine, qui sont dispersées dans la littérature et, si possible, de rechercher une standardisation des paramètres propres à un médicament. Il est donc primordial de détenir des données fiables afin notamment d’assigner une durée de stabilité adéquate3.
Une revue non exhaustive de la littérature a été réalisée et des tableaux ont été créés à partir des médicaments identifiés en usage au CHU Sainte-Justine, le tout tant pour les médicaments commerciaux, provenant de l’industrie, que pour ceux préparés magistralement sur place par le secteur fabrication du département de pharmacie.
Le but premier était de répondre à la question de stabilité en seringue des médicaments liquides utilisés au CHU Sainte-Justine. L’outil en ligne PubMed a été utilisé afin d’identifier les articles répondant à cette question. La revue de la littérature a été réalisée en employant les mots-clés Drug Stability et Syringe pour la recherche sur PubMed et Google. Ce processus, présenté selon l’approche PRISMA, est décrit à la figure 14.
|
| ||
|
Figure 1 Organigramme pour la recherche d’articles | ||
Enfin, toujours en nous basant sur une liste de médicaments administrés au CHU Sainte-Justine, nous avons effectué une recherche sur Google en utilisant le nom du médicament combiné à l’expression « drug stability ». La recherche s’est limitée arbitrairement aux 14 premiers résultats si trop de données étaient disponibles.
Une fois les articles identifiés, les informations pertinentes étaient recherchées, notamment le nom du médicament et sa concentration, le véhicule utilisé pour l’étude de stabilité (pour les préparations magistrales et intraveineuses), le matériau de fabrication (polypropylène, polyéthylène, polycarbonate, etc.) de la seringue ou de la bouteille du médicament lorsque l’information était disponible, le type de seringues utilisées, soit ambrées ou non et la mention de protégé de la lumière ou non, la température de conditionnement et enfin la standardisation proposée en termes de véhicule, concentration et stabilité.
Il est important de noter que les données de stabilité pour les bouteilles de plastique ont été extrapolées à leur équivalent en seringue en ce qui a trait au matériau. Par exemple, si une référence indiquait qu’un médicament était stable dans une bouteille en polypropylène, cette stabilité a été extrapolée aux seringues en polypropylène. Lorsque possible, seules les formulations « modernes », n’utilisant qu’un véhicule ou deux, ont été retenues, dans la mesure où elles contenaient un agent de conservation. Les plus anciennes formulations, utilisant par exemple des mélanges de méthylcellulose, des sirops de cerise ou des huiles végétales quelconques, et nécessitant souvent des préparations des véhicules eux-mêmes, ont été écartées, à moins qu’elles ne soient les seules options disponibles dans la littérature. De nos jours, les formulations magistrales tendent à utiliser des véhicules commerciaux déjà tout préparés comme les gammes Ora (Ora-Blend, Ora-Sweet, Ora-Plus), Oral (Oral-Mix, Oral-Syrup, Oral-Suspend) ou encore SyrSpend (toute une gamme). À noter également une certaine variabilité d’un article à l’autre pour les valeurs de température pièce ou de réfrigération. Ces variations peuvent s’expliquer par le fait que certaines études étaient antérieures aux normes actuellement en vigueur, notamment la norme OPQ 2021.01, « Préparations magistrales non stériles en pharmacie », et aux définitions plus rigoureuses des termes « réfrigéré » ou « température pièce » quant à leurs valeurs en degrés Celsius, qui varient d’étude en étude5. Les températures sont de toute façon étude dépendantes.
Certains fabricants de seringues, tels Becton-Dickinson, Baxter et Cardinal Health, ont également confirmé que leurs différentes seringues sont constituées de polypropylène, mais n’ont toutefois pas réalisé d’études formelles de stabilité pour des médicaments qui y sont reconditionnés. C’est le cas de la majorité des seringues de la gamme ENFit conçues spécifiquement pour l’administration entérale. Toutefois, les seringues ENFit sont conformes aux normes ISO 20695, ISO 80369 et ISO 7886-1, selon le cas. On s’appuie notamment sur ces normes pour l’utilisation de ce type de seringues pour l’administration entérale. La stabilité des médicaments que l’on y reconditionne est donc primordiale.
Les tableaux de stabilité produits par la défunte compagnie Baxa n’étaient pas accessibles aux fins du présent article, puisque cette compagnie n’existe plus; les études ayant conduit à l’élaboration de ces tableaux semblent avoir été perdues et il est donc impossible de les cautionner ou entériner. Des recherches dans les archives du secteur fabrication du département de pharmacie du CHU Sainte-Justine ont toutefois permis de retracer quelques tableaux de données de stabilité; ceux-ci faisaient originalement partie des catalogues de produits de cette compagnie6,7. Des copies PDF des tableaux sont disponibles sur le site web du CHU Sainte-Justine et il appartient au lecteur de voir si ces informations peuvent lui être utiles malgré tout8.
Toutes ces informations ont été incorporées dans différents tableaux, disponibles en annexe du présent article : un pour les médicaments commerciaux administrés par voie orale (tableau I), un pour les magistrales (tableau II), puis un dernier tableau pour les quelques préparations intraveineuses répertoriées (tableau III). Le tableau IV, pour sa part, répertorie le type de matériel utilisé pour les bouteilles de certains médicaments commerciaux liquides, aidant ainsi à la prise de décision pour la stabilité extrapolée de leur reconditionnement éventuel en seringue de plastique. Au total, plus de 300 articles ont été identifiés et utilisés grâce à cette revue, puis chaque article a été consulté individuellement afin d’en évaluer la pertinence. Tous les articles retenus servent de bibliographie au travail, et leurs coordonnées sont notées dans la colonne de droite de chaque médicament concerné.
La définition de Santé Canada de préparations en pharmacie est la suivante : « La combinaison ou le mélange de deux ingrédients ou plus (dont au moins un ingrédient est une drogue ou une composante pharmacologique active) pour créer un produit final sous forme dosifiée appropriée. Ce procédé peut nécessiter des substances chimiques brutes ou l’altération des caractéristiques physiques ou de la puissance des produits disponibles sur le marché.»9. Également, selon la norme 2014.01 sur les préparations magistrales stériles de l’Ordre des pharmaciens du Québec, les « processus de préparation mis en place permettent d’obtenir des préparations finales de qualité et sécuritaires pour le patient ». De plus cette même norme stipule que « la stabilité est déterminée à partir de la documentation scientifique reconnue »10.
Ces définitions sous-entendent un souci d’exactitude de la dose et que le produit final doit être approprié pour le patient devant le recevoir. Elles demandent aussi des données basées sur de l’information scientifique pour la préparation de ces produits. Enfin, lorsque l’on constate que, selon l’OMS, les erreurs médicamenteuses engendrent à elles seules des coûts annuels de 42 milliards de dollars américains, le souci de fournir une préparation d’un médicament sécuritaire et efficace est primordial11.
Dans un même ordre d’idées, les lignes directrices de l’American Society of Health-System Pharmacists soulignent l’importance de s’assurer que le contenant dans lequel le médicament est conditionné permet de garantir la stabilité de celui-ci12. Cela renforce l’importance de disposer de données de stabilité pour les médicaments que l’on souhaite entreposer dans des seringues en plastique.
À l’heure actuelle, le manque de préparations médicamenteuses adaptées à la clientèle pédiatrique constitue un défi, particulièrement dans le contexte canadien où, selon l’étude de Litalien et coll., un retard face aux États-Unis et à l’Europe a été constaté concernant la disponibilité de médicaments approuvés pour la clientèle pédiatrique13. Par exemple, le lévétiracétam a obtenu l’indication officielle en pédiatrie pour l’épilepsie en 2019 pour le Canada par rapport à 2005 en Europe13. Cette étude souligne également que la préparation et l’entreposage de médicaments sous des formulations spécialisées ou dans des contenants particuliers sont souvent nécessaires pour fournir des soins pharmaceutiques à cette population et doivent faire l’objet d’études en conséquence13.
La revue de la littérature n’a pas permis d’identifier d’étude évaluant les avantages d’une standardisation des protocoles pour parvenir à des concentrations finales de magistrales ou autres solutions et suspensions similaires entre différents centres hospitaliers. L’étude de Rood et coll., une étude transversale menée au Michigan auprès de 240 pharmacies communautaires et hospitalières et portant sur 147 préparations magistrales pour une clientèle pédiatrique, a démontré une grande variabilité dans les pratiques14. Les auteurs ont également conclu que la principale cause est probablement le manque de standardisation d’un milieu à un autre. Il y a une étude en cours portant sur l’analyse et la comparaison des pratiques de préparations dans les pharmacies au Québec, mais ses résultats n’ont pas encore été rendus publics.
De plus, le manque de données de stabilité contribue à une augmentation des coûts dans les secteurs de fabrication des pharmacies hospitalières. Dans une étude menée auprès de 1620 patients, Bucak et coll. ont démontré que, pour la clientèle pédiatrique du département d’urgence d’un hôpital tertiaire, en moyenne 42,5 % d’une dose de médicament doit être jetée en raison de l’indisponibilité de préparations adaptées pour les enfants15. Considérant que la majorité des doses de médicaments se calculent selon le poids de l’enfant et que des formulations pour adultes sont utilisées, cela occasionne du gaspillage puisque le médicament non utilisé doit être jeté, faute de données de stabilité16. Bien que le contexte canadien puisse différer de celui de cette étude menée en Turquie, il est raisonnable de penser que le fait de jeter des quantités non utilisées de médicaments mène à des pertes financières pouvant être importantes. Disposer d’informations sur la conservation des médicaments préparés de manière extemporanée ou dans un autre contenant que celui d’origine permet, d’une part, de les préparer d’avance et, d’autre part, d’avoir accès à des doses adaptées au poids de l’enfant, ce qui évite de recourir à des produits destinés aux adultes et de n’en utiliser qu’une partie.
Cette revue de littérature présente plusieurs limites. Tout d’abord, seuls la base de données PubMed et l’outil de recherche Google ont été utilisés pour identifier les articles pertinents. D’autres outils de recherche, par exemple sur la plateforme Embase, auraient probablement pu fournir des informations supplémentaires. Il faut noter qu’il n’y avait pas d’uniformité dans les méthodes d’évaluation de la stabilité des médicaments, car les études provenaient de divers auteurs. Les méthodes de validation de la stabilité des médicaments variaient aussi d’un article à l’autre. De plus, toutes les informations en provenance de l’ancienne compagnie Baxa ne pouvaient être validées formellement. Les compagnies pharmaceutiques n’ont pas toujours été directement consultées. Enfin, l‘accent a été mis naturellement et principalement sur les médicaments en usage au CHU Sainte-Justine.
Une revue de la littérature a permis d’identifier plusieurs médicaments pour lesquels des données de stabilité, lors de leur entreposage dans des seringues orales ou intraveineuses, étaient disponibles ou extrapolables. Ces données ont été compilées dans différents tableaux, of frantainsi un référentiel consultable par les cliniciens au besoin. Cette ressource peut constituer une réponse à la question de la stabilité de certains médicaments dans des véhicules ou contenants autres que ceux d’origine. Naturellement, les connaissances et les besoins évoluant constamment, des mises à jour seront requises dans l’avenir.
Les auteurs n’ont déclaré aucun financement lié à cet article.
Tous les auteurs ont soumis le formulaire de l’ICMJE pour la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts lié au présent article.
Les auteurs n’ont pas utilisé d’outils d’intelligence artificielle dans le travail soumis.
Les auteurs remercient les assistants techniques en pharmacie du CHU Sainte-Justine qui ont contribué à la réalisation du projet, particulièrement Mme Alexandra Larivière pour son aide dans la compilation des données. Cette personne a donné son autorisation écrite.
1. Richey RH, Hughes C, Craig JV, Shah UU, Ford JL, Barker CE et al. A systematic review of the use of dosage form manipulation to obtain required doses to inform use of manipulation in paediatric practice. Int J Pharm 2017;518: 155–66.
Crossref PubMed
2. Fernandez E, Perez R, Hernandez A, Tejada P, Arteta M, Ramos JT. Factors and mechanisms for pharmacokinetic differences between pediatric population and adults. Pharmaceutics 2011;3:53–72.
Crossref PubMed
3. Vigneron J. Stability studies: a scientific mission of the hospital pharmacist. Pharm Technol Hosp Pharm 2017;2:143–4.
4. Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ 2021;372:n71
Crossref PubMed
5. Ordre des pharmaciens du Québec. Norme 2012.01 – Préparations magistrales non stériles en pharmacie 2012. [en ligne] https://www.opq.org/documentation/norme-2012-01-preparation-magistrales-non-steriles-en-pharmacie/ (site visité le 27 décembre 2023).
6. Catalog of products. Baxa Corporation, Englewood, Colorado, USA. 1989; 20.1-20.7.
7. Innovative drug delivery systems. Baxa Corporation, Englewood, Colorado, USA. 1997: 74–6.
8. CHU sainte-Justine. Stabilité de formulations en seringues orales (6 mai 2021) [en ligne] https://www.chusj.org/fr/soins-services/P/Pharmacie/Outils/Formulations-magistrales/Outils-pratiques/Stabilite-des-formulations-en-seringues-orales (site visité le 11 février 2026).
9. Santé Canada. Politique sur la fabrication et la préparation en pharmacie de produits pharmaceutiques au Canada (26 janvier 2009). [en ligne] https://www.canada.ca/fr/sante-canada/services/medicaments-produits-sante/conformite-application-loi/bonnes-pratiques-fabrication/documents-orientation/politique-fabrication-preparation-pharmacie-pharmaceutiques.html (site visité le 27 décembre 2023).
10. Ordre des pharmaciens du Québec. Norme 2014.01 - Préparation de produits stériles non dangereux en pharmacie (2 avril 2014). [en ligne] https://www.opq.org/wp-content/uploads/2020/03/1827_38_fr-ca_0_norme201401_prod_steriles_non_dang_oct2017.pdf (site visité le 27 décembre 2023).
11. Organisation Mondiale de la Santé. Les médicaments sans les méfaits (2017). [en ligne] https://iris.who.int/bitstream/handle/10665/279498/WHO-HIS-SDS-2017.6-fre.pdf (site visité le 27 décembre 2023).
12. American Society of Health-System Pharmacists. ASHP guidelines on compounding sterile preparations. Am J Health Syst Pharm 2014;71:145–66.
Crossref PubMed
13. Litalien C, Autmizguine J, Carli A, Giroux D, Lebel D, Leclerc JM, et al. Providing suitable pediatric formulations for Canadian children: a call for action. Can J Hosp Pharm 2020;73:247–56.
Crossref PubMed
14. Rood JM, Engels MJ, Ciarkowski SL, Wagenknecht LD, Dickinson CJ, Stevenson JG. Variability in compounding of oral liquids for pediatric patients: a patient safety concern. J Am Pharm Assoc 2014;54:383–9.
Crossref
15. Bucak IH, Almis H, Dogan CN, Turgut M. The status of drug wastage in the pediatric emergency department of a tertiary hospital. Avicenna J Med 2020;10:10–4.
Crossref PubMed
16. Taketomo CK, Hodding JH, Kraus DM. Pediatric and neonatal dosage handbook. 26e éd. Wolters Kluwer: Lexi-Comp.; 2019–2020. 2406 p.
Pour toute correspondance : Jean-Marc Forest, Centre hospitalier universitaire Sainte-Justine, 3175, chemin de la Côte-Sainte-Catherine, Montréal (Québec) H3T 1C5, CANADA; téléphone : 514 345-4603; courriel : jean-marc.forest.hsj@ssss.gouv.qc.ca
PHARMACTUEL, Vol. 59, No. 1, 2026