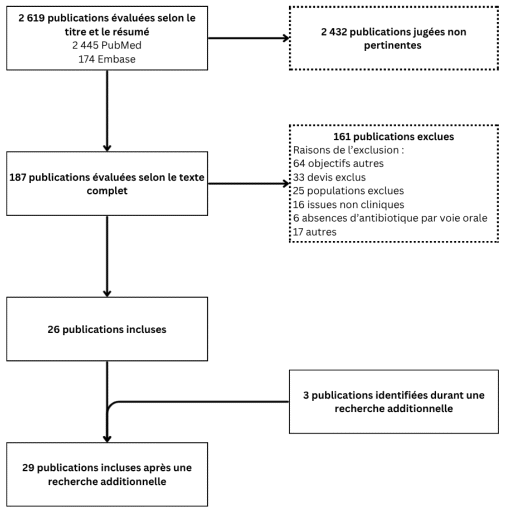
Figure 1 Diagramme de flux de la revue de la littérature
Mikhail-Paul Cardinal1*, Pharm.D., M.Sc., Amélie Allaire1*, B.Sc.inf., Pharm.D., Rachel Verret1*, Pharm.D., Marie-Kim Lacoste1*, Pharm.D., Michel Savoie2, B.Pharm., M.Sc., Jean-François Tessier2, B.Pharm., M.Sc.
1Candidat(e) au Pharm.D. au moment de la rédaction, Faculté de pharmacie, Université de Montréal, Montréal, Canada;
2Pharmacien, Centre intégré universitaire de l’Est-de-l’Île-de-Montréal, Hôpital Maisonneuve-Rosemont, Montréal, Canada
*Mikhail-Paul Cardinal, Amélie Allaire, Rachel Verret et Marie-Kim Lacoste ont contribué de façon équivalente à la rédaction de cet article.
Reçu le 7 novembre 2024; Accepté après révision par les pairs le 26 juin 2025
https://doi.org/10.63209/2025.1571
Résumé
Objectif: Les ostéomyélites et les infections de prothèse chez les adultes ont historiquement été traitées par des antibiotiques administrés par voie intraveineuse. Selon des données récentes, le traitement antibiotique administré par voie orale serait non inférieur à celui par voie intraveineuse, mais il existe peu de données probantes sur l’efficacité des molécules spécifiques. C’est pourquoi une revue de la littérature sur l’efficacité des antibiotiques par voie orale habituellement utilisés contre ces infections a été menée.
Sources des données et sélection des études: Une revue de la littérature sur l’efficacité de plusieurs antibiotiques administrés par voie orale (fluoroquinolones, rifampicine, triméthoprime-sulfaméthoxazole, linézolide, clindamycine, amoxicilline-clavulanate, céfadroxil et doxycycline) dans le traitement des ostéomyélites et des infections de prothèse a été réalisée sur PubMed et Embase. La qualité des études et les niveaux de preuves ont été évalués avec la méthode SORT.
Revue du sujet traité: Au total, 2 619 études ont été identifiées, dont 34 ont été incluses. La ciprofloxacine, la rifampicine et le triméthoprime-sulfaméthoxazole sont les molécules administrées par voie orale les plus étudiées. Les données pour le linézolide, la clindamycine et le céfadroxil diffèrent, et aucune étude n’a évalué spécifiquement l’amoxicilline-clavulanate et la doxycycline administrées par voie orale. Ainsi, des données appuient l’utilisation des antibiotiques par voie orale, mais elles sont souvent de faible qualité du fait qu’elles proviennent souvent de petites études observationnelles.
Conclusion: Les antibiotiques par voie orale semblent efficaces dans le traitement des ostéomyélites et des infections de prothèse chez l’adulte. D’autres études de qualité sont toutefois nécessaires pour élaborer des recommandations fiables.
Mots-clés: adulte, antibiotique par voie orale, infection de prothèse, ostéomyélite
ABSTRACT
Objective: Osteomyelitis and prosthetic joint infections in adults have historically been treated with intravenous antibiotics. Recent data suggest that oral antibiotic therapy may be non-inferior to intravenous treatment, but there is limited evidence regarding the efficacy of specific agents. Therefore, a literature review was conducted to assess the effectiveness of commonly used oral antibiotics for these infections.
Data sources and study selection: A literature review was performed on the efficacy of several oral antibiotics (fluoroquinolones, rifampin, trimethoprim-sulfamethoxazole, linezolid, clindamycin, amoxicillin-clavulanate, cefadroxil, and doxycycline) in the treatment of osteomyelitis and prosthetic joint infections using PubMed and Embase. Study quality and levels of evidence were assessed using the SORT methodology.
Review of the Topic: A total of 2,619 studies were identified, of which 34 were included. Ciprofloxacin, rifampin, and trimethoprim-sulfamethoxazole were the most studied oral agents. Data on linezolid, clindamycin, and cefadroxil varied, and no studies specifically evaluated oral amoxicillin-clavulanate or doxycycline. While evidence supports the use of oral antibiotics, it is often of low quality due to reliance on small observational studies.
Conclusion: Oral antibiotics appear to be effective in treating osteomyelitis and prosthetic joint infections in adults. However, further high-quality studies are needed to develop reliable recommendations.
Keywords: adult, oral antibiotic, osteomyelitis, prosthetic joint infection
This abstract was translated using Microsoft 365 Copilot and subsequently reviewed by the editorial team.
Dans le passé, le traitement standard des ostéomyélites et des infections de prothèse consistait en l’administration d’antibiotiques par voie intraveineuse (IV) pendant plusieurs semaines1. Dans les dernières années, des études ont évalué la non-infériorité d’un traitement antibiotique par voie orale par rapport au traitement standard IV2,3. L’étude randomisée contrôlée multicentrique oral versus intravenous antibiotics for bone and joint infection (OVIVA), qui comprenait plus de 1 000 participants, a montré que le taux d’échec du traitement par voie orale (13,2 %) des ostéomyélites et des infections de prothèse était non-inférieur à celui du traitement IV (14,6 %) (différence de risque : −1,4 %, intervalle de confiance à 95 % : −5,6 à 2,9)3. Il est à noter qu’il y avait une grande hétérogénéité dans le choix et la dose des antibiotiques, les interventions ainsi que dans les agents pathogènes identifiés dans l’étude, ce qui complexifie l’interprétation des sous-groupes et de l’efficacité de chaque antibiotique. Une étude découlant d’OVIVA a aussi révélé que l’usage des antibiotiques par voie orale coûtait moins cher qu’en intraveineuse et n’était associé à aucune différence significative quant à la qualité de vie4.
Les ostéomyélites sont des infections osseuses qui peuvent être classées selon plusieurs critères, notamment le mode de transmission des germes, la durée depuis le début de l’infection et le foyer anatomique5. Par exemple, une ostéomyélite hématogène est causée par une bactérie provenant du sang tandis qu’une ostéomyélite non hématogène, ou par contiguïté, est la conséquence d’une infection des tissus mous adjacents. Autrement, une ostéomyélite aiguë se caractérise par des symptômes évoluant sur plusieurs jours ou plusieurs semaines comparativement à plusieurs mois ou plusieurs années pour l’ostéomyélite chronique.
Le traitement des infections de prothèse peut être chirurgical et médical. Les interventions chirurgicales les plus communes sont la réimplantation en un ou deux temps ainsi que la méthode DAIR (débridement, antibiotiques et rétention de l’implant)6–8. Le choix de l’intervention dépend entre autres du délai depuis l’implantation de la prothèse, de son emplacement, de l’agent pathogène en cause ainsi que des symptômes et des caractéristiques du patient.
La méthode DAIR est fréquemment envisagée lors d’infections aiguës d’une prothèse primaire, bien fixée, sans tractus sinusal entre l’articulation et la peau6,8. Les pièces mobiles de la prothèse sont alors changées et un lavage de l’articulation et un débridement des tissus infectés sont effectués. Un traitement antibiotique IV, suivi d’un traitement par voie orale, est habituellement administré pendant quatre à six semaines. Celui-ci peut parfois être suivi d’un autre traitement par voie orale pendant trois à six mois selon l’antibiotique sélectionné et l’articulation touchée. Un traitement suppressif par voie orale à long terme est ensuite commencé chez certains patients6. Toutefois, ce dernier ne sera pas abordé dans le présent article, pas plus que l’administration locale d’antibiotiques durant les interventions chirurgicales.
Pour les infections de prothèse chroniques et parfois pour certaines infections aiguës, le traitement de choix est le retrait de l’implant et la réimplantation en un ou deux temps8. Lors de la réimplantation en un temps, la prothèse est retirée complètement, les tissus sont débridés et un nouvel implant est posé pendant la même intervention. Le patient reçoit ensuite un antibiotique par voie orale ou IV pendant plusieurs semaines selon l’agent pathogène causal. Dans le cadre d’une réimplantation en deux temps, la prothèse est retirée et les tissus sont débridés lors de la première intervention. Un dispositif d’espacement délivrant un antibiotique est inséré temporairement. Une deuxième intervention aura lieu plusieurs semaines plus tard après l’administration d’antibiotiques systémiques, afin d’implanter une nouvelle prothèse6.
L’approche standard dans le traitement des ostéomyélites et des infections de prothèse est l’administration d’antibiotiques IV pendant toute la durée du traitement1. Cette approche exige une longue hospitalisation ou une antibiothérapie IV à domicile (ATIVAD) qui n’est pas accessible à tous les patients en raison des nombreux défis qu’elle pose : risque d’infections et de thromboses lié à l’installation d’un accès veineux central (parfois périphérique), absence de cliniques d’ATIVAD dans certaines régions, nombreux tests de laboratoire de routine nécessaires pour suivre l’efficacité et l’innocuité de certains antibiotiques IV9–11. Enfin, plusieurs facteurs sociaux constituent une barrière à l’accessibilité de ce service, tels qu’une prise en charge inadéquate à domicile, la salubrité et des troubles de toxicomanie. Ces problèmes illustrent donc la pertinence de regrouper les données existantes sur l’utilisation d’antibiotiques par voie orale dans le traitement des ostéomyélites et des infections de prothèse.
Selon un consensus d’experts sur la prise en charge des ostéomyélites, cinq critères doivent être présents pour permettre la transition de la voie IV à la voie orale12. L’état clinique du patient doit être stable, la source de l’infection doit être maîtrisée, le tractus gastro-intestinal du patient doit être fonctionnel et permettre l’absorption d’un médicament par voie orale, le traitement antibiotique doit être accessible et appuyé par des données scientifiques et le patient ne doit pas avoir de problèmes psychosociaux empêchant la prise optimale d’un médicament par voie orale.
L’objectif du présent article est de faire une revue de la littérature sur l’efficacité des traitements par voie orale des ostéomyélites et des infections de prothèse ainsi que de qualifier le niveau de preuves avec la méthode SORT pour chaque molécule selon le type d’infection. En outre, une revue sommaire de l’innocuité des antibiotiques sera effectuée. Une attention particulière sera portée aux molécules pour lesquelles nous disposons de moins de données probantes, soit l’amoxicilline-clavulanate, le céfadroxil et la doxycycline.
Une revue de la littérature sur l’efficacité et l’innocuité des différents antibiotiques par voie orale a été effectuée sur PubMed, ainsi que sur Embase pour les études de 1974 à 2024, selon les stratégies de recherche présentées dans l’annexe. Les antibiotiques par voie orale recensés étaient ceux de la classe des fluoroquinolones, la rifampicine, le triméthoprime-sulfaméthoxazole (TMP-SMX), le linézolide, la clindamycine, le céfadroxil, l’amoxicilline-clavulanate et la doxycycline. Ces agents ont été sélectionnés pour leur utilité dans le traitement des ostéomyélites et des infections liées aux prothèses en raison de leur bonne biodisponibilité orale et de leur diffusion osseuse. Les critères d’inclusion étaient les suivants : patient de 18 ans et plus, diagnostic d’ostéomyélite ou d’infection de prothèse et présence d’un traitement antibiotique par voie orale. Les critères d’exclusion étaient les suivants : infection du pied diabétique, autre infection concomitante, traitement suppressif ou prophylactique, étude n’évaluant pas l’efficacité d’un antibiotique par voie orale (objectif autre), objectif non clinique ne permettant pas d’évaluer l’efficacité d’un antibiotique par voie orale, étude de cas, étude cas-témoin et revue de la littérature ou revue systématique sans méta-analyse. La définition du succès ou de l’échec clinique varie d’une étude à l’autre et est présentée dans le tableau I. Les études ont été révisées indépendamment par deux étudiants de quatrième année en pharmacie à chaque étape du processus de sélection. Les conflits ont été résolus par consensus.
Afin d’augmenter la sensibilité de la stratégie de recherche, les études provenant de la base de données interne du Département de pharmacie de l’Hôpital Maisonneuve-Rosemont, secteur de l’antibiogouvernance, ainsi que certaines études pertinentes trouvées dans des revues systématiques ont été incluses pour bonifier la source des données.
La qualité des données probantes sur l’efficacité de chaque antibiotique par voie orale a été évaluée avec la méthode SORT13. Cette méthode a été choisie, car elle permet d’établir rapidement le niveau de preuves de 1 à 3 à l’aide de critères clairs. Elle est plus simple à interpréter par les cliniciens. En outre, elle prend en compte le type d’objectif (orienté vers le patient ou la maladie) dans l’évaluation du niveau de preuves des études, ce qui facilite l’extrapolation et l’interprétation des résultats dans un contexte pratique.
La qualité de chaque étude a été déterminée par la méthode décrite par Ebell et ses collaborateurs13. Par la suite, le niveau de preuves appuyant l’usage de chaque antibiotique a été établi selon la qualité de l’ensemble des études. Le niveau 1 indique que toutes les données probantes sont cohérentes et proviennent d’études randomisées contrôlées et/ou de méta-analyses de grande qualité. Le niveau 2 est attribué lorsque les données probantes se contredisent et/ou proviennent d’études randomisées contrôlées et/ou de méta-analyses de plus faible qualité ou d’études observationnelles. Le niveau 3 indique que toutes les données proviennent seulement d’études observationnelles de faible qualité, de consensus ou d’opinions d’experts, de pratique courante ou d’études de cas. Par exemple, s’il y avait une étude de niveau 1 et trois études de niveau 2 pour la molécule A, le niveau de preuves de la molécule A serait de 2 afin d’être cohérent avec l’ensemble des données. De même, s’il y avait trois études de niveau 2 et une étude de niveau 3 pour la molécule B, le niveau de preuves de cette molécule B serait aussi de 2.
La figure 1 montre le diagramme de flux de la revue de la littérature. Initialement, 2 619 articles ont été repérés avec la stratégie de recherche sur PubMed et Embase. Par la suite, 2 432 études ont été exclues après une lecture critique de leur titre et de leur résumé, car elles ne répondaient pas à la question de recherche et ont été jugées non pertinentes. Ensuite, 161 autres études ont été exclues selon les critères décrits précédemment. Trois études additionnelles provenant de la base de données interne du Département de pharmacie de l’Hôpital Maisonneuve-Rosemont et de certaines revues systématiques ont été ajoutées aux études incluses. Au total, 29 études ont été incluses et analysées. Les études individuelles sont présentées dans le tableau I par ordre chronologique inverse. Le niveau de preuves pour chaque molécule est présenté dans le tableau II.
|
| ||
|
Figure 1 Diagramme de flux de la revue de la littérature | ||
La revue de la littérature a permis de trouver plusieurs études montrant que les fluoroquinolones par voie orale sont efficaces dans le traitement des ostéomyélites et des infections de prothèse, dont plusieurs études randomisées contrôlées. Deux études ont comparé la ciprofloxacine (750 mg) en monothérapie administrée deux fois par jour par voie orale au traitement IV standard de l’ostéomyélite chronique après un débridement complet14,15. Dans l’étude randomisée contrôlée de Gentry, 77 % (24/31) des 31 patients recevant le traitement par voie orale ont eu un succès thérapeutique, défini comme l’absence de symptômes d’infection à la fin du traitement et lors des suivis14. Le taux de succès était d’ailleurs comparable à celui du groupe témoin (22/28, 79 %)14. Les bactéries identifiées le plus fréquemment étaient Pseudomonas æruginosa et Staphylococcus aureus sensible à la ciprofloxacine14. Les auteurs ont toutefois exclu tous les agents pathogènes résistant à la ciprofloxacine et les patients présentant une infection plus grave14. Mader a évalué ce même traitement dans le contexte d’une ostéomyélite chronique, définie par une durée d’infection de plus de six semaines15. Cette étude randomisée contrôlée a montré que le taux de succès du traitement de ciprofloxacine par voie orale en monothérapie, administrée pendant au moins quatre semaines après le débrideent, était de 79 % (11/14) et donc comparable au taux de succès du groupe ayant pris le traitement IV standard (10/12, 83 %)15. Il est à noter que la ciprofloxacine n’a pas été utilisée comme traitement suppressif chronique. Dan a évalué, dans une étude de cohorte rétrospective, le recours à la ciprofloxacine par voie orale (750 mg deux fois par jour pendant d’un à quatre mois) spécifiquement dans un contexte d’ostéomyélite à P. æruginosa chez 22 patients16. Il a observé un seul échec16.
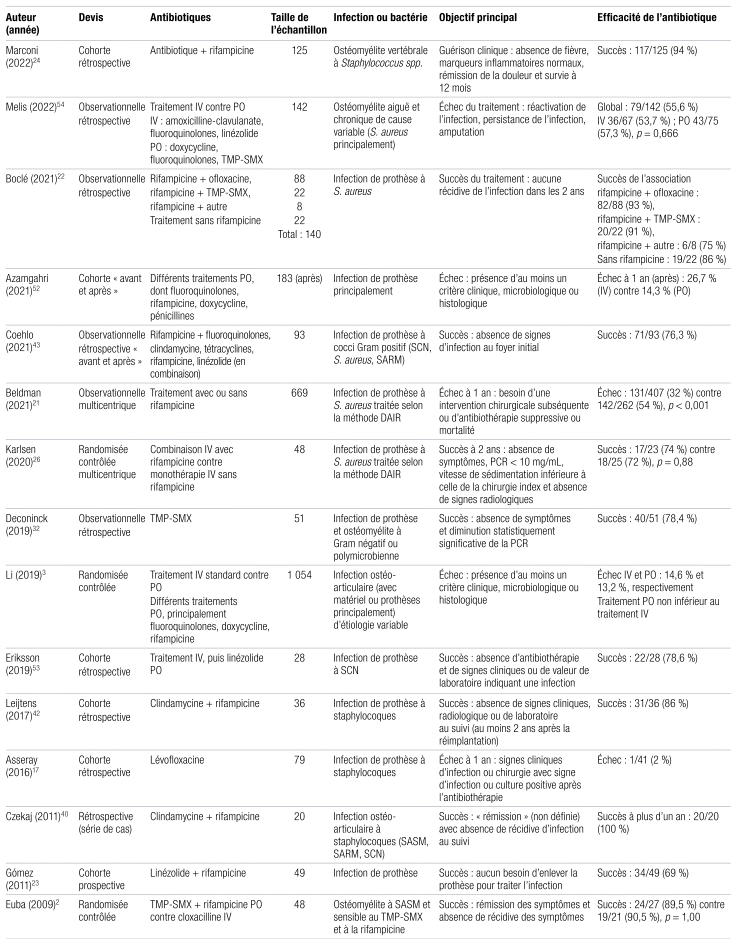
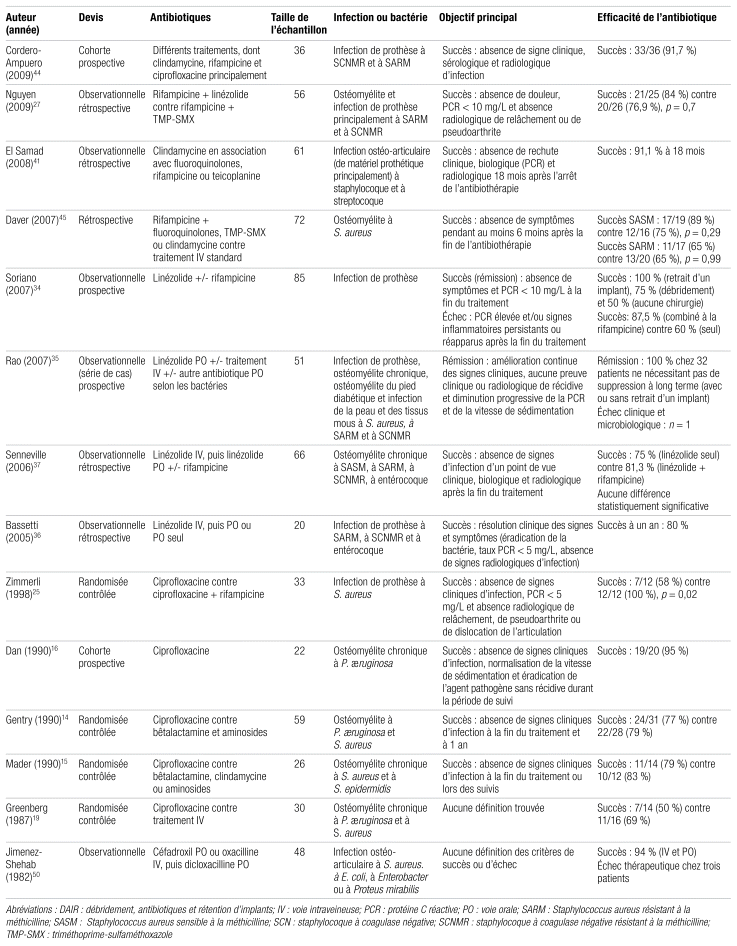
Tableau I Caractéristiques des études incluses
Pour ce qui est de la lévofloxacine, une étude de cohorte rétrospective plus récente a évalué son rôle dans le traitement des infections ostéo-articulaires, principalement des infections de prothèse17. La lévofloxacine, à raison de 500 mg par voie orale une fois par jour, a été combinée à au moins un autre agent antibiotique (surtout la rifampicine) chez 77 patients17. Le taux d’échec à un an était de 2 % (1/41). Il est important de noter qu’il est présentement recommandé d’employer les fluoroquinolones par voie orale en association avec un autre antibiotique en présence de staphylocoques afin de réduire au minimum le risque de résistance bactérienne6,12.
Les fluoroquinolones sont connues pour mener à des effets indésirables graves, comme des tendinopathies, un allongement de l’intervalle QT et les infections à Clostridioides difficile6,12,18. Plusieurs études ont donc évalué leur innocuité dans le traitement des ostéomyélites. Trois études randomisées contrôlées ont révélé un taux d’effets indésirables graves similaire pour les fluoroquinolones par voie orale et les antibiotiques IV14,15,19. Une étude observationnelle a montré qu’il n’y avait aucune différence statistiquement significative dans la fréquence des effets indésirables graves entre le groupe prenant des fluoroquinolones et celui n’en prenant pas (7,8 % contre 1,5 %, p = 0,14)20. Toutefois, le taux d’arrêt des antibiotiques était plus élevé dans le groupe recevant les fluoroquinolones comparativement au groupe témoin (35,6 % contre 3 %)20.
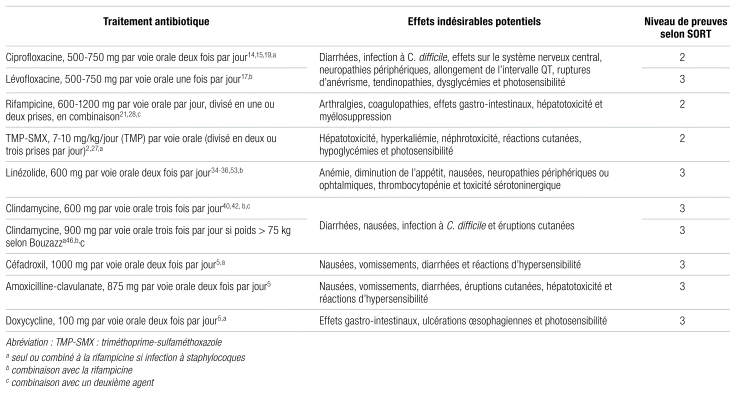
Tableau II Niveau de preuves pour le traitement par voie orale de l’ostéomyélite et des infections de prothèse
Les données probantes sur l’efficacité de la rifampicine dans les ostéomyélites et les infections de prothèse sont conflictuelles. Quelques études randomisées contrôlées ainsi que plusieurs études rétrospectives ont révélé que la rifampicine, en association avec d’autres antibiotiques, semble améliorer le taux de guérison des ostéomyélites et des infections de prothèse21–25. Une étude randomisée contrôlée chez les patients ayant une infection de prothèse à S. aureus a obtenu un taux de guérison clinique de 100 % grâce à la combinaison ciprofloxacine et rifampicine par voie orale comparativement au groupe ciprofloxacine seule par voie orale dans lequel le taux de guérison clinique était de 58 % chez 24 patients25. Cette étude phare de 1998 a été remise en question, car la monothérapie à la ciprofloxacine contre S. aureus n’est plus un traitement standard. Récemment, l’efficacité de la rifampicine a aussi été remise en cause dans une étude randomisée contrôlée qui a montré que son ajout au traitement IV standard n’avait pas d’effet statistiquement significatif dans le traitement des infections de prothèse26. La rifampicine doit toujours être utilisée en combinaison pour ce type d’infection et a surtout été étudiée en association avec des fluoroquinolones, le TMP-SMX et des bêtalactamines.
Les doses de rifampicine mentionnées dans les études varient de 600 mg jusqu’à 1200 mg par jour2,21,27. Une étude rétrospective incluant 386 patients a montré qu’il n’y avait pas de différence statistiquement significative quant à l’objectif primaire (absence d’infection à 12 mois) entre les doses faibles (moins de 10 mg/kg/jour), intermédiaires (10–20 mg/kg/jour) et élevées (plus de 20 mg/kg/jour) de rifampicine28. Cependant, la puissance de l’étude n’a pas été atteinte en raison du faible nombre de patients dans chaque sous-groupe.
La rifampicine est un antibiotique associé à divers types d’effets indésirables (gastro-intestinaux, immunoallergiques, hématologiques, hépatiques et cutanés)29. Selon une étude de cohorte prospective de 76 patients, il y avait plus d’effets indésirables dans le groupe rifampicine (n = 54) que dans le groupe témoin (n = 26) (72 % contre 28 %, p = 0,399), quoiqu’aucune différence statistiquement significative n’ait été trouvée30. Toutefois, cette même étude a montré que parmi les 28 patients nécessitant une modification de traitement en raison d’un effet indésirable, seulement deux prenaient de la rifampicine30.
L’efficacité du TMP-SMX est mentionnée dans une étude randomisée contrôlée et dans plusieurs études rétrospectives. En 2009, Euba a montré la non-infériorité de l’association de TMP-SMX et de rifampicine par voie orale par rapport à la cloxacilline IV dans le traitement des ostéomyélites à S. aureus2. Parmi les patients ayant reçu pendant huit semaines 600 mg par jour de rifampicine en combinaison avec le TMP-SMX à raison de 7 à 8 mg/kg/jour, trois échecs (3/27, 11 %) au traitement ont été constatés contre deux (2/21, 10 %) dans le groupe cloxacilline à la fin d’une période de suivi de 10 ans. Deconinck a évalué de façon rétrospective l’efficacité du TMP-SMX chez 51 patients ayant eu des infections de prothèse et des ostéomyélites. Le taux de succès a atteint 78 %32. Nguyen, quant à lui, a comparé le taux de guérison de la combinaison de rifampicine et de linézolide à celle de rifampicine et de TMP-SMX. Le taux de guérison après deux ans était similaire, soit 84 % comparativement à 77 % (p = 0,7)27. Boclé a inclus 22 patients présentant des infections de prothèse à S. aureus traités par le TMP-SMX en combinaison avec la rifampicine. Le taux de succès de leur étude rétrospective a atteint 91 %22.
Les doses de TMP-SMX utilisées varient de 4 à 10 mg/kg/jour de triméthoprime. Dans une étude, les doses étaient plus faibles, soit 160 mg de triméthoprime et 800 mg de sulfaméthoxazole par voie orale de deux à trois fois par jour2,27,32. Il est à noter que certaines données montrent un taux plus élevé d’échec avec des doses faibles (4–6 mg/kg/jour).
Une étude s’est attardée aux effets indésirables associés à l’utilisation d’antibiotiques à long terme dans le traitement des infections de prothèse30. Les effets indésirables rares du TMP-SMX ayant nécessité un arrêt ou un changement de traitement dans cette étude sont les réactions cutanées, la néphrotoxicité et les leucopénies. Les autres effets à surveiller sont l’hyperkaliémie et l’hépatotoxicité. Le risque d’hyperkaliémie est augmenté en présence de diabète, d’une kaliémie élevée avant la prescription de TMP-SMX à forte dose, d’une prise concomitante d’un inhibiteur de l’enzyme de conversion de l’angiotensine, d’un antagoniste des récepteurs de l’angiotensine II ou du sacubitril-valsartan, d’un diurétique épargneur de potassium ou d’un anti-inflammatoire non stéroïdien33.
Quelques études observationnelles et de cohorte se sont penchées sur l’efficacité du linézolide. Soriano a évalué de façon prospective l’efficacité du linézolide chez 24 patients ayant des implants orthopédiques et qui étaient traités pour une infection aiguë (présence de symptômes depuis moins de deux semaines). Parmi eux, six ont subi le retrait de leur implant, 16 ont eu des débridements et deux n’ont pas eu d’intervention intervention chirurgicale34. Le succès thérapeutique s’est élevé à 100 % avec le retrait de l’implant, à 75 % avec le débridement et à 50 % chez les patients qui n’ont pas eu d’intervention chirurgicale34. Rao a évalué de façon prospective l’utilisation du linézolide chez 51 patients, dont 23 avaient une infection de prothèse, 19 avaient une ostéomyélite chronique, six avaient une infection du pied diabétique et trois avaient des infections de la peau et des tissus mous35. À la suite du traitement, 32 des 51 patients (63 %) n’ont pas nécessité de suppression à long terme et ont eu un succès thérapeutique35. Une analyse rétrospective effectuée par Bassetti chez 20 patients ayant une infection de prothèse a d’ailleurs associé le linézolide par voie orale à un succès thérapeutique à long terme de 80 %36. Selon un consensus d’experts sur le sujet, le linézolide fait aussi partie des antibiotiques recommandés en cas d’infection de prothèse causée par des entérocoques et/ou par S. aureus résistant à la méthicilline (SARM)6. Des résultats contradictoires pour la combinaison rifampicine et linézolide ont également été obtenus. Une certaine diminution de l’exposition au linézolide par un mécanisme inconnu a été observée lors des études de mise en marché. Une étude prospective sur l’ostéomyélite chronique n’a révélé aucune différence statistiquement significative quant au succès clinique lors de l’ajout de la rifampicine alors que Soriano a eu un succès clinique plus élevé (88 % contre 60 %) avec cette association34,37. À noter que les deux études ont employé la même posologie de linézolide, soit 600 mg par voie orale deux fois par jour.
L’innocuité du linézolide est une source de préoccupations liée à son utilisation. Lors d’une administration prolongée, la thrombocytopénie, l’anémie, l’acidose lactique ainsi que la neuropathie périphérique ou la neuropathie ophtalmique parfois irréversible font partie des effets indésirables à surveiller31. En plus du risque de thrombocytopénie, une insuffisance rénale pourrait aussi avoir un effet sur les dosages plasmatiques. C’est pourquoi un suivi des concentrations est recommandé lors d’un traitement à long terme38. Un effet indésirable plus rare lié au mécanisme d’inhibition de la monoamine-oxydase augmente le risque de syndrome sérotoninergique chez les patients ayant d’autres facteurs de risque, dont la prise d’un médicament agissant sur la sérotonine31. Cependant, sa fréquence absolue dans différentes études randomisées ou rétrospectives est faible (moins de 0,5 % à 3 %)39. Ainsi, vu les effets indésirables hématologiques et neurologiques liés à une prise à long terme, un suivi et des précautions sont primordiaux dans le traitement des infections de prothèse par le linézolide.
La revue de la littérature a permis de trouver trois études rétrospectives portant spécifiquement sur la clindamycine, ainsi que quelques autres avec des sous-groupes d’étude ayant reçu ce traitement40–45. Une étude de cohorte rétrospective d’El Samad a évalué spécifiquement la clindamycine dans le traitement des infections ostéo-articulaires chez 61 patients. Les plus courantes mettaient en cause une prothèse articulaire (n = 31/61, 50,8 %)41. L’efficacité du traitement antibiotique à 18 mois était de 91,1 % (96,4 % d’infections ostéo-articulaires en présence de prothèse et 85,7 % sans présence de prothèse)41. Czekaj a évalué de façon rétrospective l’usage de la combinaison par voie orale de clindamycine et de rifampicine dans les infections ostéo-articulaires (y compris les infections de prothèse et d’implants et les ostéomyélites) à staphylocoques (SARM, S. aureus sensible à la méthicilline [SASM] et staphylocoques à coagulase négative [SCN])40. La posologie des antibiotiques était de 600 mg trois fois par jour pour la clindamycine et de 600 mg deux fois par jour pour la rifampicine, pendant une durée médiane de 45 jours40. Dans cette étude, tous les patients ont eu un succès thérapeutique, sans récurrence d’infection au suivi40. Cette même combinaison de clindamycine et de rifampicine a d’ailleurs été employée dans l’étude rétrospective de Leijtens chez 36 patients présentant une infection de prothèse à SASM et à SCN principalement, traités par la méthode DAIR ou par réimplantation en un ou deux temps42. Le succès thérapeutique a été observé dans 86 % des cas42.
Pour ce qui est de la posologie, la plupart des études ont utilisé la clindamycine à raison de 600 mg trois fois par jour40,42. Bouazza soulève un problème chez des patients ayant un poids supérieur à 75 kg, soit une augmentation de la clairance de l’antibiotique menant à une dose sous-thérapeutique46. Ils suggèrent ainsi d’accroître la dose de clindamycine à 900 mg trois fois par jour46. Toutefois, cette forte dose a aussi mis en lumière le plus grand risque d’effets gastro-intestinaux.
Il y a une interaction médicamenteuse entre la clindamycine et la rifampicine. En effet, l’induction de l’isoenzyme CYP3A4 du cytochrome P450 par la rifampicine diminue les concentrations plasmatiques de clindamycine et augmente le risque d’échec thérapeutique47,48. Les études de Leijtens et de Czekaj sur l’efficacité de cette combinaison ont cependant obtenu des résultats d’efficacité satisfaisants40,42. Bernard n’a pas observé de différence d’efficacité entre le groupe prenant l’association clindamycine et rifampicine et celui recevant la combinaison rifampicine et fluoroquinolone47.
Les effets indésirables de la clindamycine lors d’une prise prolongée incluent une réaction d’hypersensibilité, la diarrhée ainsi qu’un faible risque d’hépatotoxicité. Cependant, ce risque hépatique ne nécessite pas d’emblée un suivi de la fonction à l’aide de tests de laboratoire31. La diarrhée à C. difficile demeure toutefois un enjeu important associé à l’utilisation de la clindamycine, et les facteurs de risque associés (hospitalisation actuelle ou récente, prise de médicaments modifiant l’acidité gastrique, âge avancé, troubles gastro-intestinaux) doivent être pris en compte lors du choix de traitement49.
La revue de littérature a permis de trouver une seule étude ciblant spécifiquement le céfadroxil50. Jimenez-Shebab a mené une étude sur 48 adultes atteints d’infections ostéo-articulaires, dont 73 % étaient chroniques (plus de deux mois d’évolution) et 13 % étaient aiguës50. La moitié des patients ont pris du céfadroxil (1 g par voie orale toutes les six heures pendant 35 jours). Un taux de succès thérapeutique de 94 % a été obtenu50. Outre les études cliniques sur ce sujet, le céfadroxil a été présenté par un consensus d’experts comme un antibiotique par voie orale pouvant être employé dans le traitement des infections de prothèse à SASM, ainsi qu’à staphylocoques à coagulase négative sensible à la méthicilline6. Il est recommandé de le combiner à la rifampicine dans le cas d’infection à staphylocoques6.
La posologie recommandée est de 1000 mg par voie orale deux fois par jour, même si Jimenez-Shebab a eu recours à une posologie beaucoup plus élevée6,50.
L’innocuité de cette molécule semble rassurante pour une utilisation de plusieurs jours ou plusieurs semaines. En effet, les principaux effets indésirables mentionnés sont de type gastro-intestinal et incluent les nausées, les vomissements et les diarrhées. Les effets à long terme plus rares sont des réactions d’hypersensibilité ainsi qu’une hépatotoxicité31.
Cette revue de littérature n’a pas permis de trouver d’études sur l’amoxicilline-clavulanate par voie orale pour les ostéomyélites ou les infections de prothèse. Cette molécule ne faisait aussi pas partie des traitements évalués dans l’essai randomisé contrôlé de non-infériorité de grande envergure OVIVA3. Cependant, un consensus d’experts sur le traitement de l’ostéomyélite a recommandé l’amoxicilline-clavulanate à raison de 500 mg d’amoxicilline trois fois par jour ou de 875 mg d’amoxicilline deux fois par jour contre les ostéomyélites associées à une infection du pied diabétique12. Ce consensus d’experts est d’ailleurs cohérent avec les différentes lignes directrices sur le pied diabétique dans lesquelles l’amoxicilline-clavulanate (875 mg deux fois par jour) constitue une option de traitement par voie orale12,51. Cette association ne fait toutefois pas partie des antibiotiques recommandés par un consensus d’experts pour les infections de prothèse6.
Le manque de données probantes en limite l’usage, mais son profil d’innocuité est plutôt favorable. En effet, ses principaux effets indésirables sont de nature gastro-intestinale (nausées, vomissements et diarrhées) et dermatologique (risque d’éruptions cutanées ou de réaction d’hypersensibilité)31.
Aucune étude n’a spécifiquement évalué l’efficacité de la doxycycline par voie orale dans le traitement des ostéomyélites et des infections de prothèse. Les données sur son efficacité sont tirées d’études portant sur le traitement de l’ostéomyélite dans des sous-groupes de patients prenant de la doxycycline3,43,44,52,54. Dans l’étude d’OVIVA, 10,9 % des patients du groupe recevant le traitement par voie orale prenaient de la doxycycline3. Dans une étude pré-post intervention, évaluant la reproductibilité des résultats du protocole de l’étude OVIVA, plus du quart des patients du groupe post recevant un traitement par voie orale ont eu la doxycycline comme antibiotique, en association avec un second agent52. Bien qu’une partie significative des patients recevait la doxycycline, aucune analyse de sous-groupe ne permet d’en tirer spécifiquement des données d’efficacité52. Pour ce qui est de la posologie de la doxycycline, les données des études recensées ne fournissent pas cette information. Un consensus d’expert recommande 100 mg deux fois par jour en combinaison avec la rifampicine pour les infections de prothèse à SASM et à staphylocoques à coagulase négative sensible à la méthicilline6.
Quant à son innocuité, la doxycycline présente un profil assez favorable. Ses effets indésirables lors d’une prise à long terme sont la photosensibilité, le risque d’ulcération œsophagienne, les nausées et les diarrhées31,55. D’autres effets indésirables plus rares peuvent aussi survenir.
Globalement, l’utilisation de la voie orale pour l’antibiothérapie des ostéomyélites et des infections de prothèse est appuyée par plusieurs études. Le niveau de preuves soutenant l’efficacité de chaque molécule est présenté dans le tableau II. Bien entendu, le patient doit répondre à des critères précis pour devenir candidat à une antibiothérapie par voie orale. Certains points de discorde persistent : doit-on toujours commencer par quelques jours ou quelques semaines de traitement IV avant de passer à la voie orale? Quel agent privilégier? Quelle dose utiliser? À l’aide d’une approche pragmatique, il est possible de suggérer une conduite pour les deux derniers points.
Les molécules de cette classe d’antibiotiques sont les plus étudiées dans le traitement de l’ostéomyélite, mais la majorité des données probantes portent sur la ciprofloxacine. Aucune étude randomisée contrôlée évaluant formellement l’effet de la moxifloxacine et de la lévofloxacine dans le traitement des ostéomyélites chez l’humain n’a été trouvée. Les études randomisées contrôlées montrent que l’utilisation de la ciprofloxacine orale mène à un taux de succès similaire aux traitements IV dans le traitement des ostéomyélites. Cependant, deux de ces études incluent des ostéomyélites chroniques, ce qui limite l’extrapolation des résultats aux infections aiguës (qui ne sont pas nécessairement causées par les mêmes bactéries)14,15,19. En outre, la généralisation de ces résultats est restreinte par la petite taille d’échantillon des études et par le fait qu’elles ont été menées il y a plus de 30 ans. Il faut aussi rappeler que les fluoroquinolones par voie orale sont souvent employées en combinaison avec un autre antibiotique dans ce type d’infection pour réduire le plus possible le risque de résistance bactérienne6,12. L’efficacité des fluoroquinolones dans le traitement des ostéomyélites est aussi appuyée par plusieurs études observationnelles, mais celles-ci sont également limitées par leur petite taille d’échantillon, l’absence de groupes comparateurs et la présence de plusieurs biais16,17.
Bien que les fluoroquinolones soient associées à plusieurs effets indésirables rares (p. ex. : tendinopathie et allongement de l’intervalle QT), les données sur leur innocuité sont rassurantes pour leur usage sur une période de plusieurs semaines15–17,19,20. Cependant, ces effets indésirables entraînent un taux d’abandon de 36 %20. En outre, il serait préférable d’éviter les fluoroquinolones chez des patients présentant déjà une tendinopathie pour ne pas risquer d’exacerber ce problème. Par conséquent, il est nécessaire de prendre en compte la tolérance à long terme des fluoroquinolones lors de leur prescription dans le traitement des ostéomyélites et des infections de prothèse.
La combinaison fluoroquinolone et rifampicine est davantage étudiée dans la littérature que les autres combinaisons. Cependant, les études portant spécifiquement sur l’efficacité de l’ajout de la rifampicine présentent des résultats divergents. L’étude randomisée de Zimmerli, considérée par plusieurs comme la preuve de l’efficacité de la rifampicine en présence de rétention de matériel, mentionne la supériorité de l’association rifampicine et ciprofloxacine comparativement à la ciprofloxacine seule. Toutefois, cette étude a seulement inclus 12 patients dans chaque groupe25. Inversement, les résultats d’une autre étude randomisée contrôlée analysant la combinaison de la rifampicine avec différents antibiotiques IV se sont révélés négatifs26. Donc, les données d’efficacité de la rifampicine présentées dans la littérature sont contradictoires, mais semblent globalement appuyer les bienfaits de cette molécule lors du traitement oral en combinaison. La rifampicine était surtout étudiée pour les infections de prothèse (hanche ou genou) à staphylocoques traitées par la méthode DAIR, pour la réimplantation en un temps et pour le traitement des ostéomyélites21–26. Certains auteurs suggèrent de combiner les fluoroquinolones et la rifampicine lors du traitement des infections de prothèse ou des ostéomyélites à staphylocoques en raison des risques d’émergence de résistance12. En outre, comme la rifampicine est un inducteur fort du CYP 3A4, il est important de toujours vérifier la présence d’interactions médicamenteuses lors de son introduction.
Pour ce qui est du TMP-SMX, la revue de littérature a permis de trouver une seule étude randomisée contrôlée de petite taille et plusieurs données rétrospectives sur le traitement des ostéomyélites et des infections de prothèse avec ou sans rétention de l’implant2. Toutefois, elle comparait le TMP-SMX par voie orale directement au traitement IV standard des ostéomyélites, ce qui ajoute à sa qualité. Les données rétrospectives existantes portaient également sur un faible nombre de patients, mais les résultats vont tous dans le sens d’une efficacité supérieure à 70 %27,32,45. La dose recommandée selon la revue de littérature serait de 7 à 10 mg/kg/jour de triméthoprime. En outre, il serait prudent de ne pas administrer le TMP-SMX en cas d’hyperkaliémie afin de ne pas aggraver cette dernière.
Des études observationnelles et de cohorte rapportent une bonne efficacité du linézolide dans le traitement des infections de prothèse avec des succès thérapeutiques de 79 % et plus. Certains suivis ont d’ailleurs été menés sur plusieurs années53. Cependant, ces études ont une petite taille d’échantillon et ne permettent pas d’atteindre un haut niveau de preuves. Cette molécule ne devrait donc pas figurer parmi les premiers choix de traitement. Son profil d’innocuité est acceptable à court terme, mais un suivi particulier est nécessaire lors d’une utilisation à long terme en raison d’un risque hématologique et surtout neurologique parfois irréversible31.
Très peu de données probantes appuient l’utilisation de la clindamycine, du céfadroxil, de l’amoxicilline-clavulanate ou de la doxycycline pour traiter les ostéomyélites et les infections de prothèse. Les données sur l’efficacité de la clindamycine semblent favorables, mais celles-ci proviennent d’études avec de petites tailles d’échantillons40–45. Concernant le céfadroxil, une seule étude supporte son usage, mais elle a été menée en 1982, a une petite taille d’échantillon (n = 48) et sa validité interne est très faible en raison du manque d’explications sur le devis et les issues étudiés, ce qui limite l’interprétation des résultats50. Enfin, les données d’efficacité de l’amoxicilline-clavulanate et de la doxycycline proviennent de sous-groupes d’autres études3,43,52,54. L’utilisation de ces molécules est cependant endossée par des consensus d’experts6,12. Leur innocuité est également rassurante. Toutefois, des doses de clindamycine de 900 mg par voie orale trois fois par jour, comme le propose Bouazza pour des patients de plus de 75 kg, pourraient augmenter le risque d’effets indésirables gastro-intestinaux et devraient nécessiter une analyse risques-avantages supplémentaire avec le patient.
Tout d’abord, la recherche s’est effectuée dans deux bases de données (PubMed et Embase) et a utilisé une stratégie de recherche sensible identifiant 2 619 articles, ce qui a réduit le risque d’éliminer des études importantes d’emblée. En outre, chaque étude a été analysée par deux personnes indépendantes et à l’insu. Les conflits ont été résolus en groupe, ce qui a également réduit le risque d’exclure une étude qui aurait dû être incluse, et vice-versa. Une autre force de cette revue est le recensement des données d’efficacité de molécules moins étudiées, comme la clindamycine, le céfadroxil, la doxycycline et l’amoxicilline-clavulanate permettant aux cliniciens de prendre des décisions plus éclairées sur l’utilisation d’antibiotiques alternatifs. Enfin, cette revue a permis de catégoriser les niveaux de preuves pour chaque molécule à l’aide de la méthode SORT pour faciliter l’interprétation des résultats et permettre aux cliniciens de prendre des décisions plus rapidement.
Cette revue de littérature comporte toutefois certaines limites. Tout d’abord, l’accessibilité aux ressources a été un problème, ce qui explique pourquoi les articles écrits dans une autre langue que l’anglais ou le français, sans traduction disponible, ont été exclus. De plus, l’inclusion du terme « oral » dans la stratégie de recherche semble avoir limité la sensibilité de la recherche, car certains articles d’intérêt n’ont pas été trouvés. À l’inverse, son exclusion conduisait à une recherche beaucoup trop sensible et peu spécifique menant à environ 29 000 articles. Par conséquent, il a été convenu d’inclure le terme « oral » afin de demeurer réaliste dans l’envergure du projet et de faire une recherche additionnelle moins exhaustive sur chaque molécule dans le cas où le nombre d’articles serait faible afin de pallier cette limite. Cette façon de faire aurait d’ailleurs pu limiter le nombre de données probantes pour les molécules moins utilisées, telles que la doxycycline, l’amoxicilline-clavulanate et le céfadroxil.
Ensuite, les populations incluses dans les différentes études étaient hétérogènes et de petite taille d’échantillon. Il est donc difficile de généraliser avec certitude les résultats de ces études à d’autres populations.
Une autre limite est le manque d’homogénéité dans la définition d’un succès de traitement des ostéomyélites et des infections de prothèse d’une étude à l’autre. À titre d’exemple, Mader considérait qu’un succès était l’absence de preuves d’infection à la fin du traitement et aux suivis, tandis que Dan estimait plutôt qu’il s’agissait de la disparition des signes et des symptômes d’infection, de la normalisation du taux de sédimentation érythrocytaire et de l’éradication de la bactérie causale sans récidive aux suivis15,16. Par conséquent, les comparaisons directes des résultats entre les études doivent être faites avec prudence.
Enfin, dans la grande majorité des études randomisées contrôlées, observationnelles et de cohorte, les patients avaient subi une intervention chirurgicale, un débridement ou un retrait de l’implant. Cependant, le choix d’intervention accompagnant le traitement antibiotique n’était pas bien établi dans les études et ne faisait pas partie des objectifs de cette revue de littérature. Aucune conclusion ne peut donc être tirée sur le choix de l’intervention, ce dernier reposant sur les pratiques locales.
Somme toute, le choix du traitement doit être individualisé. Ni la voie IV ni la voie orale ne conviennent à tous les patients. Le choix de l’antibiothérapie est fonction de diverses considérations, dont celles liées à la personne (maladies concomitantes et facteurs psychosociaux), au type d’infection et au médicament (profils d’effets indésirables et de sensibilité). Bien au-delà des caractéristiques cliniques du patient, il faut aussi considérer l’accessibilité aux traitements intraveineux ainsi que le risque écologique de l’utilisation des antibiotiques. En effet, le choix d’antibiotiques peut avoir un effet collatéral sur le microbiome et accroître le risque de résistance bactérienne pour plusieurs antibiotiques, dont les fluoroquinolones. Il importe donc de limiter l’émergence d’une résistance aux fluoroquinolones afin de préserver leur utilisation pour des bactéries, comme P. æruginosa, qui peuvent être efficacement traitées par ces dernières59. La modification du microbiome peut aussi augmenter le risque d’infection à C. difficile, surtout lors de l’emploi de fluoroquinolones et de clindamycine18,49.
En conclusion, cette revue de la littérature a permis de classifier le niveau de preuves des traitements par voie orale des ostéomyélites et des infections de prothèse. Compte tenu du poids de la preuve, les fluoroquinolones et le TMP-SMX en combinaison avec la rifampicine pourraient être considérés en première intention pour le traitement par voie orale de ces types d’infections. Cependant, comme ces antibiotiques sont associées à un haut taux d’interruption de traitement à long terme et à un potentiel d’interactions important, d’autres options doivent être disponibles. Cette évaluation de la littérature soulève la nécessité de mener des études de qualité qui mesurent spécifiquement l’efficacité de différents traitements antibiotiques afin de formuler des recommandations avec un meilleur niveau de preuves. L’élaboration de ces recommandations pourrait ensuite ouvrir la porte au développement de lignes directrices locales qui tiennent compte du profil de résistance et des caractéristiques individuelles des patients de chaque milieu pour ainsi favoriser le passage du traitement IV vers le traitement par voie orale.
Le pharmacien, en tant qu’expert du médicament, peut guider les équipes soignantes vers un meilleur usage des antibiotiques en nuançant le paradigme que la voie intraveineuse est nécessairement meilleure que la voie orale. En collaboration avec les équipes et les patients, le pharmacien peut proposer des alternatives de traitements par voie orale adaptés, moins invasifs et ne compromettant pas l’efficacité du traitement.
Cet article comporte une annexe, disponible sur le site de Pharmactuel ( www.pharmactuel.com)
Les auteurs n’ont déclaré aucun financement lié au présent article.
Tous les auteurs ont soumis le formulaire de l’ICMJE sur la divulgation de conflits d’intérêts potentiels. Les auteurs n’ont déclaré aucun conflit d’intérêts lié au présent article.
1. Cortés-Penfield NW, Kulkarni PA. The history of antibiotic treatment of osteomyelitis. Open Forum Infect Dis 2019;6:ofz181.


2. Euba G, Murillo O, Fernández-Sabé N, Mascaró J, Cabo J, Pérez A et al. Long-term follow-up trial of oral rifampin-cotrimoxazole combination versus intravenous cloxacillin in treatment of chronic staphylococcal osteomyelitis. Antimicrob Agents Chemother 2009;53:2672–6.


3. Li HK, Rombach I, Zambellas R, Walker AS, McNally MA, Atkins BL et al. Oral versus intravenous antibiotics for bone and joint infection. N Engl J Med 2019;380:425–36.


4. McMeekin N, Geue C, Briggs A, Rombach I, Li HK, Bejon P et al. Cost-effectiveness of oral versus intravenous antibiotics (OVIVA) in patients with bone and joint infection: evidence from a non-inferiority trial. Wellcome Open Res 2019;4:108.

5. Bury DC, Rogers TS, Dickman MM. Osteomyelitis: diagnosis and treatment. Am Fam Physician 2021;104:395–402.

6. Nelson SB, Pinkney JA, Chen AF, Tande AJ. Periprosthetic joint infection: current clinical challenges. Clin Infect Dis 2023;77:e34–45.


7. Tande AJ, Patel R. Prosthetic joint infection. Clin Microbiol Rev 2014;27:302–45.


8. Zijlstra WP, Ploegmakers JJW, Kampinga GA, Toren-Wielema ML, Ettema HB, Knobben BAS et al. A protocol for periprosthetic joint infections from the Northern Infection Network for Joint Arthroplasty (NINJA) in the Netherlands. Arthroplasty 2022;4:19.


9. Seidelman J, Sexton DJ. Is long-term oral therapy for treatment of bone and joint infections ready for prime time? Clin Infect Dis 2021;73:e2589–91.

10. Smith T, Daniels P, Rittmann B. Complex outpatient antimicrobial therapy: alternative management strategies and outcomes. Curr Infect Dis Rep 2023;25:1–8.

11. Norris AH, Shrestha NK, Allison GM, Keller SC, Bhavan KP, Zurlo JJ et al. 2018 Infectious Diseases Society of America clinical practice guideline for the management of outpatient parenteral antimicrobial therapy. Clin Infect Dis 2019;68:e1–e35.

12. Spellberg B, Aggrey G, Brennan MB, Footer B, Forrest G, Hamilton F et al. Use of novel strategies to develop guidelines for management of pyogenic osteomyelitis in adults: a WikiGuidelines group consensus statement. JAMA Netw Open 2022;5:e2211321.


13. Ebell MH, Siwek J, Weiss BD, Woolf SH, Susman J, Ewigman B et al. Strength of recommendation taxonomy (SORT): a patient-centered approach to grading evidence in the medical literature. J Am Board Fam Pract 2004;17:59–67.


14. Gentry LO, Rodriguez GG. Oral ciprofloxacin compared with parenteral antibiotics in the treatment of osteomyelitis. Antimicrob Agents Chemother 1990;34:40–3.


15. Mader JT, Cantrell JS, Calhoun J. Oral ciprofloxacin compared with standard parenteral antibiotic therapy for chronic osteomyelitis in adults. J Bone Joint Surg Am 1990;72:104–10.


16. Dan M, Siegman-Igra Y, Pitlik S, Raz R. Oral ciprofloxacin treatment of Pseudomonas aeruginosa osteomyelitis. Antimicrob Agents Chemother 1990;34:849–52.


17. Asseray N, Bourigault C, Boutoille D, Happi L, Touchais S, Corvec S et al. Levofloxacin at the usual dosage to treat bone and joint infections: a cohort analysis. Int J Antimicrob Agents 2016;47:478–81.


18. McCusker ME, Harris AD, Perencevich E, Roghmann MC. Fluoroquinolone use and Clostridium difficile-associated diarrhea. Emerg Infect Dis 2003;9:730–3.


19. Greenberg RN, Tice AD, Marsh PK, Craven PC, Reilly PM, Bollinger M et al. Randomized trial of ciprofloxacin compared with other antimicrobial therapy in the treatment of osteomyelitis. Am J Med 1987;82:266–9.

20. Vollmer NJ, Rivera CG, Stevens RW, Oravec CP, Mara KC, Suh GA et al. Safety and tolerability of fluoroquinolones in patients with staphylococcal periprosthetic joint infections. Clin Infect Dis 2021;73:850–6.


21. Beldman M, Löwik C, Soriano A, Albiach L, Zijlstra WP, Knobben BAS et al. If, when, and how to use rifampin in acute staphylococcal periprosthetic joint infections, a multicentre observational study. Clin Infect Dis 2021;73:1634–41.


22. Boclé H, Lavigne JP, Cellier N, Crouzet J, Kouyoumdjian P, Sotto A et al. Effectiveness of early switching from intravenous to oral antibiotic therapy in Staphylococcus aureus prosthetic bone and joint or orthopedic metalware-associated infections. BMC Musculoskelet Disord. 2021;22:315.


23. Gómez J, Canovas E, Baños V, Martínez L, García E, Hernández-Torres A et al. Linezolid plus rifampin as a salvage therapy in prosthetic joint infections treated without removing the implant. Antimicrob Agents Chemother 2011;55:4308–10.


24. Marconi L, Tedeschi S, Zamparini E, Terzi S, Rossi N, Boriani L et al. Oral versus standard antimicrobial treatment for pyogenic native vertebral osteomyelitis: a single-center, retrospective, propensity score-balanced analysis. Open Forum Infect Dis 2022;9:ofac366.


25. Zimmerli W, Widmer AF, Blatter M, Frei R, Ochsner PE. Role of rifampin for treatment of orthopedic implant-related staphylococcal infections: a randomized controlled trial. Foreign-Body Infection (FBI) Study Group. JAMA 1998;279:1537–41.


26. Karlsen ØE, Borgen P, Bragnes B, Figved W, Grøgaard B, Rydinge J et al. Rifampin combination therapy in staphylococcal prosthetic joint infections: a randomized controlled trial. J Orthop Surg Res 2020;15:365.


27. Nguyen S, Pasquet A, Legout L, Beltrand E, Dubreuil L, Migaud H et al. Efficacy and tolerance of rifampicin-linezolid compared with rifampicin-cotrimoxazole combinations in prolonged oral therapy for bone and joint infections. Clin Microbiol Infect 2009;15:1163–9.


28. Tonnelier M, Bouras A, Joseph C, Samad YE, Brunschweiler B, Schmit JL et al. Impact of rifampicin dose in bone and joint prosthetic device infections due to Staphylococcus spp: a retrospective single-center study in France. BMC Infect Dis 2021;21:174.


29. Miller R, Higuera CA, Wu J, Klika A, Babic M, Piuzzi NS. Periprosthetic joint infection: a review of antibiotic treatment. JBJS Rev 2020; 8:e1900224.


30. Reinecke P, Morovic P, Niemann M, Renz N, Perka C, Trampuz A et al. Adverse events associated with prolonged antibiotic therapy for periprosthetic joint infections–A prospective study with a special focus on rifampin. Antibiotics (Basel) 2023;12:1560.

31. Pertzborn M, Rivera CG, Tai DBG. Taking the route less traveled: on the way to COpAT. Ther Adv Infect Dis 2023;10:20499361231192771.

32. Deconinck L, Dinh A, Nich C, Tritz T, Matt M, Senard O et al. Efficacy of cotrimoxazole (sulfamethoxazole-trimethoprim) as a salvage therapy for the treatment of bone and joint infections (BJIs). PLoS One 2019;14:e0224106.


33. Fare PB, Memoli E, Treglia G, Bianchetti MG, Milani GP, Marchisio P et al. Trimethoprim-associated hyperkalaemia: a systematic review and meta-analysis. J Antimicrob Chemother 2022;77:2588–95.


34. Soriano A, Gómez J, Gómez L, Azanza JR, Pérez R, Romero F et al. Efficacy and tolerability of prolonged linezolid therapy in the treatment of orthopedic implant infections. Eur J Clin Microbiol Infect Dis 2007;26:353–6.


35. Rao N, Hamilton CW. Efficacy and safety of linezolid for Gram-positive orthopedic infections: a prospective case series. Diagn Microbiol Infect Dis 2007;59:173–9.


36. Bassetti M, Vitale F, Melica G, Righi E, Di Biagio A, Molfetta L et al. Linezolid in the treatment of Gram-positive prosthetic joint infections. J Antimicrob Chemother 2005;55:387–90.


37. Senneville E, Legout L, Valette M, Yazdanpanah Y, Beltrand E, Caillaux M et al. Effectiveness and tolerability of prolonged linezolid treatment for chronic osteomyelitis: a retrospective study. Clin Ther 2006;28:1155–63.


38. Kawasuji H, Tsuji Y, Ogami C, Kimoto K, Ueno A, Miyajima Y et al. Proposal of initial and maintenance dosing regimens with linezolid for renal impairment patients. BMC Pharmacol Toxicol 2021;22:13.


39. Bai AD, McKenna S, Wise H, Loeb M, Gill SS. Association of linezolid with risk of serotonin syndrome in patients receiving antidepressants. JAMA Netw Open 2022;5:e2247426.


40. Czekaj J, Dinh A, Moldovan A, Vaudaux P, Gras G, Hoffmeyer P et al. Efficacy of a combined oral clindamycin-rifampicin regimen for therapy of staphylococcal osteoarticular infections. Scand J Infect Dis 2011;43:962–7.


41. El Samad Y, Havet E, Bentayeb H, Olory B, Canarelli B, Lardanchet JF et al. Traitement des infections ostéo-articulaires par clindamycine chez l’adulte. Med Mal Infect 2008;38: 465–70.


42. Leijtens B, Elbers JBW, Sturm PD, Kullberg BJ, Schreurs BW. Clindamycin-rifampin combination therapy for staphylococcal periprosthetic joint infections: a retrospective observational study. BMC Infect Dis 2017;17:321.


43. Coehlo A, Robineau O, Titecat M, Blondiaux N, Dezeque H, Patoz P et al. Fully oral targeted antibiotic therapy for gram-positive cocci-related periprosthetic joint infections: a real-life before and after study. J Antimicrob Chemother 2021;76:3033–6.


44. Cordero-Ampuero J, Esteban J, García-Cimbrelo E. Oral antibiotics are effective for highly resistant hip arthroplasty infections. Clin Orthop Relat Res 2009;467:2335–42.


45. Daver NG, Shelburne SA, Atmar RL, Giordano TP, Stager CE, Reitman CA et al. Oral step-down therapy is comparable to intravenous therapy for Staphylococcus aureus osteomyelitis. J Infect 2007;54:539–44.


46. Bouazza N, Pestre V, Jullien V, Curis E, Urien S, Salmon D et al. Population pharmacokinetics of clindamycin orally and intravenously administered in patients with osteomyelitis. Br J Clin Pharmacol 2012;74:971–7.


47. Bernard A, Kermarrec G, Parize P, Caruba T, Bouvet A, Mainardi JL et al. Dramatic reduction of clindamycin serum concentration in staphylococcal osteoarticular infection patients treated with the oral clindamycin-rifampicin combination. J Infect 2015;71:200–6.


48. Goulenok T, Seurat J, Selle AdL, Jullien V, Leflon-Guibout V, Grall N et al. Pharmacokinetic interaction between rifampicin and clindamycin in staphylococcal osteoarticular infections. Int J Antimicrob Agents 2023;62: 106885.


49. Vardakas KZ, Trigkidis KK, Boukouvala E, Falagas ME. Clostridium difficile infection following systemic antibiotic administration in randomised controlled trials: a systematic review and meta-analysis. IntJAntimicrob Agents 2016; 48:1–10.

50. Jimenez-Shehab M, Barragan A. Oral cefadroxil in the treatment of bone and joint infections in children and adults. J Antimicrob Chemother 1982;10(suppl. B):149–52.


51. Senneville É, Albalawi Z, van Asten SA, Abbas ZG, Allison G, Aragón-Sánchez J et al. IWGDF/IDSA guidelines on the diagnosis and treatment of diabetes-related foot infections (IWGDF/IDSA 2023). Diabetes Metab Res Rev 2024;40:e3687.

52. Azamgarhi T, Shah A, Warren S. Clinical experience of implementing oral versus intravenous antibiotics (OVIVA) in a specialist orthopedic hospital. Clin Infect Dis 2021;73:e2582–8.

53. Eriksson HK, Ahadpour D, Hailer NP, Lazarinis S, Järhult JD. Linezolid in the treatment of periprosthetic joint infection caused by coagulase-negative staphylococci. Infect Dis (Lond) 2019;51:683–90.


54. Melis F, De Vito A, Fiore V, Rostagno R, Ravera L, Babudieri S et al. Is oral antibiotic therapy as effective as intravenous treatment in bacterial osteomyelitis? A real-life experience. Eur Rev Med Pharmacol Sci 2022;26:4069–73.

55. Holmes NE, Charles PGP. Safety and efficacy review of doxycycline. Clin Med Ther 2009;1.
56. Kurapatti M, Oakley C, Singh V, Aggarwal VK. Antibiotic therapy in 2-stage revision for periprosthetic joint infection: A systematic review. JBJS Rev 2022;10.
57. Larrazabal RB, Chiu HH, Arcegono MS, Abad CLR. Oral versus intravenous antibiotic treatment for osteomyelitis in adults: a systematic review and meta-analysis. Philipp J Intern Med 2020;58:146–53.
58. Wald-Dickler N, Holtom PD, Phillips MC, Centor RM, Lee RA, Baden R et al. Oral is the new IV. Challenging decades of blood and bone infection dogma: a systematic review. Am J Med 2022;135:369–79.e1.

59. Paterson DL. “Collateral damage” from cephalosporin or quinolone antibiotic therapy. Clin Infect Dis 2004;38(suppl 4):S341–S345.

Pour toute correspondance : Mikhail-Paul Cardinal, Centre universitaire de santé McGill, 1001 boul. Décarie, Montréal (Québec) H4A 3J1 CANADA; téléphone : 514 252-3400 poste 4294; courriel : mikhail-paul.cardinal@umontreal.ca
PHARMACTUEL, Vol. 58, No. 4, 2025