Mathis Laverdière1, B.Sc., Nicolas Martel-Côté2, B.Sc., D.E.S.S., Thaïna-Rafi Jean-Baptiste2, B.Sc., D.E.S.S., Denis Lebel3, B.Pharm., M.Sc. FCSHP., FOPQ., Jean-François Bussières4,5, B.Pharm., M.Sc., MBA, FCSHP, FOPQ
1 Assistant de recherche au moment de l’étude, département de pharmacie, Unité de recherche en pratique pharmaceutique, Centre hospitalier universitaire Sainte-Justine, Montréal, Québec, Canada;
2 Spécialiste en activités cliniques, département de pharmacie, Unité de recherche en pratique pharmaceutique, Centre hospitalier universitaire Sainte-Justine, Montréal, Québec, Canada;
3 Chef du Département de pharmacie, Centre hospitalier universitaire Sainte-Justine, Montréal, Québec, Canada;
4 Pharmacien responsable, Unité de recherche en pratique pharmaceutique, Centre hospitalier universitaire Sainte-Justine, Montréal, Québec, Canada;
5 Professeur titulaire de clinique, Faculté de pharmacie, Université de Montréal, Montréal, Québec, Canada
Reçu le 6 mars 2025; accepté après révision le 25 novembre 2025
https://doi.org/10.63209/2026.1587
RÉSUMÉ
Objectif: Décrire le degré de conformité aux bonnes pratiques de pharmacovigilance en établissement de santé au Québec en 2023. Comparer ces données à celles recueillies en 2019. Évaluer la satisfaction des participants à l’égard de la communauté de pratique en pharmacovigilance au Québec.
Méthode: Il s’agit d’une étude descriptive transversale menée auprès de représentants désignés par le département de pharmacie de chaque établissement membre d’une communauté de pratique au Québec (n = 30). Un questionnaire de 60 questions a été élaboré. Celles-ci portaient sur les bonnes pratiques de pharmacovigilance, sur la satisfaction à l’égard de la communauté de pratique, sur l’organisation locale de la pharmacovigilance et la charge de travail et sur les caractéristiques du répondant. Pour chaque bonne pratique de pharmacovigilance, les participants devaient indiquer si leur établissement était totalement conforme, partiellement conforme ou non conforme.
Résultats: Du 8 au 30 janvier 2024, 24 (80 %) des 30 établissements ont répondu au questionnaire. Les réponses de quatre établissements n’étaient toutefois pas exploitables. La somme des conformités partielles et totales aux bonnes pratiques variait de 10 % à 99 %, pour une valeur moyenne de 53 ± 24 %. La proportion d’établissements conformes par domaine de critères variait de 5 % à 60 %. Dans l’ensemble, les répondants sont satisfaits de la communauté de pratique qui contribue à soutenir les activités de pharmacovigilance au Québec.
Conclusion: Cette étude met en évidence une progression de la conformité aux bonnes pratiques de pharmacovigilance en établissement de santé.
Mots-clés: médicaments, pharmacovigilance, réactions indésirables aux médicaments
ABSTRACT
Objective: To describe the degree of compliance with good pharmacovigilance practices in healthcare institutions in Quebec in 2023. To compare these data with those collected in 2019. To assess participant satisfaction with the Quebec pharmacovigilance community of practice.
Method: This was a cross-sectional descriptive study conducted with representatives designated by the pharmacy department of each institution participating in a Quebec community of practice (n = 30). A 60 question survey was developed. The questions addressed good pharmacovigilance practices, satisfaction with the community of practice, the local organization of pharmacovigilance and workload, as well as respondent characteristics. For each good pharmacovigilance practice, participants were asked to indicate whether their institution was fully compliant, partially compliant, or noncompliant.
Results: From January 8th to 30th 2024, 24 (80%) of the 30 institutions responded to the survey. However, responses from four institutions could not be used. The combined rate of partial and full compliance with good practices ranged from 10% to 99%, with an average value of 53 ± 24%. The proportion of compliant institutions by criterion domain ranged from 5% to 60%. Overall, respondents were satisfied with the community of practice, which helps support pharmacovigilance activities in Quebec.
Conclusion: This study highlights progress in compliance with good pharmacovigilance practices in healthcare institutions
This abstract was translated using Microsoft 365 Copilot and subsequently reviewed by the editorial team.
La pharmacovigilance est définie comme étant une « branche de la pharmacologie qui se consacre à la détection, à l’évaluation, à la compréhension et à la prévention des effets indésirables des médicaments, délivrés avec ou sans ordonnance, à l’échelon individuel ou populationnel »1. Au Canada, les textes législatifs utilisent le terme « réaction indésirable à un médicament ou une drogue » (RIM). En vertu de l’article C.01.018 du Règlement sur les aliments et drogues, « le fabricant prépare un rapport de synthèse annuel sur les renseignements concernant les réactions indésirables à une drogue et les réactions indésirables graves à une drogue dont il a reçu communication ou a eu connaissance au cours des douze derniers mois »2.
En d’autres termes, chaque fabricant est tenu de déclarer à Santé Canada toutes les RIM portées à sa connaissance. De plus, en vertu de l’article 21.8 de la Loi sur les aliments et drogues, « tout établissement de soins de santé […] est tenu de fournir au ministre […] les renseignements réglementaires qui relèvent de lui concernant les RIM graves […] »3.
Dans la foulée des travaux parlementaires ayant mené au projet de Loi de Vanessa et aux changements à la Loi sur les aliments et drogues le 16 décembre 2019, l’équipe de l’Unité de recherche en pratique pharmaceutique (URPP) du Centre hospitalier universitaire Sainte-Justine (CHU Sainte-Justine) a mené des travaux afin de soutenir ces nouvelles obligations réglementaires. Par exemple, Blond et coll. ont exploré les meilleures approches d’intégration de la pharmacovigilance aux dossiers des patients4. Nichols et coll. ont étudié les déterminants de la déclaration des RIM par les cliniciens, que ce soit au niveau local ou auprès d’un organisme de réglementation5. Cerruti et coll. ont examiné les perceptions de la pharmacovigilance parmi les résidents en pharmacie, les résidents en médecine et les pharmaciens d’établissements 6,7. Rault et coll. ont également mené un Delphi afin d’établir de bonnes pratiques de pharmacovigilance hospitalière auprès des chefs de départements de pharmacie du Québec8. Soyer et coll. ont mené des travaux afin d’améliorer la codification, par les archivistes médicaux, des dossiers de patients exposés à des RIM lors d’une hospitalisation9. Enfin, Rault et coll. ont sondé les pharmaciens d’établissements de santé du Québec en 2018 afin d’établir un état des lieux de la pharmacovigilance10.
En plus de ces travaux, une communauté de pratique de pharmacovigilance a été créée par l’URPP à l’automne 2018. Cette communauté est composée de 30 établissements de santé publics du Québec. Il n’y a pas de représentants des quatre départements de pharmacie des régions nordiques (région administrative 17 et 18). Un représentant a été désigné au sein de chaque établissement de santé pour participer aux activités de la communauté, qui comprennent des réunions virtuelles environ tous les deux mois, divers projets de recherche et un partage général d’informations. Au moment de la création de la communauté de pratique, le principal défi était d’organiser les pratiques locales afin qu’elles soient conformes aux nouvelles obligations juridiques. Depuis la mise en place de la communauté de pratique, 27 réunions virtuelles ont eu lieu et ont notamment permis de discuter de pharmacovigilance, des nouveaux développements rapportés dans la littérature, des changements législatifs et surtout des initiatives spécifiques entreprises par chaque établissement québécois, mais également par des établissements d’autres provinces canadiennes et même d’autres pays. La communauté de pratique est organisée sur une base volontaire et sans financement externe11,12,13.
L’objectif primaire de cette étude était de décrire le degré de conformité aux bonnes pratiques de pharmacovigilance en établissement de santé au Québec en 2023. L’objectif secondaire était de comparer ces données à celles recueillies en 2019. Enfin, l’objectif tertiaire était d’évaluer la satisfaction des participants à l’égard de la communauté de pratique en pharmacovigilance au Québec.
Il s’agit d’une étude descriptive transversale.
L’étude a été menée auprès d’un pharmacien ou d’un professionnel de la santé désigné par le département de pharmacie de chaque établissement de santé faisant partie de la communauté de pratique en pharmacovigilance (n = 30). En acceptant de répondre à l’enquête, chaque répondant consentait à ce que les données recueillies soient compilées et utilisées à des fins de communications scientifiques. Les répondants étaient invités à répondre à l’enquête par le biais du canal de communication Microsoft Teams de la communauté de pratique en pharmacovigilance du Québec.
Une enquête originale de 57 questions a été réalisée en 2019. Cette enquête s’adressait à la même population que l’étude actuelle, soit un pharmacien ou à un professionnel de la santé désigné par le département de pharmacie de chaque établissement de santé (n = 30). De cette enquête, seules les données de la section relative aux bonnes pratiques de pharmacovigilance ont été utilisées pour la présente étude.
À partir de l’enquête originale, un nouveau questionnaire en ligne de 60 questions (hébergé sur SurveyMonkey, Palo Alto, CA, ÉUA) a été élaboré et testé par deux personnes désignées (Thaïna-Rafi Jean-Baptiste et Nicolas Martel-Côté). Trente-neuf questions portaient sur les bonnes pratiques de pharmacovigilance, réparties en six domaines : gestion des RIM (11 critères), comité local de pharmacovigilance (quatre critères), base locale de données (cinq critères), formation à la pharmacovigilance (quatre critères), outils de soutien à la déclaration de RIM (trois critères), activités de pharmacovigilance dans l’établissement (12 critères). Onze questions portaient sur la satisfaction de la communauté de pratique, cinq questions sur la description de l’organisation locale de pharmacovigilance et de la charge de travail et quatre questions sur les caractéristiques des répondants. Une dernière question permettait aux répondants de fournir des commentaires supplémentaires. Toutes les données ont été recueillies du 8 au 30 janvier 2024.
Nous avons évalué la conformité des établissements à un ensemble de bonnes pratiques de pharmacovigilance élaboré dans le cadre d’un sondage effectué auprès de tous les membres de la communauté de pratique publié en 20198.
Dans l’enquête initiale, les membres avaient été sondés sur un total de 41 critères répartis en six domaines. Toutefois, en 2023, deux de ces critères (1.10 et 4.3) ont été exclus de notre formulaire, car jugés non pertinents. Comme dans le premier sondage, les répondants étaient invités à indiquer si leur établissement de santé était totalement, partiellement ou non conforme pour chacun des 39 critères retenus.
Afin d’évaluer la satisfaction des membres de la communauté de pratique en pharmacovigilance, les répondants avaient également indiqué leur niveau de satisfaction sur une échelle de 1 (totalement insatisfait) à 10 (totalement satisfait) à l’égard de huit éléments entourant le fonctionnement de la communauté de pratique : participation des membres, horaire des téléconférences (mercredi à 15 h), durée des téléconférences (60 minutes), fréquence des téléconférences (quatre fois par année), modalités d’animation, variété des sujets discutés, modalités de partage des documents et satisfaction générale.
La conformité a quant à elle été évaluée par critère et par domaine. Pour le calcul de la conformité par domaine, un établissement de santé était considéré conforme s’il répondait « partiellement conforme » ou « totalement conforme » à plus de 75 % des critères de ce domaine. Dans le cas où un répondant était inclus dans l’analyse, mais n’avait pas fourni de réponse à un critère de bonnes pratiques de pharmacovigilance, l’établissement participant a été jugé non conforme pour ce critère.
En ce qui concerne l’évaluation de la satisfaction entourant la communauté de pratique de pharmacovigilance, le score de satisfaction (moyenne, écart-type) a été calculé pour chaque critère entourant le fonctionnement de la communauté de pratique.
Des statistiques descriptives (pourcentage, moyenne, écart-type) ont été compilées. Afin de comparer la conformité par domaine, un test de Chi-Deux a été effectué. Une valeur p inférieure à 0,05 était considérée comme statistiquement significative.
En 2024, 24 (80 %) des 30 établissements ont fourni des réponses. Les réponses de quatre établissements n’étaient toutefois pas exploitables.
Des répondants ayant fourni des réponses exploitables, 13 représentaient des établissements de santé universitaires et sept des établissements de santé non universitaires. De façon générale, les répondants ont déclaré consacrer peu de temps à la gestion de la pharmacovigilance : moins d’un jour par semaine (16/20, 80 %), un jour par semaine (2/20, 10 %) ou cinq jours par semaine (2/20, 10 %). Les répondants ont rapporté une médiane de 10 RIM déclarée par an (minimum = 0; maximum = 692).
Une minorité de répondants (9/20, 45 %) ont déclaré avoir utilisé le système de transfert SFTP (Secure File Transfer Protocol) pour déclarer les effets indésirables à Santé Canada. Divers types de fichiers ont été utilisés pour gérer les déclarations de RIM localement, notamment des feuilles de calcul Excel (16/20, 80 %), des feuilles de calcul Form (2/20, 10 %), des feuilles de calcul sur l’intranet de l’établissement (2/20, 10 %) et des feuilles de calcul Smartsheet (1/20, 5 %). La majorité des répondants se sont abonnés au nouveau bulletin d’information de Santé Canada (17/20, 85 %).
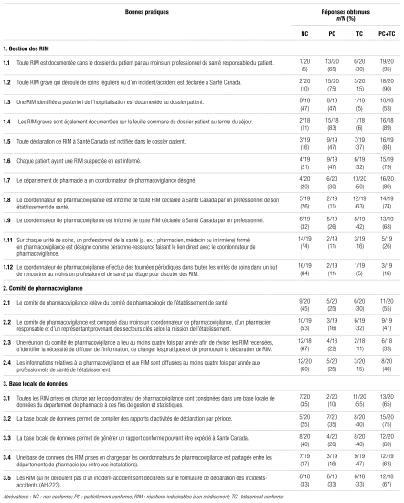
La conformité partielle par critère varie de 0 % (critère 6.6) à 83 % (critère 1.4) pour une valeur moyenne de 47 % ± 19 %. En ce qui concerne la conformité totale par critère, elle variait de 5 % (critères 1.3, 1.12, 4.2 et 4.4) à 63 % (critère 1.9) pour une valeur moyenne de 27 % ± 17 %. Quant à la conformité partielle + totale par critère, elle variait de 11 % (critère 4.4) à 95 % (critère 1.1) pour une valeur moyenne de 53 % ± 24 %. Les tableaux I (trois premiers domaines) et II (trois autres domaines) présentent le profil de conformité aux bonnes pratiques de pharmacovigilance par critère en 2023.
En ce qui concerne la proportion d’établissements conformes par domaine de critères en 2023, notre étude rapporte une conformité des établissements aux différents domaines de 5 % (domaine no 6) à 60 % (domaine no 3.). Le tableau III présente un profil du nombre d’établissements conformes aux bonnes pratiques de pharmacovigilance pour chacun des six domaines de critères en 2019 et en 2023. On note une progression de la conformité pour tous les domaines, bien qu’elle ne soit statistiquement significative que pour deux des six domaines (domaines no 1 et no 3).
En ce qui concerne la satisfaction des répondants à l’égard de la communauté de pratique en pharmacovigilance, la majorité des répondants (19/20, 95 %) a déclaré être très satisfaite de la mise en place de la communauté de pratique et souhaite qu’elle soit maintenue. Plus de la moitié des répondants (13/20, 65 %) ont déclaré qu’ils seraient désireux de présenter leurs activités à la communauté de pratique à l’avenir. Les répondants étaient de façon générale satisfaits des huit éléments entourant le fonctionnement de la communauté de pratique (tableau IV).
Cette étude présente des résultats originaux à l’égard de la mise en place d’une communauté de pratique en pharmacovigilance et la progression entourant la conformité à de bonnes pratiques de pharmacovigilance en établissement de santé au Québec.
Cohendet et coll. ont défini le concept de communauté de pratique comme étant « un groupe ayant une structure informelle, où le comportement des membres se caractérise par l’engagement volontaire dans la construction et le partage des connaissances dans un domaine donné13. Une telle communauté peut être considérée comme un dispositif de coordination permettant à ses membres d’améliorer leurs compétences individuelles, à travers l’échange d’un répertoire commun de ressources qui s’élaborent en même temps que s’articule la pratique de la communauté ». Ces auteurs ont rapporté que le concept de communautés de pratique remonte aux débuts des années quatre-vingt-dix, notamment dans les domaines de la gestion, de l’économie et de la sociologie13. Bien qu’il existe peu de littérature indexée sur le sujet, Eddy et coll. ont mené une revue systématique sur l’expérience des professionnels de la santé en matière de formation au travail d’équipe en milieu hospitalier de soins aigus14. Les auteurs ont rapporté que le partage de connaissances en équipe peut réellement contribuer à la formation des professionnels et à leur développement. Nous pensons que les communautés de pratique comme celle décrite dans cet article s’inscrivent dans cette optique de partage de connaissances contribuant à la mobilisation des acteurs en pharmacovigilance au Québec14.
Tableau I Profil de conformité aux bonnes pratiques de pharmacovigilance par critère pour les domaines de la gestion des réactions indésirables à un médicament ou une drogue, du comité local de pharmacovigilance et de la gestion de la base locale de données

Tableau II Profil de conformité aux bonnes pratiques de pharmacovigilance par critère pour les domaines de la formation en pharmacovigilance, des outils de soutien à la déclaration de RIM et des activités de pharmacovigilance
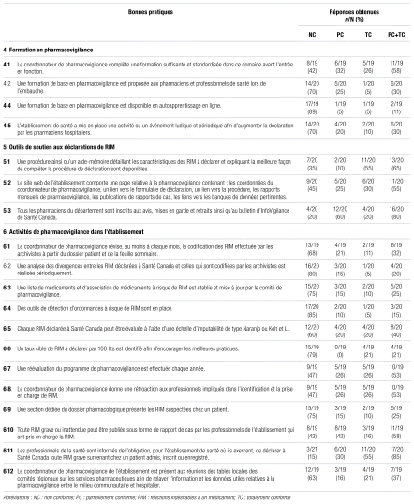
Tableau III Profil du nombre d’établissements conformes aux bonnes pratiques de pharmacovigilance pour chacun des six domaines de critères en 2019 et en 2023
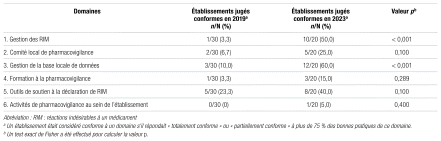
Tableau IV Satisfaction entourant la communauté de pratique en pharmacovigilance
Une majorité des répondants (65 %) provient de milieux universitaires. Sans surprise, il est plus réaliste de contribuer à des activités de pharmacovigilance en milieu universitaire, compte tenu de la taille plus grande des équipes en pharmacie, de la présence d’activités d’enseignement, de la présence d’un plus grand nombre d’étudiants et de résidents en pharmacie et de professionnels. Des 30 établissements de santé du Québec ciblés par notre enquête, on recense cinq centres hospitaliers universitaires (CHU), neuf centres intégrés universitaires de santé et de services sociaux (CIUSSS) et trois instituts universitaires; notre enquête inclut 13 répondants provenant de ces 17 établissements.
En dépit des changements apportés à la Loi sur les aliments et drogues en 2019 mettant en place l’obligation pour les établissements de santé à l’échelle du Canada de déclarer les RIM graves dans un délai de 30 jours, les répondants ont déclaré consacrer encore relativement peu de temps à la gestion de la pharmacovigilance, soit moins d’un jour par semaine pour la majorité des établissements répondants (80%). Il faut rappeler qu’il n’existe actuellement pas de recommandations entourant le temps à consacrer aux activités de pharmacovigilance en établissement de santé8. En outre, les compressions budgétaires annoncées à l’automne 2024 dans le réseau de la santé québécois ne sont pas de nature à rassurer les décideurs et cliniciens quant au respect de cette obligation fédérale de déclarer les RIM graves en établissement de santé15.
Du 16 décembre 2019 (date d’entrée en vigueur de l’obligation de déclaration des RIM graves par les établissements de santé) au 30 septembre 2024, Santé Canada a rapporté 29 089 déclarations de RIM, dont 21 761 de type grave. De toutes ces RIM, le Québec est la province en ayant rapporté le plus grand nombre en valeur absolue (7574), suivie de l’Ontario (7168) et de la Colombie-Britannique (5790)16. En ce qui a trait au nombre de RIM/million d’habitants, le Québec est la deuxième province la plus active au Canada (832 RIM/million d’habitants) après la Colombie-Britannique (1015 RIM/million d’habitants) et devant l’Ontario (424 RIM/million d’habitants)17. À titre indicatif, les répondants de notre enquête ont rapporté une médiane de 10 RIM déclarées par établissement par année [minimum = 0; maximum = 692]. Ainsi, nous pensons que les activités de la communauté de pratique ne sont pas étrangères à cette participation active du Québec à la pharmacovigilance et à la déclaration des RIM graves sur la scène canadienne.
Dans notre sondage, une minorité de répondants (47 %) a déclaré avoir utilisé le système de transfert SFTP (Secure File Transfer Protocol) pour déclarer les effets indésirables à Santé Canada, et divers modes de transmission demeurent utilisés. Nous pensons qu’une uniformisation du mode de transmission des déclarations de RIM à Santé Canada pourrait contribuer à faciliter la déclaration et, éventuellement, à accroître le nombre de RIM déclarées.
Notre étude met en évidence une conformité (partielle + totale) aux bonnes pratiques de pharmacovigilance qui varie de 10 % à 90 % pour une valeur moyenne de 53 % ± 24 %. Si la conformité est élevée pour quelques critères (p. ex., les critères 1.1, 1.2, 1.4, 1.5, 1.6, 1.7, 5.3 et 6.11), elle l’est moins pour la plupart des autres. Chaque établissement peut choisir de prioriser ses actions parmi les critères non conformes en tenant compte de ses opportunités et ressources.
Pour la conformité par domaine en 2023, on note une proportion d’établissements conformes plus élevée pour les domaines no 1 (gestion des RIM) et no 3 (gestion de la base locale de données). Compte tenu des ressources disponibles, les répondants ont rapporté cibler leurs efforts sur la gestion de la base locale de données et la gestion des RIM. La proportion d’établissements conformes est moins élevée pour les quatre autres domaines.
À notre connaissance, dans la littérature scientifique, il n’existe qu’un seul référentiel de bonnes pratiques de pharmacovigilance hospitalière, soit celui utilisé dans notre étude. Ce document a été élaboré au Québec en 2018 par les chefs de départements de pharmacie, dans le contexte des changements législatifs décrits précédemment8. Ces recommandations, établies selon une approche Delphi, a permis d’établir 41 critères (dont 39 utilisés dans la présente étude) entourant l’élaboration et l’encadrement des activités de pharmacovigilance en établissement de santé. Ainsi, il ne suffit pas d’adopter un référentiel, même localement, pour que celui-ci soit financé par le ministère de la Santé et des Services sociaux (maintenant Santé Québec) ou encore priorisé par les équipes des départements de pharmacie. En pharmacie hospitalière, les activités sont nombreuses et leur hiérarchisation demeure un défi. De plus, il faut compter plusieurs années pour qu’une majorité d’établissements de santé soit en mesure de se conformer à de nouvelles exigences. Nous pensons donc que l’adoption d’un référentiel sur les bonnes pratiques de pharmacovigilance hospitalière, combinée à la mise en place d’une communauté de pratique, a contribué au progrès entourant les activités de pharmacovigilance au Québec.
Notre enquête démontre un niveau élevé de satisfaction à l’égard de la communauté de pratique en pharmacovigilance (score moyen de 8,4). L’équipe de l’URPP du CHU Sainte-Justine assure la gestion de cette communauté de pratique sans frais pour les participants. La gestion de la communauté comprend la création et la mise à jour d’une équipe sur Microsoft Teams, la gestion des accès, la gestion d’une zone de partage de documents, la planification et l’animation de rencontres périodiques et la rédaction de comptes-rendus. Un représentant de Santé Canada est invité à chaque rencontre. Le score de satisfaction moins élevé (7,9) entourant l’élément relatif à la participation des membres vient souligner le souhait que des participants d’un plus grand nombre d’établissements de la communauté contribuent au partage de connaissances et aux présentations lors des rencontres. En outre, cette étude confirme la pertinence de poursuivre les activités de la communauté de pratique au cours des prochaines années.
Peut-on envisager de détecter et de déclarer davantage de RIM dans les prochaines années?
Au Québec, le nombre réel total de RIM ou RIM graves est inconnu. D’ailleurs, à des fins d’efficacité et de pertinence, Santé Canada s’intéresse avant tout aux RIM graves qui peuvent davantage influencer l’évolution du contenu des monographies et la pratique des cliniciens afin de prévenir ou traiter les RIM lorsqu’elles surviennent.
Au 31 mars 2024, l’Ordre des pharmaciens du Québec rapportait 10 241 membres inscrits à son tableau, dont près de 2000 exerçant en établissement de santé18. Compte tenu de ces effectifs et de l’exposition quotidienne de la majorité des pharmaciens à des patients, nous pensons que le potentiel de détection de RIM graves est bien plus élevé et que les travaux de la communauté de pratique peuvent continuer d’informer et de former les pharmaciens et autres cliniciens. En complément, dans le rapport sur les pharmacies hospitalières canadiennes pour l’exercice 2020–2021, les auteurs ont rapporté que les pharmaciens hospitaliers participaient activement à la surveillance et à la déclaration des effets indésirables potentiels et réels des médicaments et remplissaient les exigences de déclaration obligatoire (conformément à la Loi de Vanessa) dans les proportions suivantes : 24 % des répondants pour 100 % des domaines et des situations, 43 % des répondants pour 50 % à 99 % des domaines et des situations et 32 % des répondants pour 1 % à 49 % des domaines et des situations19.
En somme, il reste beaucoup à faire pour améliorer la pratique de la pharmacovigilance au Canada. Avec l’évolution du champ d’exercice des pharmaciens à travers le pays, ces professionnels de la santé sont plus que jamais sollicités pour prescrire, ajuster et cesser les thérapies médicamenteuses ainsi que pour prodiguer des soins aux patients. Si, dans les circonstances actuelles, il est difficile de prendre le temps de déclarer les RIM, nous pouvons nous attendre à ce que la situation ne s’améliore pas. Pour certains, l’informatisation des dossiers des patients pourrait être un moyen d’augmenter la déclaration des RIM; cependant, l’expérience de l’Alberta, qui a mis en œuvre un dossier de santé numérique à l’échelle de la province, ne confirme pas cette supposition, le nombre de déclarations de RIM graves restant relativement faible malgré le déploiement complété d’un dossier de santé numérique (n = 624 entre le 16 décembre 2019 et le 31 décembre 2023).
Cette étude comporte des limites. Bien que le taux de participation soit élevé (66 %), près d’un tiers des établissements de santé n’y ont pas participé contrairement à l’étude menée en 2019. Il est raisonnable de penser que les non-répondants sont moins actifs en pharmacovigilance. Il est également possible que les non-répondants soient moins satisfaits du fonctionnement de la communauté de pharmacovigilance ou que leur conformité aux bonnes pratiques de pharmacovigilance soit moins élevée.
Cette étude met en évidence une progression de la conformité aux bonnes pratiques de pharmacovigilance hospitalière. Les répondants sont satisfaits de la communauté de pratique qui contribue à soutenir les activités de pharmacovigilance au Québec.
Les auteurs n’ont déclaré aucun financement lié au présent article.
Tous les auteurs ont soumis le formulaire de l’ICMJE sur la divulgation de conflits d’intérêts potentiels. Jean-François Bussières est membre du comité de rédaction de Pharmactuel. Les autres auteurs n’ont déclaré aucun conflit d’intérêts lié au présent article.
Les auteurs n’ont pas utilisé d’outils d’intelligence artificielle dans le travail soumis.
1. Office québécois de la langue française. Grand dictionnaire terminologique. Pharmacovigilance. [en ligne] https://vitrinelinguistique.oqlf.gouv.qc.ca/fiche-gdt/fiche/8374772/pharmacovigilance (site visité le 4 mars 2025).
2. Justice Canada. Règlement sur les aliments et drogues. Article C.01.018. [en ligne] https://laws-lois.justice.gc.ca/fra/reglements/C.R.C,_ch._870/section-C.01.018.html?txthl=c.01.018 (site visité le 4 mars 2025).
3. Justice Canada. Loi sur les aliments et drogues. Article 21.8 (1). [en ligne] https://laws-lois.justice.gc.ca/fra/lois/f-27/ (site visité le 4 mars 2025).
4. Blond M, Bussières JF, Lebel D. Intégration de la pharmacovigilance au dossier pharmacologie – profil des principaux systèmes de déclaration de réactions indésirables et développement d’un outil de déclaration sur intranet dans un établissement québécois. J Pharm Clin 2006; 25(2):93–100.
5. Nichols V, Thériault-Dubé I, Touzin J, Delisle JF, Lebel D, Bussières JF et al. Risk perceptions and reasons for noncompliance in pharmacovigilance. Drug Saf 2009; 32(7) :579–90.
Crossref PubMed
6. Cerruti L, Lebel D, Bussières JF. Perceptions and practices associated with reporting adverse drug reactions among medical and pharmacy residents in Quebec. J Popul Ther Clin Pharmacol 2015; 22: e179–88.
7. Cerruti L, Lebel D, Bussières JF. Perception de la pharmacovigilance par les pharmaciens hospitaliers québécois. Ann Pharm Fr 2016; 74: 137–145.
Crossref
8. Rault P, Mégrourèche E, Labarre JS, Pettersen-Coulombe F, Lebel D, Bussières JF. Determination of good pharmacovigilance reporting practices in Quebec hospital pharmacies using a modified Delphi method. Pharmacoepidemiol Drug Saf 2019; juin 10. doi:10.1002/pds.4840
Crossref PubMed
9. Soyer J, Necsoiu D, Desjardins I, Lebel D, Bussières JF. Identification of discrepancies between adverse drug reactions coded by medical records technicians and those reported by the pharmacovigilance team in pediatrics: an intervention to improve identification, reporting and coding. Arch Pediatr 2019;26:400–6.
Crossref PubMed
10. Rault P, Mégrourèche E, Labarre JS, Pettersen-Coulombe F, Lebel D, Bussières JF. Profil de la pratique de la pharmacovigilance en établissement de santé au Québec. Pharmactuel 2019;52:172–8.
11. Duhamel A, Rault P, Lebel D, Goulet J, Charest C, Lavigne V et al. Mise en place d’une communauté de pratique en pharmacovigilance en établissement de santé au Québec. Association des pharmaciens des établissements de santé du Québec. Grand Forum 2019, Québec, Québec, Canada – 28–29 mars 2019. Pharmactuel 2019;52:139.
12. Duhamel A, Dupont C, Lebel D, Communauté de pratique en pharmacovigilance, Bussières JF. Évaluation de la satisfaction face à l’implantation d’une communauté de pratique en pharmacovigilance au Québec après 12 mois de pratique. Grand forum de l’Association des pharmaciens des établissements de santé du Québec – 19–20 mars, Québec, Québec, Canada. Pharmactuel 2020;53:157.
13. Cohendet P, Roberts J, Simon L. Créer, implanter et gérer des communautés de pratique. Gestion 2010;35 :31–35. [en ligne] https://www.cairn.info/revue-gestion-2010-4-page-31.htm (site visité le 4 mars 2025).
Crossref
14. Eddy K, Jordan Z, Stephenson M. Health professionals’ experience of teamwork education in acute hospital settings: a systematic review of qualitative literature. JBI Database System Rev Implement Rep 2016;14:96–137.
Crossref PubMed
15. Gerbet T. Coupes en santé au Québec: comment les établissements de santé feront pour recouvrer 1,5 G$. Radio-Canada. 23 novembre 2024. [en ligne] https://ici.radio-canada.ca/nouvelle/2121168/sante-quebec-deficit-milliard-cisss-ciusss (site visité le 4 mars 2025).
16. Santé Canada. Réactions indésirables graves à un médicament et incidents liés aux instruments médicaux déclarés par les hôpitaux canadiens : Résumé mensuel (2 juin 2023).. [en ligne] https://sante-infobase.canada.ca/tableau-de-bord-reactions-indesirables-hopitaux/ (site visité le 4 mars 2025).
17. Statistiques Canada. Population par province. [en ligne] https://www150.statcan.gc.ca/t1/tbl1/en/tv.action?pid=1710000901 (site visité le 4 mars 2025).
18. Ordre des pharmaciens du Québec. Rapport annuel 2023–2024. [en ligne] https://www.opq.org/documentation/rapport-annuels/ (site visité le 4 mars 2025).
19. Comité du sondage sur les pharmacies hospitalières canadiennes. Rapport du Sondage sur les pharmacies hospitalières canadiennes de 2020–21. [en ligne] https://www.cshp.ca/common/Uploaded%20files/PDFs/HPCS-2020-21-Report-FR.pdf (site visité le 4 mars 2025).
Pour toute correspondance : Mathis Laverdière, Centre hospitalier universitaire Sainte-Justine, 3175, chemin de la Côte Sainte-Catherine, Montréal, Québec, Canada; téléphone : 514-345-4603; courriel : mathis.laverdiere.hsj@ssss.gouv.qc.ca
PHARMACTUEL, Vol. 59, No. 1, 2026